苯乙烯是一种重要的有机化工原料,可广泛用于合成橡胶,工程塑料及制药等。工业上可通过乙苯催化脱氢来制取苯乙烯,反应方程式如下:
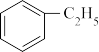 (g)
(g)
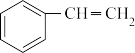 (g)+H2(g) ΔH
(g)+H2(g) ΔH
(1)已知部分物质的燃烧热数据如下表:
则
_______ 。
(2)下列关于反应的说法正确的是_______(填序号)
(3)工业装置通常采用铁基氧化物催化剂,通入过热水蒸气(615~645℃)、水油比(水与乙苯质量比)1.4~1.8、常压的条件下发生乙苯的催化脱氢反应。
①反应中通入水蒸气的作用是_______ 。
②将物质的量分数组成为m%乙苯(g)、n% 的气体通入反应器,在温度t、压强p下进行反应。平衡时,乙苯的转化率为
的气体通入反应器,在温度t、压强p下进行反应。平衡时,乙苯的转化率为 ,则苯乙烯的分压为
,则苯乙烯的分压为_______ ,平衡常数
_______ (以分压表示,分压=总压×物质的量分数)
(4)近年来,有研究者发现若将上述生产过程中通入 改为通入
改为通入 ,通入
,通入 后会发生反应
后会发生反应 。在常压下,分别按投料比为仅乙苯,乙苯
。在常压下,分别按投料比为仅乙苯,乙苯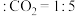 ,乙苯
,乙苯 ,测得乙苯的平衡转化率与温度的关系如下图。
,测得乙苯的平衡转化率与温度的关系如下图。
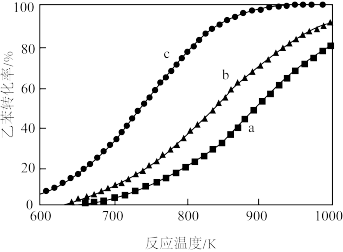
则乙苯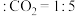 对应的曲线为
对应的曲线为_______ (填“a”,“b”或“c”),理由是_______ 。
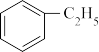 (g)
(g)
 (g)+H2(g) ΔH
(g)+H2(g) ΔH(1)已知部分物质的燃烧热数据如下表:
| 物质 | 乙苯 | 苯乙烯 | 氢气 |
燃烧热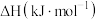 | -4610.2 | -4441.8 | -285.8 |

(2)下列关于反应的说法正确的是_______(填序号)
| A.高温有利于反应自发进行 |
| B.工业生产中应尽可能提高反应温度,并增大压强,以提高原料的利用率 |
| C.恒温恒容条件下,反应达到平衡后,向体系中再充入乙苯蒸气,乙苯的转化率将增大 |
| D.选择合适的催化剂可以缩短达到平衡的时间,但不会提高生成物中苯乙烯的含量 |
①反应中通入水蒸气的作用是
②将物质的量分数组成为m%乙苯(g)、n%
 的气体通入反应器,在温度t、压强p下进行反应。平衡时,乙苯的转化率为
的气体通入反应器,在温度t、压强p下进行反应。平衡时,乙苯的转化率为 ,则苯乙烯的分压为
,则苯乙烯的分压为
(4)近年来,有研究者发现若将上述生产过程中通入
 改为通入
改为通入 ,通入
,通入 后会发生反应
后会发生反应 。在常压下,分别按投料比为仅乙苯,乙苯
。在常压下,分别按投料比为仅乙苯,乙苯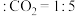 ,乙苯
,乙苯 ,测得乙苯的平衡转化率与温度的关系如下图。
,测得乙苯的平衡转化率与温度的关系如下图。
则乙苯
 对应的曲线为
对应的曲线为
更新时间:2022-04-23 12:29:24
|
相似题推荐
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
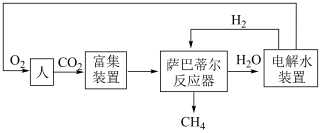
【推荐1】某空间站利用萨巴蒂尔反应: ,配合水的电解实现氧气再生的流程简图如下。
,配合水的电解实现氧气再生的流程简图如下。
(1)已知:电解液态水制备1mol ,电解反应的
,电解反应的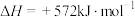 。由此计算
。由此计算 的摩尔燃烧焓
的摩尔燃烧焓
___________  。
。
(2)已知:萨巴蒂尔反应的平衡常数(K)与反应温度(t)之间的关系如图。
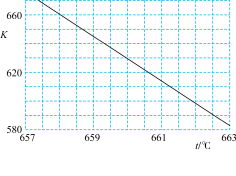
①萨巴蒂尔反应在___________ (选填“高温”或“低温”)下能自发进行。
②某研究小组模拟该反应,温度t下,向容积为10L的密闭容器中通入0.1mol 和0.4mol
和0.4mol ,反应平衡后测得容器中
,反应平衡后测得容器中 。则
。则 的转化率为
的转化率为______ ,反应温度t约为____ ℃。
(3)在相同条件下, 与
与 还会发生不利于氧循环的副反应:
还会发生不利于氧循环的副反应:
 ,在反应器中按
,在反应器中按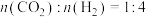 通入反应物在不同温度、不同催化剂条件下,反应进行到2min时,测得反应器中
通入反应物在不同温度、不同催化剂条件下,反应进行到2min时,测得反应器中 、
、 浓度
浓度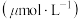 如表。
如表。
若选用催化剂Ⅰ,在350℃条件下反应,0~2min生成 的平均反应速率为
的平均反应速率为_____ 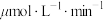 ;结合表格信息分析,从提高循环系统制氧效率的角度,反应器的最佳反应条件应选择催化剂
;结合表格信息分析,从提高循环系统制氧效率的角度,反应器的最佳反应条件应选择催化剂___________ (填“Ⅰ”或“Ⅱ”)和
___________ 。
(4)令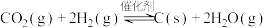 代替萨巴蒂尔反应,虽可实现氢、氧元素完全循环利用,但使用一段时间后催化剂的催化效果会明显下降,其原因是
代替萨巴蒂尔反应,虽可实现氢、氧元素完全循环利用,但使用一段时间后催化剂的催化效果会明显下降,其原因是___________ 。
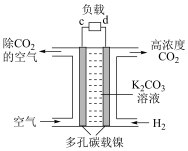
(5)“富集装置”可利用电化学法富集空间站内“空气”中的 作为萨巴蒂尔反应器的原料气之一,装置如右图。a极为
作为萨巴蒂尔反应器的原料气之一,装置如右图。a极为______ 极(填“正”或“负”),b电极上发生的电极反应为___________ 。
 ,配合水的电解实现氧气再生的流程简图如下。
,配合水的电解实现氧气再生的流程简图如下。
(1)已知:电解液态水制备1mol
 ,电解反应的
,电解反应的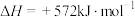 。由此计算
。由此计算 的摩尔燃烧焓
的摩尔燃烧焓
 。
。(2)已知:萨巴蒂尔反应的平衡常数(K)与反应温度(t)之间的关系如图。

①萨巴蒂尔反应在
②某研究小组模拟该反应,温度t下,向容积为10L的密闭容器中通入0.1mol
 和0.4mol
和0.4mol ,反应平衡后测得容器中
,反应平衡后测得容器中 。则
。则 的转化率为
的转化率为(3)在相同条件下,
 与
与 还会发生不利于氧循环的副反应:
还会发生不利于氧循环的副反应: ,在反应器中按
,在反应器中按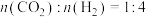 通入反应物在不同温度、不同催化剂条件下,反应进行到2min时,测得反应器中
通入反应物在不同温度、不同催化剂条件下,反应进行到2min时,测得反应器中 、
、 浓度
浓度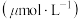 如表。
如表。| 催化剂 | 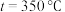 | 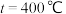 | ||
 |  |  |  | |
| 催化剂Ⅰ | 10.8 | 12722 | 345.2 | 42780 |
| 催化剂Ⅱ | 9.2 | 10775 | 34 | 38932 |
 的平均反应速率为
的平均反应速率为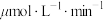 ;结合表格信息分析,从提高循环系统制氧效率的角度,反应器的最佳反应条件应选择催化剂
;结合表格信息分析,从提高循环系统制氧效率的角度,反应器的最佳反应条件应选择催化剂
(4)令
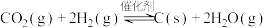 代替萨巴蒂尔反应,虽可实现氢、氧元素完全循环利用,但使用一段时间后催化剂的催化效果会明显下降,其原因是
代替萨巴蒂尔反应,虽可实现氢、氧元素完全循环利用,但使用一段时间后催化剂的催化效果会明显下降,其原因是(5)“富集装置”可利用电化学法富集空间站内“空气”中的
 作为萨巴蒂尔反应器的原料气之一,装置如右图。a极为
作为萨巴蒂尔反应器的原料气之一,装置如右图。a极为
您最近一年使用:0次
【推荐2】苯乙烯是生产塑料和合成橡胶的重要有机原料,国内外目前生产苯乙烯的方法主要是乙苯催化脱氢法,反应方程式为:
(1)已知部分物质的燃烧热数据如下表,利用表中数据计算
_______ (用a、b、c表示) 。
。
(2)实际生产过程中,通常向乙苯中掺混氮气( 不参与反应),保持体系总压为100kPa下进行反应,不同投料比m下乙苯的平衡转化率随反应温度变化关系如图所示。(其中投料比m为原料气中乙苯和
不参与反应),保持体系总压为100kPa下进行反应,不同投料比m下乙苯的平衡转化率随反应温度变化关系如图所示。(其中投料比m为原料气中乙苯和 的物质的量之比,取值分别为1∶0、1∶1、1∶5、1∶9)
的物质的量之比,取值分别为1∶0、1∶1、1∶5、1∶9)
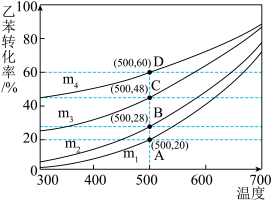
①在乙苯中掺混氮气的目的是_______ 。
②投料比m为1∶0的曲线是_______ (填曲线标号)。
③若一定的投料比,反应温度恒定时,并保持体系总压为常压的条件下进行反应,下列事实能作为该反应达到平衡的依据的是_______ (填字母)。
A.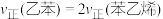
B.容器内气体密度不再变化
C.容器内苯乙烯与 的分子数之比不再变化
的分子数之比不再变化
D.容器内气体的平均相对分子质量不再变化
(3)近年来,有研究者发现若将上述生产过程中通入 改为通入
改为通入 ,在
,在 气氛中乙苯催化脱氢制苯乙烯更容易进行,反应历程如图:
气氛中乙苯催化脱氢制苯乙烯更容易进行,反应历程如图:

①该过程中发生反应的化学方程式为_______ 。
②根据反应历程分析,催化剂表面酸碱性对乙苯脱氢反应性能影响较大,如果催化剂表面碱性太强,会降低乙苯的转化率,碱性太强使乙苯转化率降低的原因是_______ (说出一点即可)。
③在600℃下,向恒容密闭容器中充入2mol乙苯和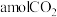 ,平衡时乙苯的转化率为50%,且容器内气体总物质的量为5mol,则
,平衡时乙苯的转化率为50%,且容器内气体总物质的量为5mol,则
_______ 。

(1)已知部分物质的燃烧热数据如下表,利用表中数据计算

 。
。| 物质 | 燃烧热 |
| 乙苯 |  |
| 苯乙烯 |  |
| 氢气 | 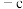 |
(2)实际生产过程中,通常向乙苯中掺混氮气(
 不参与反应),保持体系总压为100kPa下进行反应,不同投料比m下乙苯的平衡转化率随反应温度变化关系如图所示。(其中投料比m为原料气中乙苯和
不参与反应),保持体系总压为100kPa下进行反应,不同投料比m下乙苯的平衡转化率随反应温度变化关系如图所示。(其中投料比m为原料气中乙苯和 的物质的量之比,取值分别为1∶0、1∶1、1∶5、1∶9)
的物质的量之比,取值分别为1∶0、1∶1、1∶5、1∶9)
①在乙苯中掺混氮气的目的是
②投料比m为1∶0的曲线是
③若一定的投料比,反应温度恒定时,并保持体系总压为常压的条件下进行反应,下列事实能作为该反应达到平衡的依据的是
A.
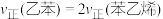
B.容器内气体密度不再变化
C.容器内苯乙烯与
 的分子数之比不再变化
的分子数之比不再变化 D.容器内气体的平均相对分子质量不再变化
(3)近年来,有研究者发现若将上述生产过程中通入
 改为通入
改为通入 ,在
,在 气氛中乙苯催化脱氢制苯乙烯更容易进行,反应历程如图:
气氛中乙苯催化脱氢制苯乙烯更容易进行,反应历程如图:
①该过程中发生反应的化学方程式为
②根据反应历程分析,催化剂表面酸碱性对乙苯脱氢反应性能影响较大,如果催化剂表面碱性太强,会降低乙苯的转化率,碱性太强使乙苯转化率降低的原因是
③在600℃下,向恒容密闭容器中充入2mol乙苯和
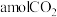 ,平衡时乙苯的转化率为50%,且容器内气体总物质的量为5mol,则
,平衡时乙苯的转化率为50%,且容器内气体总物质的量为5mol,则
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐3】乙醇是一种清洁替代能源,催化加氢制备乙醇技术是当前的研究热点。
(1) 催化加氢制备乙醇的反应为
催化加氢制备乙醇的反应为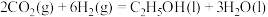
①若要计算上述反应的 ,须查阅的两个数据是
,须查阅的两个数据是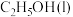 的燃烧热和
的燃烧热和__________ ,该反应的
__________ (填“>”“<”或“=”)0;
②某金属有机骨架负载的铜基催化剂上, 加氢生成
加氢生成 的部分反应机理如图所示;
的部分反应机理如图所示; 过程中两个
过程中两个 均参与反应,X的结构式为
均参与反应,X的结构式为__________ (填标号)。
反应I:
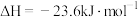
反应Ⅱ:
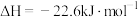
在其他条件不变时,将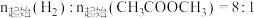 的混合气体以一定流速通入装有铜基催化剂的反应管,测得
的混合气体以一定流速通入装有铜基催化剂的反应管,测得 转化率、
转化率、 选择性
选择性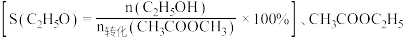 选择性
选择性
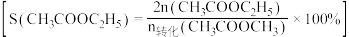 随温度的变化如图所示.
随温度的变化如图所示. 与
与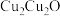 的晶胞如图所示(立方体),
的晶胞如图所示(立方体), 晶体的密度可表示为
晶体的密度可表示为__________  (用含
(用含 的代数式表示,
的代数式表示, 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。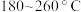 下均有
下均有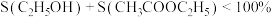 ,其原因是
,其原因是__________ ;
③ 范围内,
范围内, 转化率随温度升高而迅速增大的主要原因是
转化率随温度升高而迅速增大的主要原因是__________ ;
④温度高于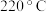 时,催化剂的催化活性下降,其原因可能是
时,催化剂的催化活性下降,其原因可能是__________ 。
(3)一定条件下,在 密闭容器内通入
密闭容器内通入 和
和 发生反应I和Ⅱ,测得
发生反应I和Ⅱ,测得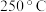 下达到平衡时
下达到平衡时 转化率为
转化率为 ,乙醇选择性为
,乙醇选择性为 .
.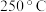 时,反应1的平衡常数
时,反应1的平衡常数
__________ 。
(1)
 催化加氢制备乙醇的反应为
催化加氢制备乙醇的反应为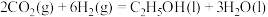
①若要计算上述反应的
 ,须查阅的两个数据是
,须查阅的两个数据是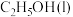 的燃烧热和
的燃烧热和
②某金属有机骨架负载的铜基催化剂上,
 加氢生成
加氢生成 的部分反应机理如图所示;
的部分反应机理如图所示;
 过程中两个
过程中两个 均参与反应,X的结构式为
均参与反应,X的结构式为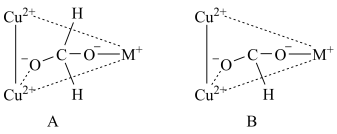
反应I:

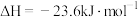
反应Ⅱ:

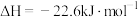
在其他条件不变时,将
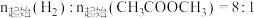 的混合气体以一定流速通入装有铜基催化剂的反应管,测得
的混合气体以一定流速通入装有铜基催化剂的反应管,测得 转化率、
转化率、 选择性
选择性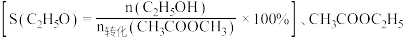 选择性
选择性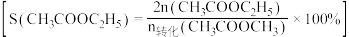 随温度的变化如图所示.
随温度的变化如图所示.
 与
与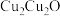 的晶胞如图所示(立方体),
的晶胞如图所示(立方体), 晶体的密度可表示为
晶体的密度可表示为 (用含
(用含 的代数式表示,
的代数式表示, 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。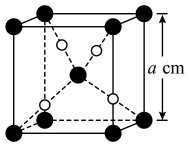
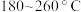 下均有
下均有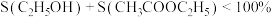 ,其原因是
,其原因是③
 范围内,
范围内, 转化率随温度升高而迅速增大的主要原因是
转化率随温度升高而迅速增大的主要原因是④温度高于
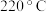 时,催化剂的催化活性下降,其原因可能是
时,催化剂的催化活性下降,其原因可能是(3)一定条件下,在
 密闭容器内通入
密闭容器内通入 和
和 发生反应I和Ⅱ,测得
发生反应I和Ⅱ,测得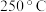 下达到平衡时
下达到平衡时 转化率为
转化率为 ,乙醇选择性为
,乙醇选择性为 .
.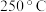 时,反应1的平衡常数
时,反应1的平衡常数
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐1】一碳化学以研究处理、利用 、
、 、
、 等重要气态物质为主要任务,在建设生态文明和应对能源危机等具有重要意义。
等重要气态物质为主要任务,在建设生态文明和应对能源危机等具有重要意义。
Ⅰ.开发 直接催化加氢合成二甲醚技术是很好的一个研究方向。
直接催化加氢合成二甲醚技术是很好的一个研究方向。
主反应:
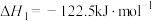
副反应:

(1)一定温度下,将 与
与 以体积比1:2置于恒容密闭容器中且只发生主反应,到达平衡后,其他条件不变,以下措施一定能提高
以体积比1:2置于恒容密闭容器中且只发生主反应,到达平衡后,其他条件不变,以下措施一定能提高 平衡转化率的是_______。
平衡转化率的是_______。
(2)催化剂作用下,恒温恒压(250℃、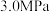 )密闭容器中以
)密闭容器中以 充入反应气,反应平衡时测得
充入反应气,反应平衡时测得 的转化率为20%,二甲醚的选择性为80%[已知二甲醚的选择性=
的转化率为20%,二甲醚的选择性为80%[已知二甲醚的选择性=  ×100%,则副反应
×100%,则副反应 的
的
_______ (保留三位小数)(提示:平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
Ⅱ.以 、水蒸气、生石灰为原料可以大规模制取氢气:
、水蒸气、生石灰为原料可以大规模制取氢气:
水气重整:

水汽变换:
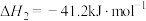
吸附反应:

图1为一定条件下,相同时间内无 、微米级
、微米级 参与的制氢反应氢气体积分数%对比曲线图;图2为其他条件不变,相同时间内800℃下不同级别
参与的制氢反应氢气体积分数%对比曲线图;图2为其他条件不变,相同时间内800℃下不同级别 对氢气体积分数的影响柱状图:
对氢气体积分数的影响柱状图:

(3)下列关于图1的叙述正确的是_______。
(4)根据图1、图2并结合反应的化学方程式,分析使用微米级 与纳米级
与纳米级 后
后 体积分数不同的重要原因
体积分数不同的重要原因_______ 。
(5)因为普通纳米级 在533℃会因烧结而完全丧失吸附性,故图2中的纳米
在533℃会因烧结而完全丧失吸附性,故图2中的纳米 采用的是
采用的是 改性的
改性的 ,在图1中画出未经改性的纳米级
,在图1中画出未经改性的纳米级 参与吸附的450~600℃范围内的氢气体积分数变化曲线
参与吸附的450~600℃范围内的氢气体积分数变化曲线_______ 。
 、
、 、
、 等重要气态物质为主要任务,在建设生态文明和应对能源危机等具有重要意义。
等重要气态物质为主要任务,在建设生态文明和应对能源危机等具有重要意义。Ⅰ.开发
 直接催化加氢合成二甲醚技术是很好的一个研究方向。
直接催化加氢合成二甲醚技术是很好的一个研究方向。主反应:

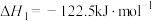
副反应:


(1)一定温度下,将
 与
与 以体积比1:2置于恒容密闭容器中且只发生主反应,到达平衡后,其他条件不变,以下措施一定能提高
以体积比1:2置于恒容密闭容器中且只发生主反应,到达平衡后,其他条件不变,以下措施一定能提高 平衡转化率的是_______。
平衡转化率的是_______。| A.升高温度 | B.使用催化剂 |
C.增大投料比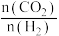 | D.将恒容容器改为恒压容器 |
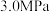 )密闭容器中以
)密闭容器中以 充入反应气,反应平衡时测得
充入反应气,反应平衡时测得 的转化率为20%,二甲醚的选择性为80%[已知二甲醚的选择性=
的转化率为20%,二甲醚的选择性为80%[已知二甲醚的选择性=  ×100%,则副反应
×100%,则副反应 的
的
Ⅱ.以
 、水蒸气、生石灰为原料可以大规模制取氢气:
、水蒸气、生石灰为原料可以大规模制取氢气:水气重整:


水汽变换:

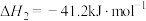
吸附反应:


图1为一定条件下,相同时间内无
 、微米级
、微米级 参与的制氢反应氢气体积分数%对比曲线图;图2为其他条件不变,相同时间内800℃下不同级别
参与的制氢反应氢气体积分数%对比曲线图;图2为其他条件不变,相同时间内800℃下不同级别 对氢气体积分数的影响柱状图:
对氢气体积分数的影响柱状图:
(3)下列关于图1的叙述正确的是_______。
A.图中虚线是有 参与的制氢过程 参与的制氢过程 |
B.加生石灰的作用之一是吸收 可以使水汽变换限度增大 可以使水汽变换限度增大 |
| C.吸附反应只是通过系统能量互补,达到降低制氢能耗的目的 |
| D.图中实线与虚线随着温度升高会逐渐靠拢,主要原因是高温下水汽变换反应不自发 |
 与纳米级
与纳米级 后
后 体积分数不同的重要原因
体积分数不同的重要原因(5)因为普通纳米级
 在533℃会因烧结而完全丧失吸附性,故图2中的纳米
在533℃会因烧结而完全丧失吸附性,故图2中的纳米 采用的是
采用的是 改性的
改性的 ,在图1中画出未经改性的纳米级
,在图1中画出未经改性的纳米级 参与吸附的450~600℃范围内的氢气体积分数变化曲线
参与吸附的450~600℃范围内的氢气体积分数变化曲线
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐2】血红蛋白(Hb)和肌红蛋白(Mb)分别存在于血液和肌肉中,都能与氧气结合,与氧气的结合度a(吸附O2的Hb或Mb的量占总Hb或Mb的量的比值)和氧气分压p(O2)密切相关。请回答下列问题:
(1)人体中的血红蛋白(Hb)能吸附O2、H+,相关反应的热化学方程式及平衡常数如下:
Ⅰ.Hb(aq)+H+(aq) HbH+(aq) ΔH1
HbH+(aq) ΔH1
Ⅱ.HbH+(aq)+O2(g) HbO2(aq)+H+(aq) ΔH2
HbO2(aq)+H+(aq) ΔH2
Ⅲ.Hb(aq)+O2(g) HbO2(aq) ΔH3
HbO2(aq) ΔH3
ΔH3 =_______ (用ΔH1、ΔH2表示),K3=_______ (用K1、K2表示)
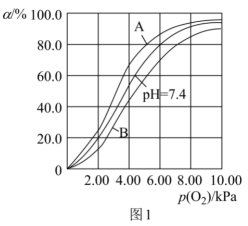
(2)Hb与氧气的结合能力受到c(H+)的影响,相关反应如下:HbO2(aq)+H+(aq) HbH+(aq)+O2(g)。37 ℃,pH分别为7.2、7.4、7.6时氧气分压p(O2)与达到平衡时Hb与氧气的结合度a的关系如图1所示,pH=7.6时对应的曲线为
HbH+(aq)+O2(g)。37 ℃,pH分别为7.2、7.4、7.6时氧气分压p(O2)与达到平衡时Hb与氧气的结合度a的关系如图1所示,pH=7.6时对应的曲线为__________ (填“A”或“B”)。
(3)Mb与氧气结合的反应如下:Mb(aq)+O2(g) MbO2(aq) ΔH,37 ℃时,氧气分压p (O2)与达平衡时Mb与氧气的结合度a的关系如图2所示。
MbO2(aq) ΔH,37 ℃时,氧气分压p (O2)与达平衡时Mb与氧气的结合度a的关系如图2所示。
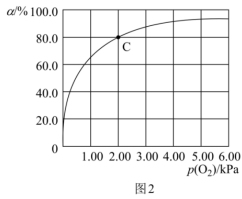
①已知Mb与氧气结合的平衡常数的表达式K= ,计算37 ℃时K=
,计算37 ℃时K=_______ kPa-1。
②人正常呼吸时,体温约为37 ℃,氧气分压约为20.00 kPa,计算此时Mb与氧气的最大结合度为_______ (结果保留3位有效数字)。
③经测定,体温升高,Mb与氧气的结合度降低,则该反应的ΔH_______ (填“>”或“<”)0。
④已知37 ℃时,上述反应的正反应速率v(正)=k1·c(Mb)·p(O2),逆反应速率v(逆)=k2·c(MbO2),若k1=120 s-1·kPa-1,则k2=_______ 。
(1)人体中的血红蛋白(Hb)能吸附O2、H+,相关反应的热化学方程式及平衡常数如下:
Ⅰ.Hb(aq)+H+(aq)
 HbH+(aq) ΔH1
HbH+(aq) ΔH1 Ⅱ.HbH+(aq)+O2(g)
 HbO2(aq)+H+(aq) ΔH2
HbO2(aq)+H+(aq) ΔH2 Ⅲ.Hb(aq)+O2(g)
 HbO2(aq) ΔH3
HbO2(aq) ΔH3 ΔH3 =
(2)Hb与氧气的结合能力受到c(H+)的影响,相关反应如下:HbO2(aq)+H+(aq)
 HbH+(aq)+O2(g)。37 ℃,pH分别为7.2、7.4、7.6时氧气分压p(O2)与达到平衡时Hb与氧气的结合度a的关系如图1所示,pH=7.6时对应的曲线为
HbH+(aq)+O2(g)。37 ℃,pH分别为7.2、7.4、7.6时氧气分压p(O2)与达到平衡时Hb与氧气的结合度a的关系如图1所示,pH=7.6时对应的曲线为
(3)Mb与氧气结合的反应如下:Mb(aq)+O2(g)
 MbO2(aq) ΔH,37 ℃时,氧气分压p (O2)与达平衡时Mb与氧气的结合度a的关系如图2所示。
MbO2(aq) ΔH,37 ℃时,氧气分压p (O2)与达平衡时Mb与氧气的结合度a的关系如图2所示。
①已知Mb与氧气结合的平衡常数的表达式K=
 ,计算37 ℃时K=
,计算37 ℃时K=②人正常呼吸时,体温约为37 ℃,氧气分压约为20.00 kPa,计算此时Mb与氧气的最大结合度为
③经测定,体温升高,Mb与氧气的结合度降低,则该反应的ΔH
④已知37 ℃时,上述反应的正反应速率v(正)=k1·c(Mb)·p(O2),逆反应速率v(逆)=k2·c(MbO2),若k1=120 s-1·kPa-1,则k2=
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐3】 循环再利用制备甲烷、甲醇等有机燃料,变废为宝历来是化学重要的研究领域。为了减少
循环再利用制备甲烷、甲醇等有机燃料,变废为宝历来是化学重要的研究领域。为了减少 的排放,可用下列方法把
的排放,可用下列方法把 转化成燃料,试回答下列问题:
转化成燃料,试回答下列问题:
a.

b.
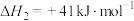
(1)已知c.
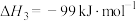 ,则
,则
___________  ;反应a在
;反应a在___________ (选填“高温”、“低温”或“任意温度”)下,易自发进行。
(2)向刚性容器中充入一定量的 和
和 ,在不同催化剂(Cat.1,Cat.2)下经相同反应时间,
,在不同催化剂(Cat.1,Cat.2)下经相同反应时间, 的转化率和甲醇的选择性[甲醇的选择性
的转化率和甲醇的选择性[甲醇的选择性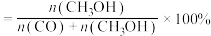 ]随温度的变化如图:
]随温度的变化如图:
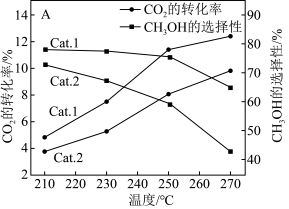
①由图可知,催化效果Cat.1___________ Cat.2(填“>”“<”或“=”)。
②在210~270℃间, 的选择性随温度的升高而下降,请写出一条可能原因
的选择性随温度的升高而下降,请写出一条可能原因___________ 。
(3)一定条件下,向刚性容器中充入物质的量之比为1:3的 和
和 发生上述反应。
发生上述反应。
①有利于提高甲醇平衡产率的条件是___________ (填标号)。
A.高温高压 B.低温高压 C.高温低压 D.低温低压
②达到平衡时 的转化率为20%,
的转化率为20%, 的选择性为75%,则
的选择性为75%,则 的转化率为
的转化率为___________ ;反应b的压强平衡常数
___________ 。(压强平衡常数为用分压表示的化学平衡常数,分压=总压×物质的量分数)
 循环再利用制备甲烷、甲醇等有机燃料,变废为宝历来是化学重要的研究领域。为了减少
循环再利用制备甲烷、甲醇等有机燃料,变废为宝历来是化学重要的研究领域。为了减少 的排放,可用下列方法把
的排放,可用下列方法把 转化成燃料,试回答下列问题:
转化成燃料,试回答下列问题:a.


b.

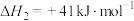
(1)已知c.

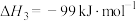 ,则
,则
 ;反应a在
;反应a在(2)向刚性容器中充入一定量的
 和
和 ,在不同催化剂(Cat.1,Cat.2)下经相同反应时间,
,在不同催化剂(Cat.1,Cat.2)下经相同反应时间, 的转化率和甲醇的选择性[甲醇的选择性
的转化率和甲醇的选择性[甲醇的选择性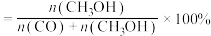 ]随温度的变化如图:
]随温度的变化如图:
①由图可知,催化效果Cat.1
②在210~270℃间,
 的选择性随温度的升高而下降,请写出一条可能原因
的选择性随温度的升高而下降,请写出一条可能原因(3)一定条件下,向刚性容器中充入物质的量之比为1:3的
 和
和 发生上述反应。
发生上述反应。①有利于提高甲醇平衡产率的条件是
A.高温高压 B.低温高压 C.高温低压 D.低温低压
②达到平衡时
 的转化率为20%,
的转化率为20%, 的选择性为75%,则
的选择性为75%,则 的转化率为
的转化率为
您最近一年使用:0次
【推荐1】开发CO2催化加氢合成二甲醚技术是有效利用CO2资源,实现“碳达峰、碳中和”目标的重要途径。
(1)已知:①CO2(g) + 3H2(g) CH3OH(g)+ H2O(g) ΔH= - 49.01 kJ·mol‑1
CH3OH(g)+ H2O(g) ΔH= - 49.01 kJ·mol‑1
②2CH3OH(g) CH3OCH3(g) + H2O(g) ΔH= - 24.52 kJ·mol-1
CH3OCH3(g) + H2O(g) ΔH= - 24.52 kJ·mol-1
则CO2催化加氢直接合成二甲醚反应的热化学方程式为_______ 。
(2)CO2催化加氢直接合成二甲醚时还会发生副反应:CO2(g)+H2(g) CO(g)+H2O(g) △H =+41.2 kJ ·mol-1,其他条件相同时,反应温度对CO2平衡总转化率及反应2.5小时的CO2实际总转化率影响如图-1所示; 反应温度对二甲醚的平衡选择性及反应2.5小时的二甲醚实际选择性影响如图2所示。(已知: CH3OCH3的选择性=
CO(g)+H2O(g) △H =+41.2 kJ ·mol-1,其他条件相同时,反应温度对CO2平衡总转化率及反应2.5小时的CO2实际总转化率影响如图-1所示; 反应温度对二甲醚的平衡选择性及反应2.5小时的二甲醚实际选择性影响如图2所示。(已知: CH3OCH3的选择性= ×100% )。
×100% )。

①图-1中,温度高于290℃,CO2平衡总转化率随温度升高而上升的原因可能是_______ 。
②图-2中,在240℃~ 300℃范围内,相同温度下,二甲醚的实际选择性高于其平衡值,从化学反应速率的角度解释原因_______ 。
(3)我国科研团队研究发现使用GaZrOx双金属氧化物可形成氧空位具有催化氧化性能,实现CO2加氢制二甲醚(DME)同时可获得甲醇(MT)。氧空位和Zr3+离子均参与CO2的活化,氧空位用于捕获CO2,同时Zr3+将电子转移给CO2形成激活的CO2分子,随后活化的CO2插入Ga- H键中,从而产生关键中间体表面甲酸盐物种。其反应机理如图-3所示:

Zr基态原子核外电子排布式为[Kr]4d25s2,中间产物c中,元素Zr、Ga 化合价分别为_______ 。
(4)一种二甲醚和CO2直接制备碳酸二甲酯( )的电化学方法如图-4所示: b极的电极反应式为
)的电化学方法如图-4所示: b极的电极反应式为_______ 。

(1)已知:①CO2(g) + 3H2(g)
 CH3OH(g)+ H2O(g) ΔH= - 49.01 kJ·mol‑1
CH3OH(g)+ H2O(g) ΔH= - 49.01 kJ·mol‑1②2CH3OH(g)
 CH3OCH3(g) + H2O(g) ΔH= - 24.52 kJ·mol-1
CH3OCH3(g) + H2O(g) ΔH= - 24.52 kJ·mol-1则CO2催化加氢直接合成二甲醚反应的热化学方程式为
(2)CO2催化加氢直接合成二甲醚时还会发生副反应:CO2(g)+H2(g)
 CO(g)+H2O(g) △H =+41.2 kJ ·mol-1,其他条件相同时,反应温度对CO2平衡总转化率及反应2.5小时的CO2实际总转化率影响如图-1所示; 反应温度对二甲醚的平衡选择性及反应2.5小时的二甲醚实际选择性影响如图2所示。(已知: CH3OCH3的选择性=
CO(g)+H2O(g) △H =+41.2 kJ ·mol-1,其他条件相同时,反应温度对CO2平衡总转化率及反应2.5小时的CO2实际总转化率影响如图-1所示; 反应温度对二甲醚的平衡选择性及反应2.5小时的二甲醚实际选择性影响如图2所示。(已知: CH3OCH3的选择性= ×100% )。
×100% )。
①图-1中,温度高于290℃,CO2平衡总转化率随温度升高而上升的原因可能是
②图-2中,在240℃~ 300℃范围内,相同温度下,二甲醚的实际选择性高于其平衡值,从化学反应速率的角度解释原因
(3)我国科研团队研究发现使用GaZrOx双金属氧化物可形成氧空位具有催化氧化性能,实现CO2加氢制二甲醚(DME)同时可获得甲醇(MT)。氧空位和Zr3+离子均参与CO2的活化,氧空位用于捕获CO2,同时Zr3+将电子转移给CO2形成激活的CO2分子,随后活化的CO2插入Ga- H键中,从而产生关键中间体表面甲酸盐物种。其反应机理如图-3所示:

Zr基态原子核外电子排布式为[Kr]4d25s2,中间产物c中,元素Zr、Ga 化合价分别为
(4)一种二甲醚和CO2直接制备碳酸二甲酯(
 )的电化学方法如图-4所示: b极的电极反应式为
)的电化学方法如图-4所示: b极的电极反应式为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐2】化学反应速率和限度与生产、生活密切相关。
Ⅰ.用纯净的锌粒与稀盐酸反应制取氢气,请回答:
(1)实验过程如图所示,分析判断_______ 段化学反应速率最快(答“O~E”、“E~F”或“F~G”)。
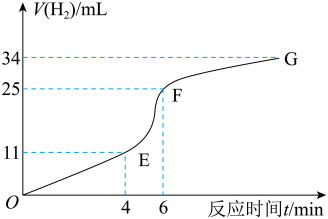
(2)将锌粒投入盛有稀盐酸的烧杯中,刚开始时产生 的速率逐渐加快,其原因是
的速率逐渐加快,其原因是_______ 。
Ⅱ.一定温度下,在体积为0.5L的恒容密闭容器中, 和之间发生反应:
和之间发生反应: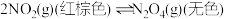 ,反应过程中各物质的物质的量与时间的关系如图所示。回答下列问题:
,反应过程中各物质的物质的量与时间的关系如图所示。回答下列问题:
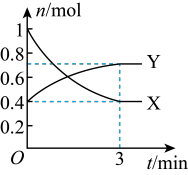
(3)曲线_______ (填“X”或“Y”)表示 的物质的量随时间的变化曲线。
的物质的量随时间的变化曲线。
(4)在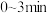 内,用
内,用 表示的反应速率为
表示的反应速率为_______ 。
(5)若在一绝热(不与外界发生热交换)容器中加入一定量 ,反应一段时间后,混合气体温度升高,说明
,反应一段时间后,混合气体温度升高,说明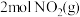 的能量比
的能量比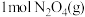 的能量
的能量_______ (填“高”或“低)。
(6)下列叙述能说明该反应已达到化学平衡状态的是_______ (填标号)。
A.容器内压强不再发生变化
B.混合气体的密度不变
C.混合气体的平均相对分子质量不变
D.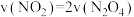
E.相同时间内消耗nmol的Y的同时消耗2nmol的X
(7)氮氧化物是重要的大气污染物,如图是监测NO含量的传感器工作原理示意图。NiO电极为_______ 极(填“正”或“负”)。

Ⅰ.用纯净的锌粒与稀盐酸反应制取氢气,请回答:
(1)实验过程如图所示,分析判断

(2)将锌粒投入盛有稀盐酸的烧杯中,刚开始时产生
 的速率逐渐加快,其原因是
的速率逐渐加快,其原因是Ⅱ.一定温度下,在体积为0.5L的恒容密闭容器中,
 和之间发生反应:
和之间发生反应: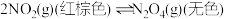 ,反应过程中各物质的物质的量与时间的关系如图所示。回答下列问题:
,反应过程中各物质的物质的量与时间的关系如图所示。回答下列问题:
(3)曲线
 的物质的量随时间的变化曲线。
的物质的量随时间的变化曲线。(4)在
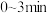 内,用
内,用 表示的反应速率为
表示的反应速率为(5)若在一绝热(不与外界发生热交换)容器中加入一定量
 ,反应一段时间后,混合气体温度升高,说明
,反应一段时间后,混合气体温度升高,说明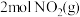 的能量比
的能量比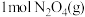 的能量
的能量(6)下列叙述能说明该反应已达到化学平衡状态的是
A.容器内压强不再发生变化
B.混合气体的密度不变
C.混合气体的平均相对分子质量不变
D.
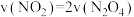
E.相同时间内消耗nmol的Y的同时消耗2nmol的X
(7)氮氧化物是重要的大气污染物,如图是监测NO含量的传感器工作原理示意图。NiO电极为

您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐3】中国政府承诺,到2020年,单位GDP二氧化碳排放比2005年下降40%-50%。减少CO2排放是一项重要课题。
(1)以CO2为原料抽取碳(C)的太阳能工艺如右图所示。

①过程1中每生成1mol FeO转移电子数为____________ 。
②过程2中发生反应的化学方程式为________________________________ 。
(2)CO2在新型钴基电催化剂作用下,转化为清洁燃料——甲酸。其工作原理如下图所示,写出生成甲酸的电极反应式:____________ 。

(3)航天员呼吸产生的CO2用下列反应处理,可实现空间站中O2的循环利用。
Sabatier反应:CO2(g)+4H2(g) CH4(g)+2H2O(g)
CH4(g)+2H2O(g)
水电解反应:2H2O(l) 2H2(g)+O2(g)
2H2(g)+O2(g)
将原料气按n(CO2)∶n(H2)=1∶4 置于密闭容器中发生Sabatier反应,测得H2O(g)的物质的量分数与温度的关系如下图所示(虚线表示平衡曲线)。

①温度过高或过低均不利于该反应的进行,原因是____________________________________ 。
②200℃达到平衡时体系的总压强为p,该反应平衡常数的计算式为________________ (不必化简,用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
(4)一种新的循环利用方案是用Bosch反应CO2(g)+2H2(g) C(s)+2H2O(g)代替Sabatier反应。
C(s)+2H2O(g)代替Sabatier反应。
①已知CO2(g)、H2O(g)的生成焓分别为-394 kJ·mol-l、-242 kJ·mol-l,Bosch反应的ΔH=__________ kJ·mol-l。(生成焓指一定条件下由对应单质生成1mol 化合物时的反应热)
②一定条件下Bosch反应必须在高温下才能启动,原因是______________________________ 。
③新方案的优点是_________________________ 。
(1)以CO2为原料抽取碳(C)的太阳能工艺如右图所示。

①过程1中每生成1mol FeO转移电子数为
②过程2中发生反应的化学方程式为
(2)CO2在新型钴基电催化剂作用下,转化为清洁燃料——甲酸。其工作原理如下图所示,写出生成甲酸的电极反应式:

(3)航天员呼吸产生的CO2用下列反应处理,可实现空间站中O2的循环利用。
Sabatier反应:CO2(g)+4H2(g)
 CH4(g)+2H2O(g)
CH4(g)+2H2O(g)水电解反应:2H2O(l)
 2H2(g)+O2(g)
2H2(g)+O2(g)将原料气按n(CO2)∶n(H2)=1∶4 置于密闭容器中发生Sabatier反应,测得H2O(g)的物质的量分数与温度的关系如下图所示(虚线表示平衡曲线)。

①温度过高或过低均不利于该反应的进行,原因是
②200℃达到平衡时体系的总压强为p,该反应平衡常数的计算式为
(4)一种新的循环利用方案是用Bosch反应CO2(g)+2H2(g)
 C(s)+2H2O(g)代替Sabatier反应。
C(s)+2H2O(g)代替Sabatier反应。①已知CO2(g)、H2O(g)的生成焓分别为-394 kJ·mol-l、-242 kJ·mol-l,Bosch反应的ΔH=
②一定条件下Bosch反应必须在高温下才能启动,原因是
③新方案的优点是
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐1】研究CO2合成CH3OH对资源综合利用有重要意义。涉及的主要反应如下,请回答:
I.CO2(g)+3H2(g) CH3OH(g)+H2O(g) ∆H1=—49kJ·mol-1
CH3OH(g)+H2O(g) ∆H1=—49kJ·mol-1
II.CO2(g)+H2(g) CO(g)+H2O(g) ∆H2=+41kJ·mol-1
CO(g)+H2O(g) ∆H2=+41kJ·mol-1
(1)CO2加氢制甲醇可在Cu—ZnO—ZrO2催化剂表面进行,其主反应历程如图1所示(催化剂表面吸附的物种用*标注),下列说法不正确的是_______ 。
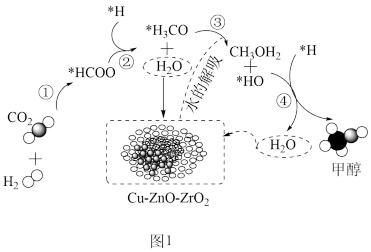
A.若该方法实现工业生产,气体以一定流速通过Cu—ZnO—ZrO2,催化剂对反应物的转化率无影响
B.H2在催化剂表面的吸附过程放热,有利于H—H键的断裂,从而降低反应活化能
C.反应②中,断裂和形成的共价键至少有3种
D.水的吸附和解吸在整个反应过程中实现了循环利用,原子利用率为100%
(2)CO2和H2按物质的量1:3投料,总物质的量为amol,在有催化剂的密闭容器中进行反应,测得CO2平衡转化率、CH3OH和CO选择性(转化的CO2中生成CH3OH或CO的百分比)随温度、压强变化情况分别如下图2、图3所示:

①下列说法正确的是_______ 。
A.升温,反应II的平衡正向移动
B.加压,反应I的平衡正向移动,平衡常数增大
C.及时分离出甲醇和水,循环使用H2和CO2,可提高原料利用率
D.升温,使反应I的CH3OH选择性降低;加压,对反应II的CO选择性无影响
②250°C时,在体积为VL的容器中,反应I和II达到化学平衡,CO2转化率为25%,CH3OH和CO选择性均为50%,则该温度下反应II的平衡常数为____ 。
③如图2,240°C以上,随着温度升高,CO2的平衡转化率升高,而CH3OH的选择性降低,分析其原因:___ 。
④如图3,压强大小关系:P1___ P3(填:>、<或=);温度T1时,三条曲线几乎交于一点,分析其原因____ 。
I.CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ∆H1=—49kJ·mol-1
CH3OH(g)+H2O(g) ∆H1=—49kJ·mol-1II.CO2(g)+H2(g)
 CO(g)+H2O(g) ∆H2=+41kJ·mol-1
CO(g)+H2O(g) ∆H2=+41kJ·mol-1(1)CO2加氢制甲醇可在Cu—ZnO—ZrO2催化剂表面进行,其主反应历程如图1所示(催化剂表面吸附的物种用*标注),下列说法不正确的是

A.若该方法实现工业生产,气体以一定流速通过Cu—ZnO—ZrO2,催化剂对反应物的转化率无影响
B.H2在催化剂表面的吸附过程放热,有利于H—H键的断裂,从而降低反应活化能
C.反应②中,断裂和形成的共价键至少有3种
D.水的吸附和解吸在整个反应过程中实现了循环利用,原子利用率为100%
(2)CO2和H2按物质的量1:3投料,总物质的量为amol,在有催化剂的密闭容器中进行反应,测得CO2平衡转化率、CH3OH和CO选择性(转化的CO2中生成CH3OH或CO的百分比)随温度、压强变化情况分别如下图2、图3所示:

①下列说法正确的是
A.升温,反应II的平衡正向移动
B.加压,反应I的平衡正向移动,平衡常数增大
C.及时分离出甲醇和水,循环使用H2和CO2,可提高原料利用率
D.升温,使反应I的CH3OH选择性降低;加压,对反应II的CO选择性无影响
②250°C时,在体积为VL的容器中,反应I和II达到化学平衡,CO2转化率为25%,CH3OH和CO选择性均为50%,则该温度下反应II的平衡常数为
③如图2,240°C以上,随着温度升高,CO2的平衡转化率升高,而CH3OH的选择性降低,分析其原因:
④如图3,压强大小关系:P1
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐2】“绿水青山就是金山银山”。近年来,绿色发展、生态保护成为中国展示给世界的一张新“名片”。汽车尾气是造成大气污染的重要原因之一,减少氢的氧化物在大气中的排放是环境保护的重要内容之一。请回答下列问题:
(1)已知:
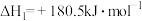

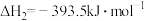

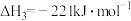
若某反应的平衡常数表达式为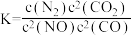 ,则此反应的热化学方程式为
,则此反应的热化学方程式为___________ 。
(2) 在一定条件下可发生分解反应:
在一定条件下可发生分解反应: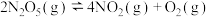 ,某温度下向恒容密闭容器中加入一定量
,某温度下向恒容密闭容器中加入一定量 ,测得
,测得 浓度随时间的变化如表:
浓度随时间的变化如表:
①反应开始时体系压强为 ,第2min时体系压强为
,第2min时体系压强为 ,则
,则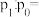
___________ 。2~5min内用 表示的该反应的平均反应速率为
表示的该反应的平均反应速率为___________ 。
②一定温度下,在恒容密闭容器中充入一定量 进行该反应,能判断反应已达到化学平衡状态的是
进行该反应,能判断反应已达到化学平衡状态的是___________ (填字母)。
a. 和
和 的浓度比保持不变 b.容器中压强不再变化
的浓度比保持不变 b.容器中压强不再变化
c.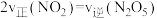 d.气体的密度保持不变
d.气体的密度保持不变
(3)一定温度下,将2mol CO、4mol NO充入一恒压密闭容器发生反应 ,已知起始压强为11MPa,达到平衡时,测得
,已知起始压强为11MPa,达到平衡时,测得 的物质的量为0.5mol,则该温度下用平衡分压表示的平衡常数
的物质的量为0.5mol,则该温度下用平衡分压表示的平衡常数
___________  (分压=总压×物质的量分数)
(分压=总压×物质的量分数)
(1)已知:

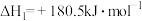

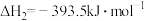

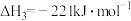
若某反应的平衡常数表达式为
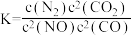 ,则此反应的热化学方程式为
,则此反应的热化学方程式为(2)
 在一定条件下可发生分解反应:
在一定条件下可发生分解反应: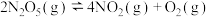 ,某温度下向恒容密闭容器中加入一定量
,某温度下向恒容密闭容器中加入一定量 ,测得
,测得 浓度随时间的变化如表:
浓度随时间的变化如表:| t/min | 0 | 1 | 2 | 3 | 4 | 5 |
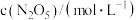 | 1.00 | 0.71 | 0.50 | 0.35 | 0.25 | 0.17 |
 ,第2min时体系压强为
,第2min时体系压强为 ,则
,则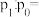
 表示的该反应的平均反应速率为
表示的该反应的平均反应速率为②一定温度下,在恒容密闭容器中充入一定量
 进行该反应,能判断反应已达到化学平衡状态的是
进行该反应,能判断反应已达到化学平衡状态的是a.
 和
和 的浓度比保持不变 b.容器中压强不再变化
的浓度比保持不变 b.容器中压强不再变化c.
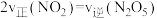 d.气体的密度保持不变
d.气体的密度保持不变(3)一定温度下,将2mol CO、4mol NO充入一恒压密闭容器发生反应
 ,已知起始压强为11MPa,达到平衡时,测得
,已知起始压强为11MPa,达到平衡时,测得 的物质的量为0.5mol,则该温度下用平衡分压表示的平衡常数
的物质的量为0.5mol,则该温度下用平衡分压表示的平衡常数
 (分压=总压×物质的量分数)
(分压=总压×物质的量分数)
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐3】氢气是一种理想的绿色能源。利用生物质发酵得到的乙醇制取氢气,具有良好的应用前景。乙醇和水蒸气重整制氢的部分反应过程如下图所示:
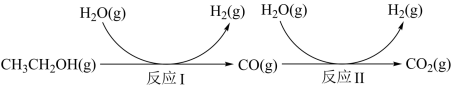
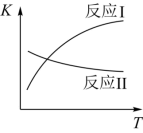
已知:反应Ⅰ和反应Ⅱ的平衡常数随温度变化曲线如图所示。
(1)反应Ⅰ中,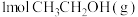 参与反应后的热量变化是
参与反应后的热量变化是 。
。
①反应Ⅰ的热化学方程式是___________ 。
②反应Ⅰ在较高温度下能够自发进行的原因是___________ 。
③已知绝热恒压下,下列说法能够判断反应Ⅰ达到化学平衡状态的是___________ (填字母)。
A 的含量保持不变 B.容器中压强保持不变
的含量保持不变 B.容器中压强保持不变
C.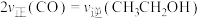 D.体系的温度保持不变
D.体系的温度保持不变
(2)反应Ⅱ中
①某温度下,已知 和
和 的起始浓度总和为
的起始浓度总和为 ,且
,且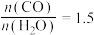 的投料比下,
的投料比下, 的平衡转化率为40%,该温度下反应平衡常数的值为
的平衡转化率为40%,该温度下反应平衡常数的值为___________ 。
②当不同的进气比[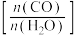 达到相同的
达到相同的 平衡转化率时,对应的反应温度和进气比的关系是
平衡转化率时,对应的反应温度和进气比的关系是___________ 。
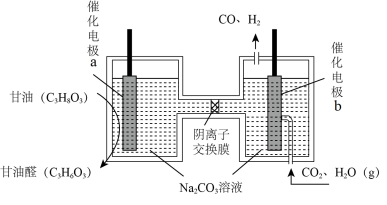
(3)我国科学家设计了一种电解装置如图所示,能将二氧化碳转化成合成气 和
和 ,同时获得甘油醛
,同时获得甘油醛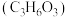 。a极接电源的
。a极接电源的___________ 极;若阴离子交换膜只允许 离子通过,当有
离子通过,当有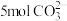 通过时,理论上可制得甘油醛
通过时,理论上可制得甘油醛___________ g。


已知:反应Ⅰ和反应Ⅱ的平衡常数随温度变化曲线如图所示。
(1)反应Ⅰ中,
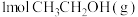 参与反应后的热量变化是
参与反应后的热量变化是 。
。①反应Ⅰ的热化学方程式是
②反应Ⅰ在较高温度下能够自发进行的原因是
③已知绝热恒压下,下列说法能够判断反应Ⅰ达到化学平衡状态的是
A
 的含量保持不变 B.容器中压强保持不变
的含量保持不变 B.容器中压强保持不变C.
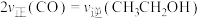 D.体系的温度保持不变
D.体系的温度保持不变(2)反应Ⅱ中
①某温度下,已知
 和
和 的起始浓度总和为
的起始浓度总和为 ,且
,且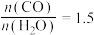 的投料比下,
的投料比下, 的平衡转化率为40%,该温度下反应平衡常数的值为
的平衡转化率为40%,该温度下反应平衡常数的值为②当不同的进气比[
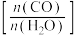 达到相同的
达到相同的 平衡转化率时,对应的反应温度和进气比的关系是
平衡转化率时,对应的反应温度和进气比的关系是(3)我国科学家设计了一种电解装置如图所示,能将二氧化碳转化成合成气
 和
和 ,同时获得甘油醛
,同时获得甘油醛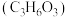 。a极接电源的
。a极接电源的 离子通过,当有
离子通过,当有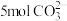 通过时,理论上可制得甘油醛
通过时,理论上可制得甘油醛
您最近一年使用:0次



