名校
解题方法
1 . 常温常压下,3.2g甲醇完全燃烧生成CO2和液态水时放热72.58kJ,甲醇燃烧热的热化学方程式为( )
A.CH3OH(1)+ O2(g)=CO2(g)+2H2O(1) ΔH=+725.8kJ·mol-1 O2(g)=CO2(g)+2H2O(1) ΔH=+725.8kJ·mol-1 |
| B.2CH3OH(1)+3O2(g)=2CO2(g)+4H2O(1) ΔH=-725.8kJ·mol-1 |
C.CH3OH(1)+ O2(g)=CO2(g)+2H2O(1) ΔH=-725.8kJ·mol-1 O2(g)=CO2(g)+2H2O(1) ΔH=-725.8kJ·mol-1 |
| D.2CH3OH(1)+3O2(g)=2CO2(g)+4H2O(1) ΔH=-1451.6kJ·mol-1 |
您最近一年使用:0次
2022-10-16更新
|
325次组卷
|
7卷引用:福建省三明市泰宁县福建省泰宁第一中学2019-2020学年高二上学期第二次阶段考试化学试题
名校
解题方法
2 . 在101kPa时,32g CH4完全燃烧生成CO2和液态H2O,放出的热量为1780kJ,则甲烷的燃烧热为
| A.1780kJ/mol | B.-1780kJ/mol |
| C.890kJ/mol | D.-890kJ/mol |
您最近一年使用:0次
2021-07-16更新
|
584次组卷
|
5卷引用:河北省安平中学2020-2021学年高一下学期第四次月考(期末)化学试题
3 . 已知B2H6(g)+3O2(g)=B2O3(s)+3H2O(1) △H=-2165kJ/mol为高能燃料乙硼烷燃烧的热化学方程式,则0.5molB2H6(g)在该条件下完全燃烧时
| A.放出2165kJ热量 | B.吸收2165kJ热量 |
| C.放出1082.5kJ热量 | D.吸收1082.5kJ热量 |
您最近一年使用:0次
名校
解题方法
4 . (1)0.3mol气态高能燃料乙硼烷(B2H6)在氧气中燃烧,生成固态三氧化二硼和液态水放出649.5kJ热量,其热化学方程式为:_______ ;又已知H2O(l)=H2O(g) ΔH=+44kJ/mol,则11.2L(标准状况)乙硼烷完全燃烧生成气态水时放出的热量是_______ kJ。
(2)已知H—H键键能为436kJ·mol-1,H—N键键能为391kJ·mol-1,根据化学方程式:N2+3H2⇌2NH3 ΔH=-92.4kJ·mol-1,则N≡N键键能是_______ 。
(3)1mol氧气与足量氢气反应生成水蒸气放热483.6kJ,写出该反应的热化学方程式:_______ 。若1g水蒸气转化成液态水放热2.444kJ,写出表示氢气燃烧热的热化学方程式:_______ 。
(4)含11.2gKOH的稀溶液与1L0.1mol·L-1的H2SO4溶液反应放出11.46kJ的热量,该离子反应的热化学方程式为_______ ,则KOH与H2SO4反应的中和热为_______ 。
(5)已知:①C(s)+O2(g)=CO2(g) ΔH1=-393.5kJ·mol-1
②2CO(g)+O2(g)=2CO2(g) ΔH2=-566kJ·mol-1
③TiO2(s)+2Cl2(g)=TiCl4(s)+O2(g) ΔH3=+141kJ·mol-1
则TiO2(s)+2Cl2(g)+2C(s)=TiCl4(s)+2CO(g)的ΔH=_______ 。
(2)已知H—H键键能为436kJ·mol-1,H—N键键能为391kJ·mol-1,根据化学方程式:N2+3H2⇌2NH3 ΔH=-92.4kJ·mol-1,则N≡N键键能是
(3)1mol氧气与足量氢气反应生成水蒸气放热483.6kJ,写出该反应的热化学方程式:
(4)含11.2gKOH的稀溶液与1L0.1mol·L-1的H2SO4溶液反应放出11.46kJ的热量,该离子反应的热化学方程式为
(5)已知:①C(s)+O2(g)=CO2(g) ΔH1=-393.5kJ·mol-1
②2CO(g)+O2(g)=2CO2(g) ΔH2=-566kJ·mol-1
③TiO2(s)+2Cl2(g)=TiCl4(s)+O2(g) ΔH3=+141kJ·mol-1
则TiO2(s)+2Cl2(g)+2C(s)=TiCl4(s)+2CO(g)的ΔH=
您最近一年使用:0次
名校
5 . 在燃烧1.12L(标准状况)CO与O2的混合气体时,放出5.66kJ的热量,在相同的状况下,最后产物的密度为原来气体密度的1.25倍,则CO的燃烧热为
| A.283kJ·mol-1 | B.-283kJ·mol-1 |
| C.-566kJ·mol-1 | D.566kJ·mol-1 |
您最近一年使用:0次
2021-06-03更新
|
447次组卷
|
6卷引用:江西省抚州市金溪县第一中学2019-2020学年高二上学期第二次月考化学试题
江西省抚州市金溪县第一中学2019-2020学年高二上学期第二次月考化学试题(已下线)1.2 燃烧热 能源-2021-2022学年高二化学课后培优练(人教版选修4)(已下线)第1章 化学反应的热效应(基础过关卷)-【高效检测】2021-2022学年高二化学章末测试卷(人教版2019选择性必修1)江西省南城第二中学2021-2022学年高二上学期第一次月考化学试题四川省泸州市泸县第一中学2023-2024学年高二上学期11月期中考试化学试题江西省宜春市丰城市东煌学校2023-2024学年高二上学期11月期中化学试题
11-12高二上·福建福州·阶段练习
名校
解题方法
6 . 分析表中的四个热化学方程式,判断氢气和丙烷的标准燃烧热分别是
| “嫦娥一号”发射火箭燃料 | 液氢(H2) | ①2H2(g)+O2(g)=2H2O(l)ΔH=-571.6kJ∙mol-1 ②2H2(l)+O2(l)=2H2O(g) ΔH=-482.6kJ∙mol-1 |
| 北京奥运会“祥云”火炬燃料 | 丙烷(C3H8) | ③C3H8(l)+5O2(g)=3CO2(g)+4H2O(g) ΔH=-2013.8kJ∙mol-1 ④C3H8(g)+5O2(g)=3CO2(g)+4H2O(l) ΔH=-2221.5kJ∙mol-1 |
| A.-571.6kJ∙mol-1,-2221.5kJ∙mol-1 | B.-285.5kJ∙mol-1,-2013.8kJ∙mol-1 |
| C.-285.8kJ∙mol-1,-2221.5kJ∙mol-1 | D.-241.3kJ∙mol-1,-2013.8kJ∙mol-1 |
您最近一年使用:0次
2021-03-17更新
|
541次组卷
|
20卷引用:2011-2012年福建省福州市罗源一中高二上学期第一次月考化学试卷
(已下线)2011-2012年福建省福州市罗源一中高二上学期第一次月考化学试卷(已下线)2015安徽望江中学同步课时练(人教选修4)第一章检测试卷2015-2016学年云南省昆明三中高二下期中化学试卷2016-2017学年陕西省西安中学高二上10月月考化学试卷四川省成都七中实验学校2018-2019学年高二上学期10月月考化学试题(已下线)2014届甘肃省天水市秦安县高三上学期期末检测化学试卷(已下线)2013-2014福建安溪一中、惠安一中、养正中学下学期期中高二化学(已下线)2014-2015学年云南省玉溪市第一中学高二上学期期中考试化学试卷2015-2016学年山东省淄博市淄川一中等三校高二上期末联考化学试卷贵州省遵义市航天高级中学2018-2019学年高二(理)上学期第一次月考化学试题【全国百强校】贵州省遵义航天高级中学2018-2019学年高二上学期第一次月考化学试题吉林省东辽五中2019-2020学年高二上学期9月月考化学试题江西省赣州市赣县第三中学2020-2021学年高二上学期9月入学考试化学试题(重点班)吉林省辽源市田家炳高级中学校2020-2021学年高二上学期第一次月考化学试题安徽省六安市舒城育才学校2020-2021学年高二上学期期末考试化学试题(已下线)1.2 燃烧热 能源-2021-2022学年高二化学课后培优练(人教版选修4)陕西省泾阳县2020-2021学年高二上学期期中考试化学试题(已下线)1.1.2 热化学方程式 燃烧热(素养提优B练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)河北省衡水市武强中学2021-2022学年高二下学期期中考试化学试题(已下线)第一章 化学反应的热效应(A卷·知识通关练)-【单元测试】2022-2023学年高二化学分层训练AB卷(人教版2019选择性必修1)
7 . 下列各组物质的燃烧热相等的是
| A.碳和一氧化碳 | B.1moL 和2moL 和2moL |
C.3moL 和1moL 和1moL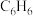 | D.淀粉和纤维素 |
您最近一年使用:0次
8 . 298 K、101 kPa时,根据6C(石墨,s)+3H2(g)=C6H6(l)设计的反应路径如下:

上述条件下石墨、氢气、苯的燃烧热依次为△H(石墨)、△H(H2)、△H(C6H6),下列说法正确的是

上述条件下石墨、氢气、苯的燃烧热依次为△H(石墨)、△H(H2)、△H(C6H6),下列说法正确的是
| A.△H1=△H2+△H3 |
| B.C6H6的能量一定高于CO2和H2O的能量 |
| C.1 mol C6H6(g)完全燃烧生成CO2(g)和H2O(l)的△H>△H3 |
| D.6×△H(石墨)+3×△H(H2)=△H2 |
您最近一年使用:0次
2020-12-20更新
|
228次组卷
|
3卷引用:河南省重点高中2020-2021学年高二上学期阶段性测试(二) 化学试题
河南省重点高中2020-2021学年高二上学期阶段性测试(二) 化学试题(已下线)第25练 反应热的计算-2023年高考化学一轮复习小题多维练(全国通用)安徽省芜湖市第一中学2021-2022学年高一下学期期中考试化学试题
名校
解题方法
9 . 填空
(1)已知C(s,石墨)=C(s,金刚石) ΔH>0,则稳定性:金刚石___ (填“>”或“<”)石墨。
(2)已知:2C(s)+2O2(g)=2CO2(g) ΔH1;2C(s)+O2(g)=2CO(g) ΔH2;则ΔH1____ (填“>”或“<”)ΔH2。
(3)“嫦娥五号”发射时,用肼(N2H4)作燃料,四氧化二氮作氧化剂,二者反应生成氮气和气态水。已知:
①N2(g)+2O2(g)=N2O4(g) ΔH=+10.7 kJ·mol-1;
②N2H4(g)+O2(g)=N2(g)+2H2O(g) ΔH=-543 kJ·mol-1
写出气态肼和N2O4反应的热化学方程式:________ 。
(4)25 ℃、101 kPa时,14 g CO在足量的O2中充分燃烧,放出141.3 kJ热量,则CO的燃烧热ΔH=____ 。
(5)0.50 L 2.00 mol·L-1H2SO4溶液与2.10 L 1.00 mol·L-1 KOH溶液完全反应,放出114.6 kJ热量,该反应的中和热ΔH=______ 。
(6)已知断开1 mol H-H键、1 mol N-H键、1 mol N≡N键分别需要的能量是436 kJ、391 kJ、946 kJ,则N2与H2反应生成NH3的热化学方程式是________ 。
(1)已知C(s,石墨)=C(s,金刚石) ΔH>0,则稳定性:金刚石
(2)已知:2C(s)+2O2(g)=2CO2(g) ΔH1;2C(s)+O2(g)=2CO(g) ΔH2;则ΔH1
(3)“嫦娥五号”发射时,用肼(N2H4)作燃料,四氧化二氮作氧化剂,二者反应生成氮气和气态水。已知:
①N2(g)+2O2(g)=N2O4(g) ΔH=+10.7 kJ·mol-1;
②N2H4(g)+O2(g)=N2(g)+2H2O(g) ΔH=-543 kJ·mol-1
写出气态肼和N2O4反应的热化学方程式:
(4)25 ℃、101 kPa时,14 g CO在足量的O2中充分燃烧,放出141.3 kJ热量,则CO的燃烧热ΔH=
(5)0.50 L 2.00 mol·L-1H2SO4溶液与2.10 L 1.00 mol·L-1 KOH溶液完全反应,放出114.6 kJ热量,该反应的中和热ΔH=
(6)已知断开1 mol H-H键、1 mol N-H键、1 mol N≡N键分别需要的能量是436 kJ、391 kJ、946 kJ,则N2与H2反应生成NH3的热化学方程式是
您最近一年使用:0次
2020-12-15更新
|
319次组卷
|
6卷引用:2015届四川省成都郫县高三第二次阶诊断性考试理综化学试卷
2015届四川省成都郫县高三第二次阶诊断性考试理综化学试卷河北省安平中学2017-2018学年高一下学期期末考试化学试题1贵州省毕节市七星关区毕节市实验高级中学2020-2021学年高二上学期期中考试化学试题(已下线)第六章能力提升检测卷(精练)-2022年高考化学一轮复习讲练测(已下线)专题18 化学反应与能量(限时精练)-2022年高三毕业班化学常考点归纳与变式演练重庆市沙坪坝实验中学校2021-2022学年高二上学期12月月考化学试题
名校
10 . 1 g火箭燃料N2H4(g)燃烧,生成N2(g)和H2O(g),同时放出16.7 kJ的热量,表示该反应的热化学方程式正确的是
| A.N2H4+O2=N2 + 2H2O △H =- 534.4 kJ/mol |
| B.N2H4+O2 =N2 +2H2O △H=-1068.8 kJ/mol |
| C.N2H4(g)+O2(g) =N2(g)+2H2O(g) △H =-534.4 kJ/mol |
D. N2H4(g)+ N2H4(g)+ O2(g)= O2(g)= N2(g) + H2O(g) △H =+267.2 kJ/mol N2(g) + H2O(g) △H =+267.2 kJ/mol |
您最近一年使用:0次
2020-11-28更新
|
162次组卷
|
7卷引用:重庆市万州纯阳中学2020-2021学年高二上学期期中考试化学试题
重庆市万州纯阳中学2020-2021学年高二上学期期中考试化学试题(已下线)练习2 燃烧热 能源-2020-2021学年【补习教材·寒假作业】高二化学(人教版)甘肃省永昌县第一高级中学2020-2021学年高二上学期期中考试化学(理)试题(已下线)1.2.1 反应热的测量和热化学方程式-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修第一册)黑龙江省哈尔滨市尚志中学2022-2023学年高二上学期12月月考化学试题甘肃省兰州市天水市第三中学等2校2022-2023学年高二上学期10月期中化学试题甘肃省天水市清水县2022-2023学年高二上学期12月期中考试化学试题



