名校
解题方法
1 . 常温常压下,3.2g甲醇完全燃烧生成CO2和液态水时放热72.58kJ,甲醇燃烧热的热化学方程式为( )
A.CH3OH(1)+ O2(g)=CO2(g)+2H2O(1) ΔH=+725.8kJ·mol-1 O2(g)=CO2(g)+2H2O(1) ΔH=+725.8kJ·mol-1 |
| B.2CH3OH(1)+3O2(g)=2CO2(g)+4H2O(1) ΔH=-725.8kJ·mol-1 |
C.CH3OH(1)+ O2(g)=CO2(g)+2H2O(1) ΔH=-725.8kJ·mol-1 O2(g)=CO2(g)+2H2O(1) ΔH=-725.8kJ·mol-1 |
| D.2CH3OH(1)+3O2(g)=2CO2(g)+4H2O(1) ΔH=-1451.6kJ·mol-1 |
您最近一年使用:0次
2022-10-16更新
|
325次组卷
|
7卷引用:福建省三明市泰宁县福建省泰宁第一中学2019-2020学年高二上学期第二次阶段考试化学试题
2 . 汽车在行驶过程中有如下反应发生:
ⅰ.N2(g)+O2(g) ⇌2NO(g)ΔH=+180.7 kJ·mol-1
ⅱ.2NO(g)+2CO(g) ⇌N2(g)+2CO2(g)ΔH=-746.5 kJ·mol-1
(1)能表示CO燃烧热的热化学方程式为___________ 。
(2)反应ⅱ在___________ (填“较高”或“较低”)温度下能自发进行。
(3)T温度时,向10 L恒容密闭容器中充入2 molNO和2molCO发生反应ⅱ,5min时达到平衡,测得0~5min内该反应速率v(N2)=0.016 mol·L-1·min-1
①T温度时,该反应的平衡常数K=___________ 。
②平衡时容器内压强与起始时容器内压强之比为___________ 。
(4)一定条件下,向起始容积为5 L的恒压密闭容器中充入1 mol N2和1 mol O2发生反应ⅰ。O2的平衡转化率[α(O2)]与温度(T)的关系如图1所示;正反应的平衡常数(K正)与温度(T)的关系如图2所示。
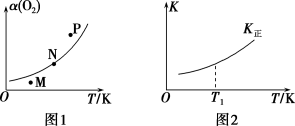
①图1中,M、N、P三点所对应的状态下,v正>v逆的是___________ (填字母),理由为___________ 。
②T1温度时,K正=1,则O2的平衡转化率为___________ (保留三位有效数字)。
ⅰ.N2(g)+O2(g) ⇌2NO(g)ΔH=+180.7 kJ·mol-1
ⅱ.2NO(g)+2CO(g) ⇌N2(g)+2CO2(g)ΔH=-746.5 kJ·mol-1
(1)能表示CO燃烧热的热化学方程式为
(2)反应ⅱ在
(3)T温度时,向10 L恒容密闭容器中充入2 molNO和2molCO发生反应ⅱ,5min时达到平衡,测得0~5min内该反应速率v(N2)=0.016 mol·L-1·min-1
①T温度时,该反应的平衡常数K=
②平衡时容器内压强与起始时容器内压强之比为
(4)一定条件下,向起始容积为5 L的恒压密闭容器中充入1 mol N2和1 mol O2发生反应ⅰ。O2的平衡转化率[α(O2)]与温度(T)的关系如图1所示;正反应的平衡常数(K正)与温度(T)的关系如图2所示。

①图1中,M、N、P三点所对应的状态下,v正>v逆的是
②T1温度时,K正=1,则O2的平衡转化率为
您最近一年使用:0次
解题方法
3 . 在恒压下化学反应所吸收或放出的热量,称为化学反应的焓变。回答下列问题:
(1)25℃、101 kPa时,1 g氨气完全燃烧放出18.6 kJ的热量,则4NH3(g)+3O2(g)=2N2(g)+6H2O(l) △H=______ kJ·mol-1。
(2)常压下,某铝热反应的温度与能量变化如图所示:
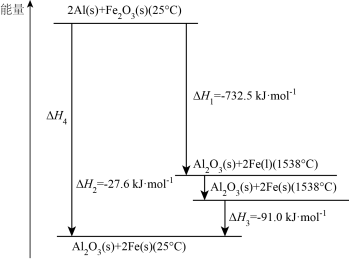
①常压、1538℃时,Fe(s)→Fe(l) △H=______ kJ·mol-1。
②常压、25℃时,该铝热反应的热化学方程式为__________ 。
(3)在稀溶液中酸与碱发生中和反应生成1 mol水时所释放的热量称为中和热。部分酸与碱反应的中和热如下表:
①I、IV的热化学方程式(用离子方程式形式表示)依次为_____ 、_____ 。
②I、II的△H相同,III、IV、V的△H比I、II大,其原因是__________ 。
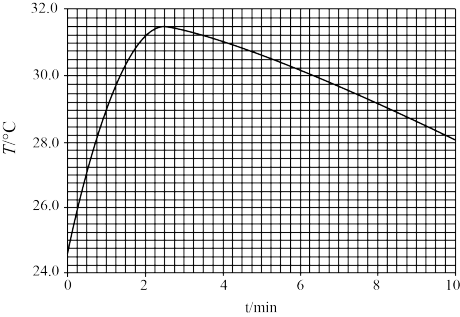
③体积和浓度均为25.0 mL 1.00 mol·L-1的硝酸和NaOH溶液(起始温度相同)混合时,测得混合溶液的温度与时间的关系如图所示,已知硝酸和NaOH溶液的密度均为1.00 g·mL-1,混合溶液的比热容为4.18 J·g-1·℃-1。由实验数据可计算出该反应的中和热△H为______ kJ·mol-1(结果保留1位小数)。
(1)25℃、101 kPa时,1 g氨气完全燃烧放出18.6 kJ的热量,则4NH3(g)+3O2(g)=2N2(g)+6H2O(l) △H=
(2)常压下,某铝热反应的温度与能量变化如图所示:

①常压、1538℃时,Fe(s)→Fe(l) △H=
②常压、25℃时,该铝热反应的热化学方程式为
(3)在稀溶液中酸与碱发生中和反应生成1 mol水时所释放的热量称为中和热。部分酸与碱反应的中和热如下表:
| 组别 | 酸与碱 | 中和热△H/(kJ/mol) |
| Ⅰ | HCl+NaOH | -57.1 |
| Ⅱ | HNO3+KOH | -57.1 |
| Ⅲ | CH3COOH+NaOH | -56.1 |
| Ⅳ | HCl+NH3·H2O | -53.4 |
| Ⅴ | CH3COOH+NH3·H2O | -50.4 |
②I、II的△H相同,III、IV、V的△H比I、II大,其原因是
③体积和浓度均为25.0 mL 1.00 mol·L-1的硝酸和NaOH溶液(起始温度相同)混合时,测得混合溶液的温度与时间的关系如图所示,已知硝酸和NaOH溶液的密度均为1.00 g·mL-1,混合溶液的比热容为4.18 J·g-1·℃-1。由实验数据可计算出该反应的中和热△H为

您最近一年使用:0次
4 . 298 K、101 kPa时,根据6C(石墨,s)+3H2(g)=C6H6(l)设计的反应路径如下:

上述条件下石墨、氢气、苯的燃烧热依次为△H(石墨)、△H(H2)、△H(C6H6),下列说法正确的是

上述条件下石墨、氢气、苯的燃烧热依次为△H(石墨)、△H(H2)、△H(C6H6),下列说法正确的是
| A.△H1=△H2+△H3 |
| B.C6H6的能量一定高于CO2和H2O的能量 |
| C.1 mol C6H6(g)完全燃烧生成CO2(g)和H2O(l)的△H>△H3 |
| D.6×△H(石墨)+3×△H(H2)=△H2 |
您最近一年使用:0次
2020-12-20更新
|
228次组卷
|
3卷引用:河南省重点高中2020-2021学年高二上学期阶段性测试(二) 化学试题
河南省重点高中2020-2021学年高二上学期阶段性测试(二) 化学试题(已下线)第25练 反应热的计算-2023年高考化学一轮复习小题多维练(全国通用)安徽省芜湖市第一中学2021-2022学年高一下学期期中考试化学试题
5 . 化学是一门应用性科学,在人们生活及社会生产中应用广泛。回答下列有关问题:
(1)已知下列物质: 、醋酸溶液、乙醇、淀粉、谷氨酸钠、
、醋酸溶液、乙醇、淀粉、谷氨酸钠、 。
。
①属于非电解质的是___________ 。
②属于弱电解质的是___________ ,其电离常数表达式为___________ 。
③ 可用来制作燃料电池,以
可用来制作燃料电池,以 溶液为电解质溶液,则负极反应式为
溶液为电解质溶液,则负极反应式为___________ 。
(2)已知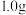 液态甲醇完全燃烧生成
液态甲醇完全燃烧生成 和液态水时,放出
和液态水时,放出 的热量,则液态甲醇的燃烧热
的热量,则液态甲醇的燃烧热
___________  。
。
(3)下图为氮气和氢气合成氨的反应过程中的能量变化曲线:

上面的图象中,a、b曲线中有一种使用了催化剂,则使用催化剂的曲线为___________ (填“a”或“b”),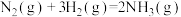

___________  。
。
(1)已知下列物质:
 、醋酸溶液、乙醇、淀粉、谷氨酸钠、
、醋酸溶液、乙醇、淀粉、谷氨酸钠、 。
。①属于非电解质的是
②属于弱电解质的是
③
 可用来制作燃料电池,以
可用来制作燃料电池,以 溶液为电解质溶液,则负极反应式为
溶液为电解质溶液,则负极反应式为(2)已知
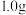 液态甲醇完全燃烧生成
液态甲醇完全燃烧生成 和液态水时,放出
和液态水时,放出 的热量,则液态甲醇的燃烧热
的热量,则液态甲醇的燃烧热
 。
。(3)下图为氮气和氢气合成氨的反应过程中的能量变化曲线:

上面的图象中,a、b曲线中有一种使用了催化剂,则使用催化剂的曲线为
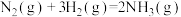

 。
。
您最近一年使用:0次
6 . 由H2和CO组成的混合气体0.5mol,完全燃烧后放出142.55kJ的能量,已知H2的燃烧热△H=-285.80kJ/mol,CO的燃烧热△H=-283.00kJ/mol。该混合气体中H2的体积分数为( )
| A.25% | B.45% | C.75% | D.80% |
您最近一年使用:0次
7 . 一定条件下,充分燃烧一定量的丁烷放出热量为QkJ(Q>0),经测定完全吸收生成的二氧化碳需消耗5mol·L-1的KOH溶液100mL,恰好生成正盐,则此条件下反应:C4H10(g)+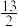 O2(g)=4CO2(g)+5H2O(g)的△H为( )
O2(g)=4CO2(g)+5H2O(g)的△H为( )
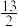 O2(g)=4CO2(g)+5H2O(g)的△H为( )
O2(g)=4CO2(g)+5H2O(g)的△H为( )| A.+8QkJ | B.+16QkJ | C.-8QkJ | D.-16QkJ |
您最近一年使用:0次
2020-10-28更新
|
312次组卷
|
23卷引用:2014-2015学年河南省周口中英文学校高二10月月考化学试卷
(已下线)2014-2015学年河南省周口中英文学校高二10月月考化学试卷(已下线)2011-2012学年陕西省师大附中高一下学期期末考试化学试卷(已下线)2013届甘肃省张掖二中高三10月月考化学试卷(奥班)(已下线)2014年化学高考总复习课时演练 6化学反应与能量练习卷2014-2015学年吉林省吉林市一中高一下期末考试化学试卷2015-2016学年内蒙古包头九中高一6月月考化学试卷2016-2017学年青海省西宁五中高二上月考一化学卷2016-2017学年青海省西宁五中高二11月月考化学试卷2016-2017学年辽宁省沈阳铁路实验中学高一4月月考化学试卷黑龙江省双鸭山市第一中学2017-2018学年高二9月月考化学试题吉林省汪清县第六中学2017-2018学年高二上学期期末考试化学试题河北省承德市第二中学2017-2018学年高二上学期第一次月考化学试题【全国百强校】陕西省西安市长安区第一中学2018-2019学年高二上学期期中考试化学试题(已下线)第01章 化学反应的热效应(B卷能力提高篇)-2020-2021学年高二化学选择性必修1同步单元AB卷(新教材人教版)宁夏回族自治区海原县第一中学2020-2021学年高二上学期第一次月考化学试题新疆乌鲁木齐市第四中学2020-2021学年高二上学期期中考试化学试题黑龙江省大庆市实验中学实验一部2020-2021学年高一下学期4月阶段性教学质量检测化学试题福建省宁化第一中学2021-2022学年高二上学期开学考试化学试题云南省玉龙县第一中学2021-2022学年高二下学期3月份考试化学试题福建省三明市第二中学2022-2023学年高二上学期开学适应性练习化学试题安徽省太和县第八中学2021-2022学年高二上学期第一次月考化学试题(已下线)专题02 盖斯定律、反应热的计算【考题猜想】(6大题型)-2023-2024学年高二化学期中考点大串讲(人教版2019选择性必修1)天津市蓟州中学2022-2023学年高二上学期第一次月考化学试题
名校
解题方法
8 . 在25℃时,2mol乙醇(C2H5OH)在氧气中完全燃烧放出的热量为2733.6kJ,写出表示乙醇燃烧热的热化学方程式________ 。
您最近一年使用:0次
9 . 化学在能源开发与利用中起着十分关键的作用。
(1)蕴藏在海底的“可燃冰”是高压下形成的外观像冰的甲烷水合物固体。甲烷气体氧化和水汽化的热化学方程式分别为:
①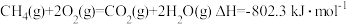 ,
,
②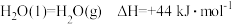 。
。
则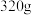 “可燃冰”(分子式为
“可燃冰”(分子式为 )释放的甲烷气体完全氧化生成二氧化碳气体和液态水时放出的热量为
)释放的甲烷气体完全氧化生成二氧化碳气体和液态水时放出的热量为_________ 。
(2)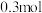 的气态高能燃料乙硼烷(
的气态高能燃料乙硼烷( )在氧气中氧化生成固态三氧化二硼和液态水时放出
)在氧气中氧化生成固态三氧化二硼和液态水时放出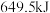 热量,其热化学方程式为
热量,其热化学方程式为________________ 。
(3)家用液化气的主要成分之一是丁烷( )。常温常压条件下,
)。常温常压条件下,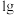 丁烷完全氧化生成
丁烷完全氧化生成 气体和液态水时放出热量
气体和液态水时放出热量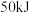 ,则表示丁烷摩尔燃烧焓的热化学方程式为
,则表示丁烷摩尔燃烧焓的热化学方程式为______________ 。
(4)下列制氢气方法中最节能的是_________ (填序号)。
A.电解水制氢气: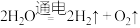
B.高温使水分解制氢气: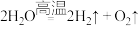
C.太阳光催化分解水制氢气: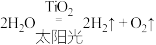
D.天然气制氢气: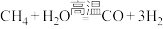
(1)蕴藏在海底的“可燃冰”是高压下形成的外观像冰的甲烷水合物固体。甲烷气体氧化和水汽化的热化学方程式分别为:
①
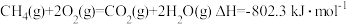 ,
,②
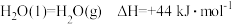 。
。则
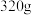 “可燃冰”(分子式为
“可燃冰”(分子式为 )释放的甲烷气体完全氧化生成二氧化碳气体和液态水时放出的热量为
)释放的甲烷气体完全氧化生成二氧化碳气体和液态水时放出的热量为(2)
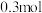 的气态高能燃料乙硼烷(
的气态高能燃料乙硼烷( )在氧气中氧化生成固态三氧化二硼和液态水时放出
)在氧气中氧化生成固态三氧化二硼和液态水时放出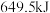 热量,其热化学方程式为
热量,其热化学方程式为(3)家用液化气的主要成分之一是丁烷(
 )。常温常压条件下,
)。常温常压条件下,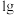 丁烷完全氧化生成
丁烷完全氧化生成 气体和液态水时放出热量
气体和液态水时放出热量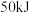 ,则表示丁烷摩尔燃烧焓的热化学方程式为
,则表示丁烷摩尔燃烧焓的热化学方程式为(4)下列制氢气方法中最节能的是
A.电解水制氢气:
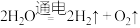
B.高温使水分解制氢气:
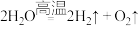
C.太阳光催化分解水制氢气:
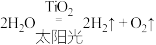
D.天然气制氢气:
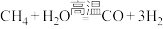
您最近一年使用:0次
2020-10-07更新
|
278次组卷
|
3卷引用:河南省原阳县第三高级中学2020-2021学年高二上学期第一次月考化学试题
10 . 充分燃烧一定量的丁烷气体放出的热量为Q。完全吸收它生成的CO2气体生成正盐,需5 mol/L的KOH溶液100 mL,则丁烷的燃烧热为( )
| A.16Q | B.8Q | C.4Q | D.2Q |
您最近一年使用:0次



