名校
解题方法
1 . 常温常压下,3.2g甲醇完全燃烧生成CO2和液态水时放热72.58kJ,甲醇燃烧热的热化学方程式为( )
A.CH3OH(1)+ O2(g)=CO2(g)+2H2O(1) ΔH=+725.8kJ·mol-1 O2(g)=CO2(g)+2H2O(1) ΔH=+725.8kJ·mol-1 |
| B.2CH3OH(1)+3O2(g)=2CO2(g)+4H2O(1) ΔH=-725.8kJ·mol-1 |
C.CH3OH(1)+ O2(g)=CO2(g)+2H2O(1) ΔH=-725.8kJ·mol-1 O2(g)=CO2(g)+2H2O(1) ΔH=-725.8kJ·mol-1 |
| D.2CH3OH(1)+3O2(g)=2CO2(g)+4H2O(1) ΔH=-1451.6kJ·mol-1 |
您最近一年使用:0次
2022-10-16更新
|
325次组卷
|
7卷引用:福建省三明市泰宁县福建省泰宁第一中学2019-2020学年高二上学期第二次阶段考试化学试题
名校
解题方法
2 . 在101kPa时,32g CH4完全燃烧生成CO2和液态H2O,放出的热量为1780kJ,则甲烷的燃烧热为
| A.1780kJ/mol | B.-1780kJ/mol |
| C.890kJ/mol | D.-890kJ/mol |
您最近一年使用:0次
2021-07-16更新
|
586次组卷
|
5卷引用:江西省新余市渝水区第一中学2019-2020学年高二上学期第一次月考化学试题
3 . 已知B2H6(g)+3O2(g)=B2O3(s)+3H2O(1) △H=-2165kJ/mol为高能燃料乙硼烷燃烧的热化学方程式,则0.5molB2H6(g)在该条件下完全燃烧时
| A.放出2165kJ热量 | B.吸收2165kJ热量 |
| C.放出1082.5kJ热量 | D.吸收1082.5kJ热量 |
您最近一年使用:0次
名校
解题方法
4 . (1)0.3mol气态高能燃料乙硼烷(B2H6)在氧气中燃烧,生成固态三氧化二硼和液态水放出649.5kJ热量,其热化学方程式为:_______ ;又已知H2O(l)=H2O(g) ΔH=+44kJ/mol,则11.2L(标准状况)乙硼烷完全燃烧生成气态水时放出的热量是_______ kJ。
(2)已知H—H键键能为436kJ·mol-1,H—N键键能为391kJ·mol-1,根据化学方程式:N2+3H2⇌2NH3 ΔH=-92.4kJ·mol-1,则N≡N键键能是_______ 。
(3)1mol氧气与足量氢气反应生成水蒸气放热483.6kJ,写出该反应的热化学方程式:_______ 。若1g水蒸气转化成液态水放热2.444kJ,写出表示氢气燃烧热的热化学方程式:_______ 。
(4)含11.2gKOH的稀溶液与1L0.1mol·L-1的H2SO4溶液反应放出11.46kJ的热量,该离子反应的热化学方程式为_______ ,则KOH与H2SO4反应的中和热为_______ 。
(5)已知:①C(s)+O2(g)=CO2(g) ΔH1=-393.5kJ·mol-1
②2CO(g)+O2(g)=2CO2(g) ΔH2=-566kJ·mol-1
③TiO2(s)+2Cl2(g)=TiCl4(s)+O2(g) ΔH3=+141kJ·mol-1
则TiO2(s)+2Cl2(g)+2C(s)=TiCl4(s)+2CO(g)的ΔH=_______ 。
(2)已知H—H键键能为436kJ·mol-1,H—N键键能为391kJ·mol-1,根据化学方程式:N2+3H2⇌2NH3 ΔH=-92.4kJ·mol-1,则N≡N键键能是
(3)1mol氧气与足量氢气反应生成水蒸气放热483.6kJ,写出该反应的热化学方程式:
(4)含11.2gKOH的稀溶液与1L0.1mol·L-1的H2SO4溶液反应放出11.46kJ的热量,该离子反应的热化学方程式为
(5)已知:①C(s)+O2(g)=CO2(g) ΔH1=-393.5kJ·mol-1
②2CO(g)+O2(g)=2CO2(g) ΔH2=-566kJ·mol-1
③TiO2(s)+2Cl2(g)=TiCl4(s)+O2(g) ΔH3=+141kJ·mol-1
则TiO2(s)+2Cl2(g)+2C(s)=TiCl4(s)+2CO(g)的ΔH=
您最近一年使用:0次
5 . 下列依据热化学方程式得出的结论正确的是
A.若  ,则 ,则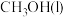 的燃烧热为 的燃烧热为 |
B.若  ,则红磷比白磷稳定 ,则红磷比白磷稳定 |
C.已知  ,则 ,则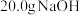 固体与稀盐酸完全中和,放出 固体与稀盐酸完全中和,放出 的热量 的热量 |
D.已知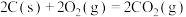  , ,  ,则 ,则 |
您最近一年使用:0次
2021-01-10更新
|
523次组卷
|
7卷引用:广东省台山市华侨中学2020-2021学年高二上学期第二次月考化学试题
解题方法
6 . 航天燃料从液态变为固态,是一项技术突破。铍是高效率的火箭材料,燃烧时放出巨大的能量,每千克的铍完全燃烧放出的热量为62700kJ。则铍燃烧的热化学方程式正确的是
A.Be+ O2=BeO ΔH=-564.3kJ·mol-1 O2=BeO ΔH=-564.3kJ·mol-1 |
B.Be(s)+ O2(g)=BeO(s) ΔH=+564.3kJ·mol-1 O2(g)=BeO(s) ΔH=+564.3kJ·mol-1 |
C.Be(s)+ O2(g)=BeO(s) ΔH=-564.3kJ·mol-1 O2(g)=BeO(s) ΔH=-564.3kJ·mol-1 |
D.Be(s)+ O2(g)=BeO(g) ΔH=-564.3kJ O2(g)=BeO(g) ΔH=-564.3kJ |
您最近一年使用:0次
解题方法
7 . 已知几种烷烃的燃烧热如下:
请回答下列问题∶
(1)写出丁烷燃烧热的热化学方程式为___________
(2)等质量的甲烷和乙烷充分燃烧放热较多的是___________
(3)某家用石油气(丙烷和丁烷的混合气)3.36L(标准状况下,下同)充分燃烧生成 (g)和
(g)和 (g)时放出的热量为365.9kJ,则石油气中丁烷的体积分数为
(g)时放出的热量为365.9kJ,则石油气中丁烷的体积分数为___________ (保留一位小数)。
| 名称 | 甲烷 | 乙烷 | 丙烷 | 丁烷 |
| △H/kJ·mol-1 | -891 | -1560 | -2220 | -2878 |
(1)写出丁烷燃烧热的热化学方程式为
(2)等质量的甲烷和乙烷充分燃烧放热较多的是
(3)某家用石油气(丙烷和丁烷的混合气)3.36L(标准状况下,下同)充分燃烧生成
 (g)和
(g)和 (g)时放出的热量为365.9kJ,则石油气中丁烷的体积分数为
(g)时放出的热量为365.9kJ,则石油气中丁烷的体积分数为
您最近一年使用:0次
名校
8 . 在燃烧1.12L(标准状况)CO与O2的混合气体时,放出5.66kJ的热量,在相同的状况下,最后产物的密度为原来气体密度的1.25倍,则CO的燃烧热为
| A.283kJ·mol-1 | B.-283kJ·mol-1 |
| C.-566kJ·mol-1 | D.566kJ·mol-1 |
您最近一年使用:0次
2021-06-03更新
|
447次组卷
|
6卷引用:江西省抚州市金溪县第一中学2019-2020学年高二上学期第二次月考化学试题
江西省抚州市金溪县第一中学2019-2020学年高二上学期第二次月考化学试题(已下线)1.2 燃烧热 能源-2021-2022学年高二化学课后培优练(人教版选修4)(已下线)第1章 化学反应的热效应(基础过关卷)-【高效检测】2021-2022学年高二化学章末测试卷(人教版2019选择性必修1)江西省南城第二中学2021-2022学年高二上学期第一次月考化学试题四川省泸州市泸县第一中学2023-2024学年高二上学期11月期中考试化学试题江西省宜春市丰城市东煌学校2023-2024学年高二上学期11月期中化学试题
9 . 汽车在行驶过程中有如下反应发生:
ⅰ.N2(g)+O2(g) ⇌2NO(g)ΔH=+180.7 kJ·mol-1
ⅱ.2NO(g)+2CO(g) ⇌N2(g)+2CO2(g)ΔH=-746.5 kJ·mol-1
(1)能表示CO燃烧热的热化学方程式为___________ 。
(2)反应ⅱ在___________ (填“较高”或“较低”)温度下能自发进行。
(3)T温度时,向10 L恒容密闭容器中充入2 molNO和2molCO发生反应ⅱ,5min时达到平衡,测得0~5min内该反应速率v(N2)=0.016 mol·L-1·min-1
①T温度时,该反应的平衡常数K=___________ 。
②平衡时容器内压强与起始时容器内压强之比为___________ 。
(4)一定条件下,向起始容积为5 L的恒压密闭容器中充入1 mol N2和1 mol O2发生反应ⅰ。O2的平衡转化率[α(O2)]与温度(T)的关系如图1所示;正反应的平衡常数(K正)与温度(T)的关系如图2所示。
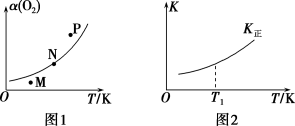
①图1中,M、N、P三点所对应的状态下,v正>v逆的是___________ (填字母),理由为___________ 。
②T1温度时,K正=1,则O2的平衡转化率为___________ (保留三位有效数字)。
ⅰ.N2(g)+O2(g) ⇌2NO(g)ΔH=+180.7 kJ·mol-1
ⅱ.2NO(g)+2CO(g) ⇌N2(g)+2CO2(g)ΔH=-746.5 kJ·mol-1
(1)能表示CO燃烧热的热化学方程式为
(2)反应ⅱ在
(3)T温度时,向10 L恒容密闭容器中充入2 molNO和2molCO发生反应ⅱ,5min时达到平衡,测得0~5min内该反应速率v(N2)=0.016 mol·L-1·min-1
①T温度时,该反应的平衡常数K=
②平衡时容器内压强与起始时容器内压强之比为
(4)一定条件下,向起始容积为5 L的恒压密闭容器中充入1 mol N2和1 mol O2发生反应ⅰ。O2的平衡转化率[α(O2)]与温度(T)的关系如图1所示;正反应的平衡常数(K正)与温度(T)的关系如图2所示。

①图1中,M、N、P三点所对应的状态下,v正>v逆的是
②T1温度时,K正=1,则O2的平衡转化率为
您最近一年使用:0次
名校
解题方法
10 . Ⅰ.已知下列热化学方程式:
①2H2(g)+O2(g)=2H2O(l) △H=-570kJ/mol
②2H2O(g)=2H2(g)+O2(g) △H=+483.6kJ/mol
③2CO(g)=2C(s)+O2(g) △H=+220.8kJ/mol
④2C(s)+2O2(g)=2CO2(g) △H=-787kJ/mol
回答下列问题:
(1)上述反应中属于放热反应的是______ (填写序号)。
(2)H2的燃烧热为______ 。
(3)燃烧10gH2生成液态水,放出的热量为______ 。
(4)C(s)的燃烧热的热化学方程式为______
(5)已知:1L1mol/LH2SO4溶液与2L1mol/LNaOH溶液完全反应,放出114.6kJ的热量,由此推知H2SO4与NaOH发生中和反应,写出该中和热的热化学方程式为______ 。
Ⅱ.已知:工业上制二甲醚是在一定温度(230~280℃)、压强(2.0~10.0MPa)和催化剂作用下进行的,反应器中发生了下列反应:
CO(g)+2H2(g)=CH3OH(g) ΔH1=-90.7kJ·mol-1 ①
2CH3OH(g)=CH3OCH3(g)+H2O(g) ΔH2=-23.5kJ·mol-1 ②
CO(g)+H2O(g)=CO2(g)+H2(g) ΔH3=-41.2kJ·mol-1 ③
(6)反应器中的总反应可表示为3CO(g)+3H2(g)⇌CH3OCH3(g)+CO2(g),计算该反应的ΔH=______ 。
①2H2(g)+O2(g)=2H2O(l) △H=-570kJ/mol
②2H2O(g)=2H2(g)+O2(g) △H=+483.6kJ/mol
③2CO(g)=2C(s)+O2(g) △H=+220.8kJ/mol
④2C(s)+2O2(g)=2CO2(g) △H=-787kJ/mol
回答下列问题:
(1)上述反应中属于放热反应的是
(2)H2的燃烧热为
(3)燃烧10gH2生成液态水,放出的热量为
(4)C(s)的燃烧热的热化学方程式为
(5)已知:1L1mol/LH2SO4溶液与2L1mol/LNaOH溶液完全反应,放出114.6kJ的热量,由此推知H2SO4与NaOH发生中和反应,写出该中和热的热化学方程式为
Ⅱ.已知:工业上制二甲醚是在一定温度(230~280℃)、压强(2.0~10.0MPa)和催化剂作用下进行的,反应器中发生了下列反应:
CO(g)+2H2(g)=CH3OH(g) ΔH1=-90.7kJ·mol-1 ①
2CH3OH(g)=CH3OCH3(g)+H2O(g) ΔH2=-23.5kJ·mol-1 ②
CO(g)+H2O(g)=CO2(g)+H2(g) ΔH3=-41.2kJ·mol-1 ③
(6)反应器中的总反应可表示为3CO(g)+3H2(g)⇌CH3OCH3(g)+CO2(g),计算该反应的ΔH=
您最近一年使用:0次



