名校
解题方法
1 . 回收利用含硫烟气有利于节约资源、保护环境。
I.含H2S的烟气回收
(1)将一部分含H2S的烟气在空气中燃烧,将燃烧所得产物与剩余烟气混合,冷却后可回收得到硫磺(S8)。该工艺中涉及反应如下:
反应1: ;
;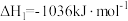
反应2: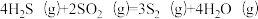 ;
;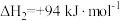
反应3: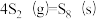 ;
;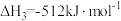
①反应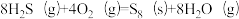 的△H=
的△H=_______ kJ∙mol-1。
②相同条件下需控制反应1与反应2中的烟气体积比为1:2的原因是_______ 。
Ⅱ.含SO2的烟气回收
(2)以FeS2/Al2O3为催化剂,用H2还原SO2制S。
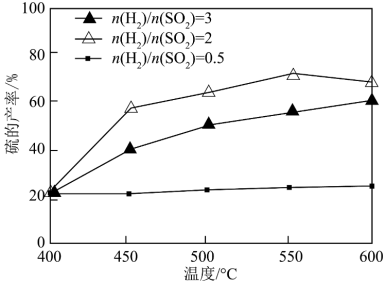
其他条件一定,改变起始时H2与SO2的比例,反应相同时间,测得S的产率随温度的变化关系如图所示。500℃,n(H2)/n(SO2)=3时硫的产率比n(H2)/n(SO2)=2时小的原因可能是_______ 。
(3)以V2O5/炭基材料为催化剂,SO2在炭表面被氧气催化氧化为SO3,SO3再转化为硫酸盐等。
①V2O5/炭基材料脱硫涉及反应: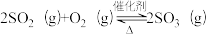 ,下列关于该反应的说法正确的是
,下列关于该反应的说法正确的是_______ (填字母序号)。
a.通入过量空气,可提高SO2的平衡转化率
b.当n(SO2):n(SO3)=l:1时,可判断反应达到平衡
c.使SO3液化从平衡体系中分离,能加快正反应速率,增大SO2转化率
②450℃、在V2O5催化下,SO2和O2的反应过程是按照如下两步完成的:
反应I:_______(快反应)
反应Ⅱ: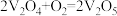 (慢反应)
(慢反应)
请补充上述反应的化学方程式_______ ,决定总反应速率快慢的是反应_______ (填“I”或“Ⅱ”)。
Ⅲ.工业上可采取多种方法减少SO2的排放,回答下列方法中的问题。
(4)方法1(双碱法):用NaOH溶液吸收SO2,并用CaO使NaOH再生NaOH溶液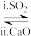 Na2SO3溶液
Na2SO3溶液
①写出过程i的离子方程式:_______ 。
②CaO在水中存在如下转化: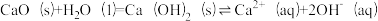
从平衡移动的角度,简述过程i中NaOH再生的原理:_______ 。
方法2:用氨水除去SO2
③已知25℃,NH3·H2O的 ,H2SO3的
,H2SO3的 ,
, 。若氨水的浓度为2.0mol∙L-1,溶液中的c(OH-)=
。若氨水的浓度为2.0mol∙L-1,溶液中的c(OH-)=_______ mol∙L-1。将SO2通入该氨水中,当c(OH-)降至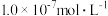 时,溶液中的
时,溶液中的
_______ 。
I.含H2S的烟气回收
(1)将一部分含H2S的烟气在空气中燃烧,将燃烧所得产物与剩余烟气混合,冷却后可回收得到硫磺(S8)。该工艺中涉及反应如下:
反应1:
 ;
;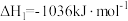
反应2:
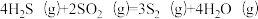 ;
;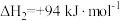
反应3:
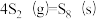 ;
;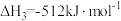
①反应
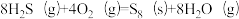 的△H=
的△H=②相同条件下需控制反应1与反应2中的烟气体积比为1:2的原因是
Ⅱ.含SO2的烟气回收
(2)以FeS2/Al2O3为催化剂,用H2还原SO2制S。
其他条件一定,改变起始时H2与SO2的比例,反应相同时间,测得S的产率随温度的变化关系如图所示。500℃,n(H2)/n(SO2)=3时硫的产率比n(H2)/n(SO2)=2时小的原因可能是

(3)以V2O5/炭基材料为催化剂,SO2在炭表面被氧气催化氧化为SO3,SO3再转化为硫酸盐等。
①V2O5/炭基材料脱硫涉及反应:
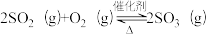 ,下列关于该反应的说法正确的是
,下列关于该反应的说法正确的是a.通入过量空气,可提高SO2的平衡转化率
b.当n(SO2):n(SO3)=l:1时,可判断反应达到平衡
c.使SO3液化从平衡体系中分离,能加快正反应速率,增大SO2转化率
②450℃、在V2O5催化下,SO2和O2的反应过程是按照如下两步完成的:
反应I:_______(快反应)
反应Ⅱ:
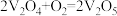 (慢反应)
(慢反应)请补充上述反应的化学方程式
Ⅲ.工业上可采取多种方法减少SO2的排放,回答下列方法中的问题。
(4)方法1(双碱法):用NaOH溶液吸收SO2,并用CaO使NaOH再生NaOH溶液
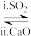 Na2SO3溶液
Na2SO3溶液①写出过程i的离子方程式:
②CaO在水中存在如下转化:
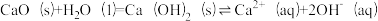
从平衡移动的角度,简述过程i中NaOH再生的原理:
方法2:用氨水除去SO2
③已知25℃,NH3·H2O的
 ,H2SO3的
,H2SO3的 ,
, 。若氨水的浓度为2.0mol∙L-1,溶液中的c(OH-)=
。若氨水的浓度为2.0mol∙L-1,溶液中的c(OH-)=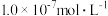 时,溶液中的
时,溶液中的
您最近一年使用:0次
名校
2 . 已知:①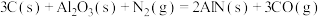
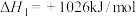
②
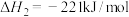 ;
;
③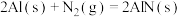
 ;
;
则反应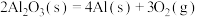 的
的 等于
等于
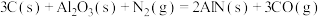
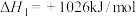
②

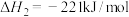 ;
;③
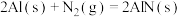
 ;
;则反应
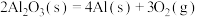 的
的 等于
等于| A.+753kJ/mol | B.-753kJ/mol | C.+3351kJ/mol | D.-3351kJ/mol |
您最近一年使用:0次
2023-01-10更新
|
587次组卷
|
4卷引用:江苏省无锡市匡园双语学校2023-2024学年高二下学期第一次月考化学试卷
江苏省无锡市匡园双语学校2023-2024学年高二下学期第一次月考化学试卷 湖北省孝感市2022-2023学年高二上学期1月期末考试化学试题广东省江门市第一中学2022-2023学年高二上学期期末考试(线上考试)化学试题(已下线)专题02 反应热的计算-【好题汇编】备战2023-2024学年高二化学上学期期末真题分类汇编(人教版2019)



