1 . 用 还原
还原 可合成
可合成 。回答下列问题:
。回答下列问题:
(1)利用 光解水制
光解水制 具有重要的经济价值,原理如图所示。
具有重要的经济价值,原理如图所示。 表面发生的电极反应式为
表面发生的电极反应式为_____ 。
写出 还原
还原 生成
生成 和
和 的热化学方程式:
的热化学方程式:_____ 。
(3)一定条件下,向某恒容密闭容器中充入2
 和3
和3
 反应生成
反应生成 和
和 ,起始时压强为
,起始时压强为 ,测得在相同时间内不同温度下
,测得在相同时间内不同温度下 的转化率如图所示。
的转化率如图所示。_____ 。
② K时,该反应的平衡常数
K时,该反应的平衡常数
_____ (列出计算式即可,不必化简。以分压代替浓度,分压=总压×物质的量分数)。
(4)为了探究浓度对反应速率的影响,473K时,向某恒容密闭容器中充入 和
和 进行实验,实验数据如下表所示:
进行实验,实验数据如下表所示:
该反应速率的通式为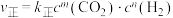 ,
,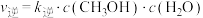 (
( 、
、 是只与温度有关的速率常数)。由表中数据可确定反应速率通式中
是只与温度有关的速率常数)。由表中数据可确定反应速率通式中
_____ 、
_____ 。实验发现,当实验1中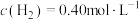 时达到平衡,请计算该温度下此反应的
时达到平衡,请计算该温度下此反应的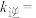
_____ 。
 还原
还原 可合成
可合成 。回答下列问题:
。回答下列问题:(1)利用
 光解水制
光解水制 具有重要的经济价值,原理如图所示。
具有重要的经济价值,原理如图所示。 表面发生的电极反应式为
表面发生的电极反应式为
| 共价键 |  |  |  |  |  |
键能/( ) ) | 464 | 358 | 799 | 432 | 411 |
 还原
还原 生成
生成 和
和 的热化学方程式:
的热化学方程式:(3)一定条件下,向某恒容密闭容器中充入2

 和3
和3
 反应生成
反应生成 和
和 ,起始时压强为
,起始时压强为 ,测得在相同时间内不同温度下
,测得在相同时间内不同温度下 的转化率如图所示。
的转化率如图所示。
②
 K时,该反应的平衡常数
K时,该反应的平衡常数
(4)为了探究浓度对反应速率的影响,473K时,向某恒容密闭容器中充入
 和
和 进行实验,实验数据如下表所示:
进行实验,实验数据如下表所示:| 实验 | 起始浓度/( ) ) | 初始速率/( ) ) | |
 |  | ||
| 1 | 0.25 | 1.00 | 0.45 |
| 2 | 0.25 | 2.00 | 3.60 |
| 3 | 2.00 | 1.00 | 3.6 |
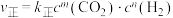 ,
,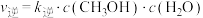 (
( 、
、 是只与温度有关的速率常数)。由表中数据可确定反应速率通式中
是只与温度有关的速率常数)。由表中数据可确定反应速率通式中

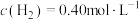 时达到平衡,请计算该温度下此反应的
时达到平衡,请计算该温度下此反应的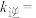
您最近一年使用:0次
2024-05-12更新
|
90次组卷
|
2卷引用:2024届青海省西宁市大通县高三下学期第二次模拟考试理科综合试题-高中化学
2 . 烯烃是重要的化工原料。回答下列问题:
(1)在浓硫酸的作用下,2—丁醇发生消去反应:
① (l)
(l) CH3CH2CH=CH2(1-丁烯,g)+H2O(g) ΔH1
CH3CH2CH=CH2(1-丁烯,g)+H2O(g) ΔH1
② (l)
(l) CH3CH=CHCH3(2-丁烯,g)+H2O(g) ΔH2
CH3CH=CHCH3(2-丁烯,g)+H2O(g) ΔH2
则1—丁烯转化为2—丁烯的热化学方程式为___________ 。
(2)某温度下,向一体积为10L的恒容密闭容器中充入1mol溴蒸气和1mol1—丁烯,发生反应:CH3CH2CH=CH2(g)+Br2(g) CH2=CHCH=CH2(g)+2HBr(g) △H>0,10min后,反应达到平衡,此时容器中物质的总物质的量为2.5mol。
CH2=CHCH=CH2(g)+2HBr(g) △H>0,10min后,反应达到平衡,此时容器中物质的总物质的量为2.5mol。
①达到平衡后,欲增大CH2=CHCH=CH2的产率,可采取的措施为___________ 。
②平衡时,溴蒸气的转化率为___________ ,0~10min内,v(HBr)=___________ mol·L·min-1。
③该温度下,反应的平衡常数K=___________ 。
(3)1,3—丁二烯在苯溶液中能发生聚合反应生成二聚体,该反应为可逆反应。不同温度下,溶液中1,3—丁二烯的浓度与反应时间的关系如图所示,下列说法正确的是___________(填标号)。

(4)工业上用电解丁醛的方法制备1—丁醇和丁酸的总反应为2CH3CH2CH2CHO+H2O CH3CH2CH2COOH+CH3CH2CH2CH2OH,电解装置示意图如图,阴极的电极反应式为
CH3CH2CH2COOH+CH3CH2CH2CH2OH,电解装置示意图如图,阴极的电极反应式为___________ ,生成的a为___________ (填名称)。

(1)在浓硫酸的作用下,2—丁醇发生消去反应:
①
 (l)
(l) CH3CH2CH=CH2(1-丁烯,g)+H2O(g) ΔH1
CH3CH2CH=CH2(1-丁烯,g)+H2O(g) ΔH1②
 (l)
(l) CH3CH=CHCH3(2-丁烯,g)+H2O(g) ΔH2
CH3CH=CHCH3(2-丁烯,g)+H2O(g) ΔH2则1—丁烯转化为2—丁烯的热化学方程式为
(2)某温度下,向一体积为10L的恒容密闭容器中充入1mol溴蒸气和1mol1—丁烯,发生反应:CH3CH2CH=CH2(g)+Br2(g)
 CH2=CHCH=CH2(g)+2HBr(g) △H>0,10min后,反应达到平衡,此时容器中物质的总物质的量为2.5mol。
CH2=CHCH=CH2(g)+2HBr(g) △H>0,10min后,反应达到平衡,此时容器中物质的总物质的量为2.5mol。①达到平衡后,欲增大CH2=CHCH=CH2的产率,可采取的措施为
②平衡时,溴蒸气的转化率为
③该温度下,反应的平衡常数K=
(3)1,3—丁二烯在苯溶液中能发生聚合反应生成二聚体,该反应为可逆反应。不同温度下,溶液中1,3—丁二烯的浓度与反应时间的关系如图所示,下列说法正确的是___________(填标号)。

| A.T1>T2 |
| B.c点的正反应速率小于c点的逆反应速率 |
| C.a点的正反应速率大于b点的逆反应速率 |
| D.b点时二聚体的浓度为0.45mol·L-1 |
 CH3CH2CH2COOH+CH3CH2CH2CH2OH,电解装置示意图如图,阴极的电极反应式为
CH3CH2CH2COOH+CH3CH2CH2CH2OH,电解装置示意图如图,阴极的电极反应式为
您最近一年使用:0次
2022-01-08更新
|
253次组卷
|
2卷引用:青海省海东市2022届高考一模理科综合化学试题
3 . 减少工业和生活废弃物的排放并合理开发利用,近年来受到了人们的普遍关注。
Ⅰ.利用工业废水中的CO2制取甲醇,反应为CO2+3H2 CH3OH+H2O。
CH3OH+H2O。
(1)已知下列反应的能量变化如图所示:
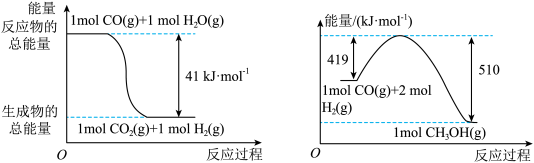
由二氧化碳和氢气制备甲醇的热化学方程式为____________________________ 。
Ⅱ.利用工业废气CO合成甲醇,反应为CO(g)+2H2(g) CH3OH(g)。
CH3OH(g)。
(2)一定条件下,在1 L密闭容器中充入0.6 mol CO和1.4 mol H2,8 min后达到平衡,CO的转化率为50%,则8 min内H2的平均反应速率为__________________ 。
(3)若反应原料是来自煤的气化,已知该反应的平衡常数表达式为K=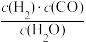 ,每生成1 mol H2需要吸收131.3 kJ的热量。写出该反应的热化学方程式
,每生成1 mol H2需要吸收131.3 kJ的热量。写出该反应的热化学方程式____________________________ 。
(4)T ℃时,能发生反应:2CH3OH(g) CH3OCH3(g)+H2O(g)。已知反应平衡常数为400,此温度下,在1 L密闭容器中加入一定量的甲醇,反应到某时刻测得各组分的物质的量浓度如表:
CH3OCH3(g)+H2O(g)。已知反应平衡常数为400,此温度下,在1 L密闭容器中加入一定量的甲醇,反应到某时刻测得各组分的物质的量浓度如表:
此刻正、逆反应速率的关系是v(正)_______ (填“>”、“<”或“=”)v(逆),平衡时c(CH3OCH3)是___________ 。
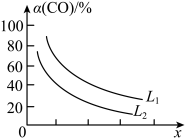
(5)已知反应3CO(g)+3H2(g) CH3OCH3(g)+CO2(g),CO的平衡转化率α(CO)与温度、压强的关系如图所示。图中X表示
CH3OCH3(g)+CO2(g),CO的平衡转化率α(CO)与温度、压强的关系如图所示。图中X表示_________ (填“温度”或“压强”),判断的理由是_______________________ 。
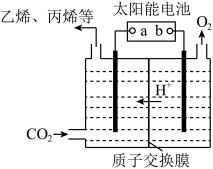
(6)强酸性电解质溶液中,用惰性电极电解CO2可转化为多种燃料,其原理如图所示。b为电源的_____ 极。电解时,生成乙烯的电极反应式为_________________________ 。
Ⅰ.利用工业废水中的CO2制取甲醇,反应为CO2+3H2
 CH3OH+H2O。
CH3OH+H2O。(1)已知下列反应的能量变化如图所示:

由二氧化碳和氢气制备甲醇的热化学方程式为
Ⅱ.利用工业废气CO合成甲醇,反应为CO(g)+2H2(g)
 CH3OH(g)。
CH3OH(g)。(2)一定条件下,在1 L密闭容器中充入0.6 mol CO和1.4 mol H2,8 min后达到平衡,CO的转化率为50%,则8 min内H2的平均反应速率为
(3)若反应原料是来自煤的气化,已知该反应的平衡常数表达式为K=
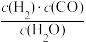 ,每生成1 mol H2需要吸收131.3 kJ的热量。写出该反应的热化学方程式
,每生成1 mol H2需要吸收131.3 kJ的热量。写出该反应的热化学方程式(4)T ℃时,能发生反应:2CH3OH(g)
 CH3OCH3(g)+H2O(g)。已知反应平衡常数为400,此温度下,在1 L密闭容器中加入一定量的甲醇,反应到某时刻测得各组分的物质的量浓度如表:
CH3OCH3(g)+H2O(g)。已知反应平衡常数为400,此温度下,在1 L密闭容器中加入一定量的甲醇,反应到某时刻测得各组分的物质的量浓度如表:| 物质 | CH3OH | CH3OCH3 | H2O |
| c/(mol·L-1) | 0.46 | 1.0 | 1.0 |
此刻正、逆反应速率的关系是v(正)

(5)已知反应3CO(g)+3H2(g)
 CH3OCH3(g)+CO2(g),CO的平衡转化率α(CO)与温度、压强的关系如图所示。图中X表示
CH3OCH3(g)+CO2(g),CO的平衡转化率α(CO)与温度、压强的关系如图所示。图中X表示
(6)强酸性电解质溶液中,用惰性电极电解CO2可转化为多种燃料,其原理如图所示。b为电源的
您最近一年使用:0次
2017-04-12更新
|
348次组卷
|
4卷引用:青海省西宁市2017届高三下学期复习检测一(一模)理综-化学试题
青海省西宁市2017届高三下学期复习检测一(一模)理综-化学试题(已下线)2019年5月1日 《每日一题》三轮复习-化学反应原理综合题(已下线)2019年5月16日 《每日一题》四轮复习——押高考化学第28题(1)新疆维吾尔自治区和田地区洛浦县2022-2023学年高二上学期11月期中考试化学试题



