解题方法
1 . 甲醇( )作为重要的清洁燃料和合成化学的关键前驱体,在化工行业需求旺盛。以
)作为重要的清洁燃料和合成化学的关键前驱体,在化工行业需求旺盛。以 为催化剂在水溶液中电催化二氧化碳还原为
为催化剂在水溶液中电催化二氧化碳还原为 和
和 的能量变化如图所示:
的能量变化如图所示:
 )作为重要的清洁燃料和合成化学的关键前驱体,在化工行业需求旺盛。以
)作为重要的清洁燃料和合成化学的关键前驱体,在化工行业需求旺盛。以 为催化剂在水溶液中电催化二氧化碳还原为
为催化剂在水溶液中电催化二氧化碳还原为 和
和 的能量变化如图所示:
的能量变化如图所示: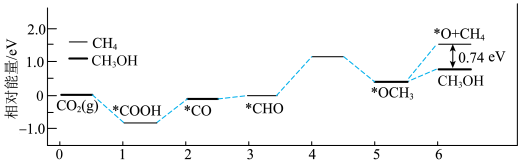
A.生成甲醇反应的决速步为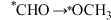 |
| B.两反应只涉及极性键的断裂和生成 |
| C.通过上图分析:甲烷比甲醇稳定 |
D.用 作催化剂可提高甲醇的选择性 作催化剂可提高甲醇的选择性 |
您最近一年使用:0次
解题方法
2 . 某化学反应X→Y分两步进行;①X→M;②M→Y。其能量变化如图所示,下列说法错误的是
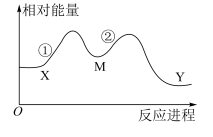

| A.M是该反应的催化剂,可降低该反应的焓变,提高该反应的速率 |
| B.该反应是放热反应 |
| C.X、Y、M三种物质中Y最稳定 |
| D.反应①是总反应的决速步骤 |
您最近一年使用:0次
解题方法
3 . 一个化学反应在给定条件(通常指温度、压强)下能否自发进行以及在什么条件下有可能按预期的方向发生,需寻求一种客观的判据,用它来判断一个化学反应能否正向自发进行。研究表明,可逆反应在适当条件下进行一段时间后一定会达到化学平衡状态。在研究了大量实验的基础上,人们发现可以用化学平衡常数来定量描述化学反应的限度。
(1)下列关于自发反应的叙述,正确的是___________。
(2)下列说法中正确的是___________。
(3)某温度下,可逆反应 的平衡常数为K。下列对K的说法正确的是___________。
的平衡常数为K。下列对K的说法正确的是___________。
(4)在一定温度下,下列反应的化学平衡常数数值如下:
①
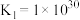
②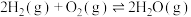
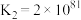
③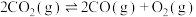
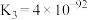
下列说法正确的是___________。
(5)在某密闭容器中把CO和 的混合物加热到800℃,存在平衡:
的混合物加热到800℃,存在平衡: ,且平衡常数
,且平衡常数 。若在2L的密闭容器中充入1molCO和1mol
。若在2L的密闭容器中充入1molCO和1mol 的混合物并加热到800℃,则平衡时CO的转化率为___________。
的混合物并加热到800℃,则平衡时CO的转化率为___________。
(6)地下水中的氮污染主要是由 引起的,人们对
引起的,人们对 的转化进行了长时间的研究,目前主要有物理方法、化学方法和生物方法,其中化学方法主要包含活泼金属还原法和催化反硝化法。催化反硝化法是一种经济可行的脱氮方法,其原理是在Pd/Cu双金属催化剂作用下,
的转化进行了长时间的研究,目前主要有物理方法、化学方法和生物方法,其中化学方法主要包含活泼金属还原法和催化反硝化法。催化反硝化法是一种经济可行的脱氮方法,其原理是在Pd/Cu双金属催化剂作用下, 将硝酸盐还原成氮气:
将硝酸盐还原成氮气: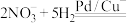

①氮肥 溶于水的过程中熵值
溶于水的过程中熵值___________ (填“增大”或“减小”),Pd/Cu双金属催化剂___________ (填“是”或“不是”)决定反应自发发生的决定因素。
②已知: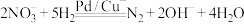 的
的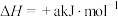 ,
, (a、b均为正值),该反应
(a、b均为正值),该反应___________ (填“能”“不能”或“无法判断是否能”)自发进行。
(7)在一定体积的密闭容器中进行如下化学反应:
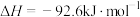 ,其化学平衡常数(K)和温度(T)的关系如下表所示:
,其化学平衡常数(K)和温度(T)的关系如下表所示:
①试判断
___________  (填写“>”、“=”或“<”)
(填写“>”、“=”或“<”)
②T℃( )的某时刻下,
)的某时刻下, ,
,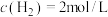 ,
, ,此时该反应是否处于平衡状态
,此时该反应是否处于平衡状态___________ (选填“是”或“否”),此时反应速率是
___________  (选择“>”、“=”或“<”),其原因是
(选择“>”、“=”或“<”),其原因是___________ 。
(1)下列关于自发反应的叙述,正确的是___________。
| A.自发反应的逆过程在相同条件下也必定是自发的 |
| B.铁在潮湿的空气中生锈属于非自发反应 |
| C.自发过程可以是物理过程,不一定是自发反应,而自发反应一定是自发过程 |
| D.自发反应与外界条件无关 |
A.若 , , ,化学反应在任何温度下都能自发进行 ,化学反应在任何温度下都能自发进行 |
B.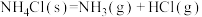 在室温下不能自发进行,则该反应的 在室温下不能自发进行,则该反应的 |
C. 在低温下能自发进行,则该反应的 在低温下能自发进行,则该反应的 |
| D.加入合适的催化剂能降低反应的活化能,从而改变反应的焓变 |
 的平衡常数为K。下列对K的说法正确的是___________。
的平衡常数为K。下列对K的说法正确的是___________。| A.温度越高,K一定越大 |
B.如果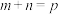 ,则 ,则 |
| C.若缩小反应器的容积,增大压强,则K增大 |
| D.K值越大,表明该反应越有利于C的生成,反应物的转化率越大 |
①

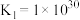
②
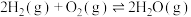
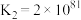
③
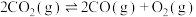
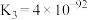
下列说法正确的是___________。
A.该温度下,反应①的平衡常数表达式为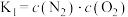 |
B.该温度下,反应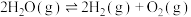 的平衡常数的数值约为 的平衡常数的数值约为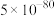 |
C.该温度下,反应①、反应②的逆反应、反应③产生 的倾向由大到小的顺序为 的倾向由大到小的顺序为 |
| D.以上说法都不正确 |
 的混合物加热到800℃,存在平衡:
的混合物加热到800℃,存在平衡: ,且平衡常数
,且平衡常数 。若在2L的密闭容器中充入1molCO和1mol
。若在2L的密闭容器中充入1molCO和1mol 的混合物并加热到800℃,则平衡时CO的转化率为___________。
的混合物并加热到800℃,则平衡时CO的转化率为___________。| A.40% | B.50% | C.60% | D.83.3% |
 引起的,人们对
引起的,人们对 的转化进行了长时间的研究,目前主要有物理方法、化学方法和生物方法,其中化学方法主要包含活泼金属还原法和催化反硝化法。催化反硝化法是一种经济可行的脱氮方法,其原理是在Pd/Cu双金属催化剂作用下,
的转化进行了长时间的研究,目前主要有物理方法、化学方法和生物方法,其中化学方法主要包含活泼金属还原法和催化反硝化法。催化反硝化法是一种经济可行的脱氮方法,其原理是在Pd/Cu双金属催化剂作用下, 将硝酸盐还原成氮气:
将硝酸盐还原成氮气: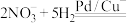

①氮肥
 溶于水的过程中熵值
溶于水的过程中熵值②已知:
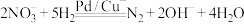 的
的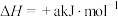 ,
, (a、b均为正值),该反应
(a、b均为正值),该反应(7)在一定体积的密闭容器中进行如下化学反应:

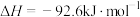 ,其化学平衡常数(K)和温度(T)的关系如下表所示:
,其化学平衡常数(K)和温度(T)的关系如下表所示:| T℃ | 25 | 125 | 225 |
| K | 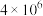 |  |  |

 (填写“>”、“=”或“<”)
(填写“>”、“=”或“<”)②T℃(
 )的某时刻下,
)的某时刻下, ,
,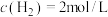 ,
, ,此时该反应是否处于平衡状态
,此时该反应是否处于平衡状态
 (选择“>”、“=”或“<”),其原因是
(选择“>”、“=”或“<”),其原因是
您最近一年使用:0次
4 . 下列说法正确的是
| A.增大反应物的浓度,可以提高活化分子百分数 |
| B.通过压缩体积增大压强,可提高单位体积内活化分子数,从而增大反应速率 |
| C.使用催化剂能降低反应的活化能,增大活化分子百分数,从而改变Δ H |
| D.反应物分子的每一次碰撞都是有效碰撞 |
您最近一年使用:0次
解题方法
5 .  与ICl的反应分两步完成,其能量曲线如下图所示。
与ICl的反应分两步完成,其能量曲线如下图所示。
反应②: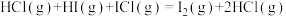
下列有关说法正确的是
 与ICl的反应分两步完成,其能量曲线如下图所示。
与ICl的反应分两步完成,其能量曲线如下图所示。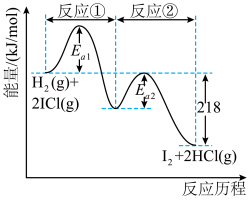

反应②:
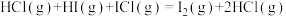
下列有关说法正确的是
A.由于 ,所以该化学反应的速率主要由反应②决定 ,所以该化学反应的速率主要由反应②决定 |
| B.基元反应①为放热反应,基元反应②反应物的总键能大于生成物的总键能 |
C. |
| D.升高温度,活化分子百分数增加,化学反应速率加快 |
您最近一年使用:0次
2024-03-20更新
|
137次组卷
|
3卷引用:山东省枣庄薛城实验中学等校2023-2023学年高二上学期12月大联考化学试题
解题方法
6 . 2007年2月,中国首条“生态马路”在上海复兴路隧道建成,它运用了“光触媒”技术,在路面涂上一种光催化剂涂料,可将汽车尾气中45%的NO和CO转化成N2和CO2。下列对此反应的叙述中正确的
| A.使用光催化剂不改变反应速率 |
| B.使用光催化剂能增大NO的转化率 |
| C.升高温度能加快反应速率 |
| D.改变压强对反应速率无影响 |
您最近一年使用:0次
名校
解题方法
7 .  可活化
可活化 放出
放出 ,其反应历程如图所示:
,其反应历程如图所示:

下列关于活化历程的说法正确的是
 可活化
可活化 放出
放出 ,其反应历程如图所示:
,其反应历程如图所示:
下列关于活化历程的说法正确的是
A.该转化过程 >0 >0 |
B.该反应过程中,最大能垒(活化能)为204.32 |
C.在此反应过程中 的成键数目未发生变化 的成键数目未发生变化 |
| D.整个过程中,Ni是该反应的催化剂 |
您最近一年使用:0次
名校
8 . 对于在一定条件下进行的化学反应,改变下列条件,可以提高反应物中的活化分子百分数的是
①升高温度②加入催化剂③增大体系压强④增大反应物浓度
①升高温度②加入催化剂③增大体系压强④增大反应物浓度
| A.①② | B.②③ | C.③④ | D.①④ |
您最近一年使用:0次
解题方法
9 . 我国学者结合实验和计算机模拟结果,研究了在催化剂(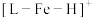 )表面上某物质发生分解反应的历程,如图所示:
)表面上某物质发生分解反应的历程,如图所示:
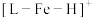 )表面上某物质发生分解反应的历程,如图所示:
)表面上某物质发生分解反应的历程,如图所示:
A.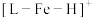 可有效提高反应物的平衡转化率 可有效提高反应物的平衡转化率 |
B.该过程的总反应为 |
C. 浓度过大或者过小,均导致反应速率降低 浓度过大或者过小,均导致反应速率降低 |
D.该历程中最大的能垒(基元反应活化能)为 |
您最近一年使用:0次
2024-02-01更新
|
90次组卷
|
2卷引用:山东省德州市2023-2024学年高二上学期期末考试化学试题
名校
解题方法
10 . 大气中的臭氧层能有效阻挡紫外线。臭氧层中O3分解过程如图所示,下列说法正确的是
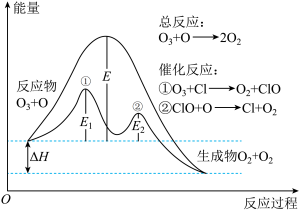

| A.催化反应①、②和总反应均是放热反应 |
| B.决定O3分解反应速率的是催化反应② |
| C.E1是催化反应①正反应的活化能 |
| D.Cl 是反应的催化剂,改变了反应历程,降低了△H |
您最近一年使用:0次



