解题方法
1 . 在碳循环中,以 为原料生产尿素的反应历程与能量变化示意图如图所示。
为原料生产尿素的反应历程与能量变化示意图如图所示。
_______ 0(填“>”、“<”或“=”)。从图像分析决定生产尿素的总反应的反应速率的步骤是第_______ 步反应,并说明理由______________ 。
 为原料生产尿素的反应历程与能量变化示意图如图所示。
为原料生产尿素的反应历程与能量变化示意图如图所示。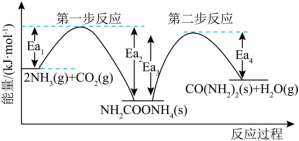

您最近半年使用:0次
2 . 用钌(Ru)基催化剂催化CO2(g)和H2(g)的反应示意图如图,当反应生成46g液态HCOOH时放出31.2kJ的热量。下列说法正确的是

| A.反应历程中存在极性键、非极性键的断裂与形成 |
| B.图示中物质Ⅰ、Ⅱ、Ⅲ均为该反应的催化剂 |
| C.使用催化剂可以降低反应的活化能,从而改变反应的焓变 |
D.由题意知:HCOOH(l)=CO2(g)+H2(g) ΔH=+31.2kJ mol﹣1 mol﹣1 |
您最近半年使用:0次
3 . 工业上可采用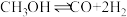 的方法来制取高纯度的
的方法来制取高纯度的 和
和 。我国学者采用量子力学方法,通过计算机模拟,研究了在钯基催化剂表面上甲醇制氢的反应历程,其中吸附在钯催化剂表面上的物种用*标注。甲醇(
。我国学者采用量子力学方法,通过计算机模拟,研究了在钯基催化剂表面上甲醇制氢的反应历程,其中吸附在钯催化剂表面上的物种用*标注。甲醇( )脱氢反应的第一步历程,有如下两种可能方式(其中
)脱氢反应的第一步历程,有如下两种可能方式(其中 、
、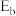 为活化能):
为活化能):
方式①: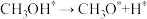
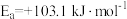
方式②: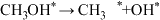
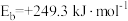
图为计算机模拟的各步反应的能量变化示意图。
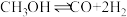 的方法来制取高纯度的
的方法来制取高纯度的 和
和 。我国学者采用量子力学方法,通过计算机模拟,研究了在钯基催化剂表面上甲醇制氢的反应历程,其中吸附在钯催化剂表面上的物种用*标注。甲醇(
。我国学者采用量子力学方法,通过计算机模拟,研究了在钯基催化剂表面上甲醇制氢的反应历程,其中吸附在钯催化剂表面上的物种用*标注。甲醇( )脱氢反应的第一步历程,有如下两种可能方式(其中
)脱氢反应的第一步历程,有如下两种可能方式(其中 、
、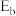 为活化能):
为活化能):方式①:
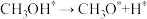
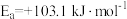
方式②:
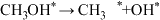
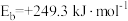
图为计算机模拟的各步反应的能量变化示意图。
| A.主要历经方式② |
B.总反应的焓变( )大于0 )大于0 |
C.最小能垒(活化能)为 |
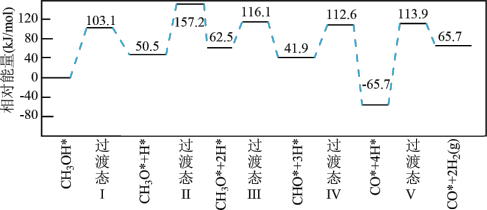
D.焓变最小的基元反应为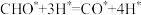 |
您最近半年使用:0次
解题方法
4 . 甲醇( )作为重要的清洁燃料和合成化学的关键前驱体,在化工行业需求旺盛。以
)作为重要的清洁燃料和合成化学的关键前驱体,在化工行业需求旺盛。以 为催化剂在水溶液中电催化二氧化碳还原为
为催化剂在水溶液中电催化二氧化碳还原为 和
和 的能量变化如图所示:
的能量变化如图所示:
 )作为重要的清洁燃料和合成化学的关键前驱体,在化工行业需求旺盛。以
)作为重要的清洁燃料和合成化学的关键前驱体,在化工行业需求旺盛。以 为催化剂在水溶液中电催化二氧化碳还原为
为催化剂在水溶液中电催化二氧化碳还原为 和
和 的能量变化如图所示:
的能量变化如图所示: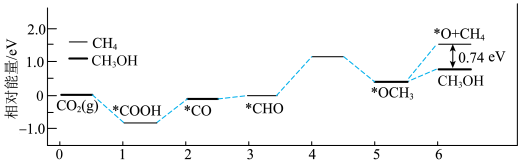
A.生成甲醇反应的决速步为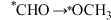 |
| B.两反应只涉及极性键的断裂和生成 |
| C.通过上图分析:甲烷比甲醇稳定 |
D.用 作催化剂可提高甲醇的选择性 作催化剂可提高甲醇的选择性 |
您最近半年使用:0次
5 . 空气中 含量的控制和
含量的控制和 资源利用,具有重要意义。
资源利用,具有重要意义。
(1)燃煤烟气中的 捕集可通过如下所示的物质转化实现。
捕集可通过如下所示的物质转化实现。

“吸收”后所得的 溶液与石灰乳反应的化学方程式为
溶液与石灰乳反应的化学方程式为______ ;载人航天器内,常用LiOH固体而很少用KOH固体吸收空气中的 ,其原因是
,其原因是______ 。
(2)二氧化碳催化加氢制甲醇,涉及反应有:
反应Ⅰ.

反应Ⅱ.

反应Ⅲ.

某压强下在体积固定的密闭容器中,按照 投料发生反应Ⅰ、Ⅱ、Ⅲ。
投料发生反应Ⅰ、Ⅱ、Ⅲ。
平衡时,CO、 在含碳产物中物质的量分数及
在含碳产物中物质的量分数及 转化率随温度的变化如下图一所示。
转化率随温度的变化如下图一所示。

①n曲线代表的物质为______ 。
②在150~250℃范围内, 转化率随温度升高而降低的原因是
转化率随温度升高而降低的原因是______ 。
(3) 和
和 反应制备
反应制备 的反应机理如下图二所示(带*的表示吸附在催化剂表面)
的反应机理如下图二所示(带*的表示吸附在催化剂表面)

①研究表明,图中过程ⅱ的活化能小但实际反应速率慢,是控速步骤,导致该步反应速率小的原因可能是______ 。
A. 对该反应有阻碍作用 B.其它物种的存在削弱了同一吸附位上H的吸附
对该反应有阻碍作用 B.其它物种的存在削弱了同一吸附位上H的吸附
C.温度变化导致活化能增大 D.温度变化导致平衡常数减小
②已知:图中HCOO为甲酸物种,结构是 ,
,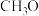 为甲氧基物种。从化学键视角将图中ⅰ与ⅱ的过程可描述为
为甲氧基物种。从化学键视角将图中ⅰ与ⅱ的过程可描述为______ 。
 含量的控制和
含量的控制和 资源利用,具有重要意义。
资源利用,具有重要意义。(1)燃煤烟气中的
 捕集可通过如下所示的物质转化实现。
捕集可通过如下所示的物质转化实现。
“吸收”后所得的
 溶液与石灰乳反应的化学方程式为
溶液与石灰乳反应的化学方程式为 ,其原因是
,其原因是(2)二氧化碳催化加氢制甲醇,涉及反应有:
反应Ⅰ.


反应Ⅱ.


反应Ⅲ.


某压强下在体积固定的密闭容器中,按照
 投料发生反应Ⅰ、Ⅱ、Ⅲ。
投料发生反应Ⅰ、Ⅱ、Ⅲ。平衡时,CO、
 在含碳产物中物质的量分数及
在含碳产物中物质的量分数及 转化率随温度的变化如下图一所示。
转化率随温度的变化如下图一所示。
①n曲线代表的物质为
②在150~250℃范围内,
 转化率随温度升高而降低的原因是
转化率随温度升高而降低的原因是(3)
 和
和 反应制备
反应制备 的反应机理如下图二所示(带*的表示吸附在催化剂表面)
的反应机理如下图二所示(带*的表示吸附在催化剂表面)
①研究表明,图中过程ⅱ的活化能小但实际反应速率慢,是控速步骤,导致该步反应速率小的原因可能是
A.
 对该反应有阻碍作用 B.其它物种的存在削弱了同一吸附位上H的吸附
对该反应有阻碍作用 B.其它物种的存在削弱了同一吸附位上H的吸附C.温度变化导致活化能增大 D.温度变化导致平衡常数减小
②已知:图中HCOO为甲酸物种,结构是
 ,
,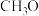 为甲氧基物种。从化学键视角将图中ⅰ与ⅱ的过程可描述为
为甲氧基物种。从化学键视角将图中ⅰ与ⅱ的过程可描述为
您最近半年使用:0次
解题方法
6 . 接触法制硫酸的工艺流程中的关键步骤是SO2的催化氧化: ,在催化剂表面的反应历程如下:
,在催化剂表面的反应历程如下:
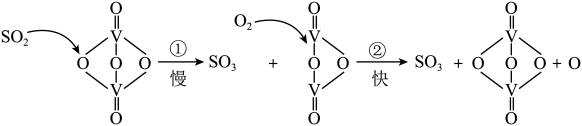
下列说法正确的是
 ,在催化剂表面的反应历程如下:
,在催化剂表面的反应历程如下:
下列说法正确的是
| A.过程中既有V-O键的断裂,又有V-O键的形成 |
| B.该反应的中间产物是V2O5 |
| C.反应①的活化能比反应②大 |
| D.反应放热,为提高SO2转化率,应尽可能在较低温度下反应 |
您最近半年使用:0次
解题方法
7 . 下列对有关事实或解释正确的是
| 编号 | 事实 | 解释 |
| A | 锌与稀盐酸反应,加入氯化钠固体,速率加快 | 增大了氯离子浓度,反应速率加快 |
| B | 锌与稀硫酸反应,滴入较多硫酸铜溶液,生成氢气的速率减慢 | 锌置换铜的反应干扰了锌置换氢的反应,致使生成氢气的速率变慢 |
| C |  的双氧水中加入二氧化锰粉末,分解速率迅速加快 的双氧水中加入二氧化锰粉末,分解速率迅速加快 | 降低了反应的焓变,活化分子数增多,有效碰撞增多,速率加快 |
| D | 面粉生产车间容易发生爆炸 | 固体表面积大,反应速率加快 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
8 . CO2是一种温室气体,对人类的生存环境产生巨大的影响,将CO2作为原料转化为有用化学品,对实现碳中和及生态环境保护有着重要意义。
Ⅰ.工业上以CO2和NH3为原料合成尿素,在合成塔中存在如下转化:

(1)液相中,合成尿素的热化学方程式为:2NH3(l)+CO2(l) H2O(l)+NH2CONH2(l) ΔH=
H2O(l)+NH2CONH2(l) ΔH=___________ kJ/mol。
Ⅱ.可利用CO2和CH4催化制备合成气(CO、H2),在一定温度下容积为1 L密闭容器中,充入等物质的量CH4和CO2,加入Ni/Al2O3使其发生反应:CH4(g)+CO2(g) 2CO(g)+2H2(g)。
2CO(g)+2H2(g)。
(2)制备“合成气”反应历程分两步:
上述反应中C(ads)为吸附性活性炭,反应历程的能量图变化如下图所示:
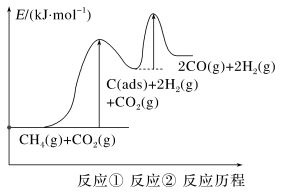
①反应速率快慢比较:反应①___________ 反应②(填“>”“<”或“=”),请依据有效碰撞理论微观探析其原因___________ 。
②一定温度下,反应CH4(g)+CO2(g) 2CO(g)+2H2(g)的平衡常数K=
2CO(g)+2H2(g)的平衡常数K=___________ (用k1、k2、k3、k4表示)。
(3)制备合成气(CO、H2)过程中发生副反应:CO2(g)+H2(g) CO(g)+H2O(g) ΔH2=+41.0 kJ/mol,在刚性密闭容器中,进料比
CO(g)+H2O(g) ΔH2=+41.0 kJ/mol,在刚性密闭容器中,进料比 分别等于1.0、1.5、2.0,且反应达到平衡状态。反应体系中,
分别等于1.0、1.5、2.0,且反应达到平衡状态。反应体系中, 随温度变化的关系如图所示:
随温度变化的关系如图所示:
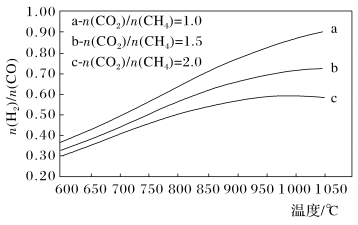
随着进料比 的增加,
的增加, 的值
的值___________ (填“增大”、“不变”或“减小”),其原因是___________ 。
Ⅰ.工业上以CO2和NH3为原料合成尿素,在合成塔中存在如下转化:

(1)液相中,合成尿素的热化学方程式为:2NH3(l)+CO2(l)
 H2O(l)+NH2CONH2(l) ΔH=
H2O(l)+NH2CONH2(l) ΔH=Ⅱ.可利用CO2和CH4催化制备合成气(CO、H2),在一定温度下容积为1 L密闭容器中,充入等物质的量CH4和CO2,加入Ni/Al2O3使其发生反应:CH4(g)+CO2(g)
 2CO(g)+2H2(g)。
2CO(g)+2H2(g)。(2)制备“合成气”反应历程分两步:
| 步骤 | 反应 | 正反应速率方程 | 逆反应速率方程 |
| 反应① | CH4(g) C(ads)+2H2(g) C(ads)+2H2(g) | v正=k1·c(CH4) | v逆=k2·c2(H2) |
| 反应② | C(ads)+CO2(g) 2CO(g) 2CO(g) | v正=k3·c(CO2) | v逆=k4·c2(CO) |

①反应速率快慢比较:反应①
②一定温度下,反应CH4(g)+CO2(g)
 2CO(g)+2H2(g)的平衡常数K=
2CO(g)+2H2(g)的平衡常数K=(3)制备合成气(CO、H2)过程中发生副反应:CO2(g)+H2(g)
 CO(g)+H2O(g) ΔH2=+41.0 kJ/mol,在刚性密闭容器中,进料比
CO(g)+H2O(g) ΔH2=+41.0 kJ/mol,在刚性密闭容器中,进料比 分别等于1.0、1.5、2.0,且反应达到平衡状态。反应体系中,
分别等于1.0、1.5、2.0,且反应达到平衡状态。反应体系中, 随温度变化的关系如图所示:
随温度变化的关系如图所示:
随着进料比
 的增加,
的增加, 的值
的值
您最近半年使用:0次
9 . 下列说法中正确的是
①充有氖气的霓虹灯管通电时会发出红色光的主要原因是电子由基态向激发态跃迁时吸收除红光以外的光线② 不符合泡利原理③增大压强,活化分子百分数增大,单位时间内有效碰撞次数增多,化学反应速率加快④
不符合泡利原理③增大压强,活化分子百分数增大,单位时间内有效碰撞次数增多,化学反应速率加快④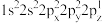 违反了洪特规则,是激发态原子的电子排布⑤钠离子的最高能级为3s⑥25℃时,将
违反了洪特规则,是激发态原子的电子排布⑤钠离子的最高能级为3s⑥25℃时,将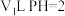 的盐酸与
的盐酸与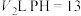 的氢氧化钠溶液混合后
的氢氧化钠溶液混合后 ,则
,则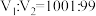 ⑦F的最高能级的电子云轮廓图:
⑦F的最高能级的电子云轮廓图: ⑧使用铁触媒能加快合成氨的反应速率实验事实能用勒夏特列原理解释⑨氯乙酸、二氯乙酸、三氯乙酸、三氟乙酸的酸性依次增强
⑧使用铁触媒能加快合成氨的反应速率实验事实能用勒夏特列原理解释⑨氯乙酸、二氯乙酸、三氯乙酸、三氟乙酸的酸性依次增强
①充有氖气的霓虹灯管通电时会发出红色光的主要原因是电子由基态向激发态跃迁时吸收除红光以外的光线②
 不符合泡利原理③增大压强,活化分子百分数增大,单位时间内有效碰撞次数增多,化学反应速率加快④
不符合泡利原理③增大压强,活化分子百分数增大,单位时间内有效碰撞次数增多,化学反应速率加快④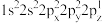 违反了洪特规则,是激发态原子的电子排布⑤钠离子的最高能级为3s⑥25℃时,将
违反了洪特规则,是激发态原子的电子排布⑤钠离子的最高能级为3s⑥25℃时,将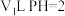 的盐酸与
的盐酸与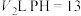 的氢氧化钠溶液混合后
的氢氧化钠溶液混合后 ,则
,则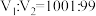 ⑦F的最高能级的电子云轮廓图:
⑦F的最高能级的电子云轮廓图: ⑧使用铁触媒能加快合成氨的反应速率实验事实能用勒夏特列原理解释⑨氯乙酸、二氯乙酸、三氯乙酸、三氟乙酸的酸性依次增强
⑧使用铁触媒能加快合成氨的反应速率实验事实能用勒夏特列原理解释⑨氯乙酸、二氯乙酸、三氯乙酸、三氟乙酸的酸性依次增强| A.①②③⑦ | B.②④⑥⑨ | C.②⑥⑨ | D.①②③⑦⑧ |
您最近半年使用:0次
解题方法
10 . 某化学反应X→Y分两步进行;①X→M;②M→Y。其能量变化如图所示,下列说法错误的是
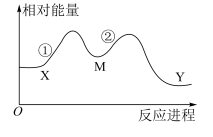

| A.M是该反应的催化剂,可降低该反应的焓变,提高该反应的速率 |
| B.该反应是放热反应 |
| C.X、Y、M三种物质中Y最稳定 |
| D.反应①是总反应的决速步骤 |
您最近半年使用:0次



