名校
1 . 碳达峰是指我国承诺2030年前,二氧化碳的排放不再增长。因此,诸多科学家都在大力研合理利用 和CO以减少碳的排放。
和CO以减少碳的排放。
(1) 可通过以下4种方式转化成有机物,从而有效实现碳循环。
可通过以下4种方式转化成有机物,从而有效实现碳循环。
a.
b.
c.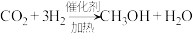
已知: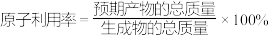
以上反应中,最环保节能的是_______ ,原子利用率最高的是_______ 。(填编号)
(2)我国科学家设计出一条仅11步的工业合成路线,实现了 到淀粉的合成。其第一步是把
到淀粉的合成。其第一步是把 还原为甲醇(
还原为甲醇( ),该方法的化学方程式是:
),该方法的化学方程式是:
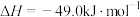 。回答下列问题:
。回答下列问题:
①能说明该反应已达平衡状态的是_______ (填字母)。
A.单位时间内生成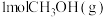 的同时消耗了
的同时消耗了
B.在恒温恒容的容器中,混合气体的平均摩尔质量保持不变
C.在绝热恒容的容器中,反应的平衡常数不再变化
D.在恒温恒压的容器中,混合气体的密度不再变化
②该反应正逆反应的活化能大小为:Ea(正)_______ Ea(逆)(填“>”、“=”或“<”)
(3)利用CO高温时与磷石膏(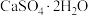 )反应,可减少CO的排放,又可以实现硫酸盐资源的再利用。已知该反应的产物与温度有关。
)反应,可减少CO的排放,又可以实现硫酸盐资源的再利用。已知该反应的产物与温度有关。
①在700℃时,主要的还原产物是一种硫的最低价盐,该物质为_______ (填化学式)。
②在1150℃时,向盛有足量 的真空恒容密闭容器中充入一定量CO,反应体系起始压强为
的真空恒容密闭容器中充入一定量CO,反应体系起始压强为 ,主要发生反应:
,主要发生反应: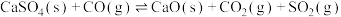 。该反应达到平衡时,
。该反应达到平衡时,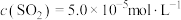 ,CO的转化率为50%,则初始时
,CO的转化率为50%,则初始时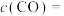
_______ mol/L,该反应的压强平衡常数
_______ MPa(忽略副反应;气体分压=总压×气体物质的量分数)。
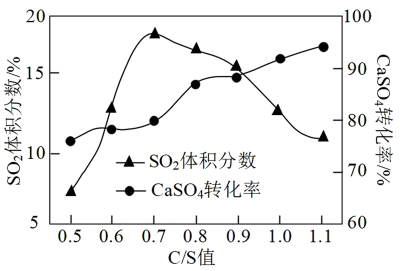
(4)工业上也可用炭粉还原磷石膏,该反应的产物与C/S值(炭粉与 的物质的量之比)有关。向密闭容器中加入几组不同C/S值的炭粉与磷石膏的混合物,1100℃煅烧至无气体产生,结果如图所示。当C/S值为0.5时,反应产物主要为CaO、
的物质的量之比)有关。向密闭容器中加入几组不同C/S值的炭粉与磷石膏的混合物,1100℃煅烧至无气体产生,结果如图所示。当C/S值为0.5时,反应产物主要为CaO、 和
和 ;当C/S值大于0.7时,反应所得气体中
;当C/S值大于0.7时,反应所得气体中 的体积分数下降,可能的原因是
的体积分数下降,可能的原因是_______ 。
 和CO以减少碳的排放。
和CO以减少碳的排放。(1)
 可通过以下4种方式转化成有机物,从而有效实现碳循环。
可通过以下4种方式转化成有机物,从而有效实现碳循环。a.

b.

c.
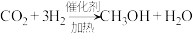
已知:
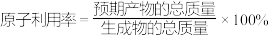
以上反应中,最环保节能的是
(2)我国科学家设计出一条仅11步的工业合成路线,实现了
 到淀粉的合成。其第一步是把
到淀粉的合成。其第一步是把 还原为甲醇(
还原为甲醇( ),该方法的化学方程式是:
),该方法的化学方程式是:
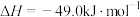 。回答下列问题:
。回答下列问题:①能说明该反应已达平衡状态的是
A.单位时间内生成
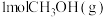 的同时消耗了
的同时消耗了
B.在恒温恒容的容器中,混合气体的平均摩尔质量保持不变
C.在绝热恒容的容器中,反应的平衡常数不再变化
D.在恒温恒压的容器中,混合气体的密度不再变化
②该反应正逆反应的活化能大小为:Ea(正)
(3)利用CO高温时与磷石膏(
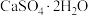 )反应,可减少CO的排放,又可以实现硫酸盐资源的再利用。已知该反应的产物与温度有关。
)反应,可减少CO的排放,又可以实现硫酸盐资源的再利用。已知该反应的产物与温度有关。①在700℃时,主要的还原产物是一种硫的最低价盐,该物质为
②在1150℃时,向盛有足量
 的真空恒容密闭容器中充入一定量CO,反应体系起始压强为
的真空恒容密闭容器中充入一定量CO,反应体系起始压强为 ,主要发生反应:
,主要发生反应: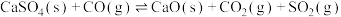 。该反应达到平衡时,
。该反应达到平衡时,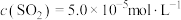 ,CO的转化率为50%,则初始时
,CO的转化率为50%,则初始时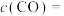

(4)工业上也可用炭粉还原磷石膏,该反应的产物与C/S值(炭粉与
 的物质的量之比)有关。向密闭容器中加入几组不同C/S值的炭粉与磷石膏的混合物,1100℃煅烧至无气体产生,结果如图所示。当C/S值为0.5时,反应产物主要为CaO、
的物质的量之比)有关。向密闭容器中加入几组不同C/S值的炭粉与磷石膏的混合物,1100℃煅烧至无气体产生,结果如图所示。当C/S值为0.5时,反应产物主要为CaO、 和
和 ;当C/S值大于0.7时,反应所得气体中
;当C/S值大于0.7时,反应所得气体中 的体积分数下降,可能的原因是
的体积分数下降,可能的原因是
您最近一年使用:0次
2022-09-21更新
|
142次组卷
|
2卷引用:四川省蓬溪中学校2023-2024学年高二上学期开学考试化学试题
名校
解题方法
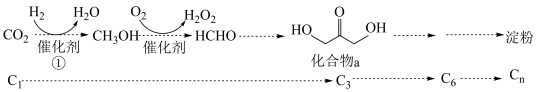
2 . 2021年我国科学家以 为原料人工合成淀粉,其效率约为传统农业生产淀粉的8.5倍,其部分合成路线如图所示,下列有关说法正确的是
为原料人工合成淀粉,其效率约为传统农业生产淀粉的8.5倍,其部分合成路线如图所示,下列有关说法正确的是
①
②
③
④
 为原料人工合成淀粉,其效率约为传统农业生产淀粉的8.5倍,其部分合成路线如图所示,下列有关说法正确的是
为原料人工合成淀粉,其效率约为传统农业生产淀粉的8.5倍,其部分合成路线如图所示,下列有关说法正确的是
①

②

③

④

| A.第①步反应断裂了非极性键与极性键 |
| B.催化剂降低了反应的活化能,改变了反应的焓变,降低了合成淀粉的难度 |
C. |
| D.反应④是吸热反应,活化能较大,所以是决速步 |
您最近一年使用:0次
3 . 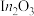 上
上 加氢制甲醇的某种反应路线如图,下列说法错误的是
加氢制甲醇的某种反应路线如图,下列说法错误的是
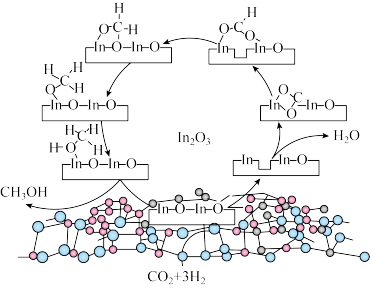
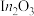 上
上 加氢制甲醇的某种反应路线如图,下列说法错误的是
加氢制甲醇的某种反应路线如图,下列说法错误的是
A.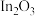 降低了总反应的活化能 降低了总反应的活化能 |
| B.该路线有非极性键的断裂和形成 |
| C.该合成路线符合绿色化学理念 |
| D.甲醇与水分子能形成分子间氢键 |
您最近一年使用:0次
4 . 三甲胺(N (CH3)3)是重要的化工原料,最近我国科学家发明了使用铜催化剂将 二甲基甲酰胺 [N(CH3)2CHO,简称为
二甲基甲酰胺 [N(CH3)2CHO,简称为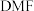 ]转化为三甲胺的合成路线,单一
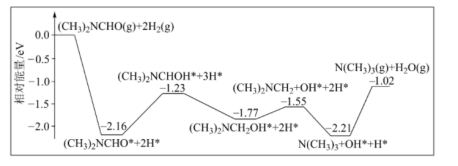
]转化为三甲胺的合成路线,单一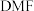 分子在铜催化剂表面的反应历程如图所示,(*表示物质吸附在铜催化剂上)下列说法正确的是
分子在铜催化剂表面的反应历程如图所示,(*表示物质吸附在铜催化剂上)下列说法正确的是
 二甲基甲酰胺 [N(CH3)2CHO,简称为
二甲基甲酰胺 [N(CH3)2CHO,简称为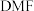 ]转化为三甲胺的合成路线,单一
]转化为三甲胺的合成路线,单一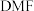 分子在铜催化剂表面的反应历程如图所示,(*表示物质吸附在铜催化剂上)下列说法正确的是
分子在铜催化剂表面的反应历程如图所示,(*表示物质吸附在铜催化剂上)下列说法正确的是 
| A.该历程中决速步骤为: (CH3)2NCH2OH*=(CH3)2NCH2+OH* |
B.该反应的原子利用率为 ,该历程中的最大能垒(活化能)为2.16eV ,该历程中的最大能垒(活化能)为2.16eV |
| C.升高温度可以加快反应速率,并提高DMF的平衡转化率 |
D.若 完全转化为三甲胺,则会释放出1.02eV·NA的能量 完全转化为三甲胺,则会释放出1.02eV·NA的能量 |
您最近一年使用:0次
2021-11-06更新
|
632次组卷
|
5卷引用:专题13 反应微观机理分析-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)
(已下线)专题13 反应微观机理分析-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)黑龙江省八校2022届高三上学期期中联合考试化学试题(已下线)押新高考卷11题 反应机理分析-备战2022年高考化学临考题号押题(新高考通版)山东省枣庄滕州市2022-2023学年高三上学期期中考试化学试题山东省滕州市第二中学2022-2023学年高三上学期11月定时检测化学试题
名校
解题方法
5 . 研究发现,以CO2和NH3为原料合成尿素的反应2NH3(g)+CO2(g) CO(NH2)2(s)+H2O(g) ΔH分两步完成,其能量变化如图所示:
CO(NH2)2(s)+H2O(g) ΔH分两步完成,其能量变化如图所示:
第一步:2NH3(g)+CO2(g) NH2COONH4(s) ΔH1
NH2COONH4(s) ΔH1
第二步:NH2COONH4(s) CO(NH2)2(s)+H2O(g) ΔH2
CO(NH2)2(s)+H2O(g) ΔH2
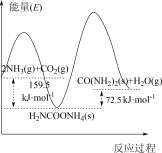
(1)合成尿素的决速反应是_____ (填“第一步”或“第二步”)反应,理由是_____ 。
(2)已知合成尿素2NH3(g)+CO2(g) CO(NH2)2(s)+H2O(g) ΔH的活化能Ea(逆)为194kJ∙mol-1,该反应在
CO(NH2)2(s)+H2O(g) ΔH的活化能Ea(逆)为194kJ∙mol-1,该反应在_____ (填“高温”、“低温”或“任意温度”)下可自发进行。
(3)对于2SO2(g)+O2(g) 2SO3(g) ΔH=-196.6kJ∙mol-1,在T℃时,K=0.5;向1L的三个密闭容器中,按不同方式投入相应的物质,保持容器容积不变,测得反应达到平衡时的有关数据如下:
2SO3(g) ΔH=-196.6kJ∙mol-1,在T℃时,K=0.5;向1L的三个密闭容器中,按不同方式投入相应的物质,保持容器容积不变,测得反应达到平衡时的有关数据如下:
则 =
=_____ ;
_____  (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
 CO(NH2)2(s)+H2O(g) ΔH分两步完成,其能量变化如图所示:
CO(NH2)2(s)+H2O(g) ΔH分两步完成,其能量变化如图所示:第一步:2NH3(g)+CO2(g)
 NH2COONH4(s) ΔH1
NH2COONH4(s) ΔH1第二步:NH2COONH4(s)
 CO(NH2)2(s)+H2O(g) ΔH2
CO(NH2)2(s)+H2O(g) ΔH2
(1)合成尿素的决速反应是
(2)已知合成尿素2NH3(g)+CO2(g)
 CO(NH2)2(s)+H2O(g) ΔH的活化能Ea(逆)为194kJ∙mol-1,该反应在
CO(NH2)2(s)+H2O(g) ΔH的活化能Ea(逆)为194kJ∙mol-1,该反应在(3)对于2SO2(g)+O2(g)
 2SO3(g) ΔH=-196.6kJ∙mol-1,在T℃时,K=0.5;向1L的三个密闭容器中,按不同方式投入相应的物质,保持容器容积不变,测得反应达到平衡时的有关数据如下:
2SO3(g) ΔH=-196.6kJ∙mol-1,在T℃时,K=0.5;向1L的三个密闭容器中,按不同方式投入相应的物质,保持容器容积不变,测得反应达到平衡时的有关数据如下:| 容器 | A | B | C | |
| 物质投入量 | 2molSO2和1molO2 | 2molSO3 | 1.6molSO20.8molO2和0.4molSO3 | |
| 平衡时数据 | 反应能量变化的绝对值(kJ) |  |  |  |
| 反应物转化率 |  |  |  | |
 =
=
 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
您最近一年使用:0次
解题方法
6 . 一定温度下, 的氯化、溴化过程中决速步反应能量图及一段时间后产物的选择性如图所示,下列叙述
的氯化、溴化过程中决速步反应能量图及一段时间后产物的选择性如图所示,下列叙述不正确 的是
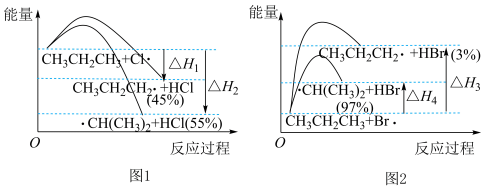
 的氯化、溴化过程中决速步反应能量图及一段时间后产物的选择性如图所示,下列叙述
的氯化、溴化过程中决速步反应能量图及一段时间后产物的选择性如图所示,下列叙述
A. |
| B.升高温度,体系中n(1-氯丙烷)与n(2-氯丙烷)的比值增大 |
C.在该温度下,丙烷与体积比1:1的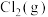 和 和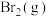 的混合气体反应,产物中2-溴丙烷含量最高 的混合气体反应,产物中2-溴丙烷含量最高 |
| D.以丙烷为原料合成丙醇时,“先溴代再水解”有利于提高2-丙醇的含量 |
您最近一年使用:0次
名校
7 . 工业上以CO2和NH3为原料合成尿素,下图是反应历程及相对能量变化,历程中的所有物质均为气态。下列说法正确的是
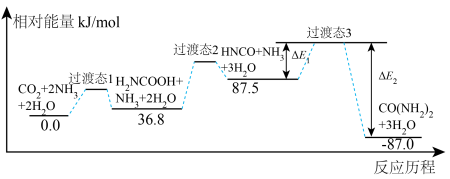

| A.反应中氨气被氧化 |
| B.若ΔE1=66kJ/mol,则△E2=240.5kJ/mol |
| C.该反应的速率控制步骤对应的反应热是△H=+36.8kJ/mol |
| D.历程中,N 原子杂化方式不变 |
您最近一年使用:0次
名校
8 . 氨是重要的化工原料,我国目前氨的生产能力位居世界首位。回答下列问题:
(1)二十世纪初,工业卜以CO2和NH3为原料在一定温度和压强下合成尿素。反应分两步:a.CO2和NH3生成NH2COONH4;b.NH2COONH4分解生成尿素,结合反应过程中能量变化示意图(如图),回答问题:

①活化能:反应a___________ 反应b(填“>”、“<”或“=”)。
②反应a为___________ 反应(填“放热”或“吸热”)。
③ △H=
△H=___________ kJ/mol(用含“E1、E2、E3、E4”的代数式表示)。
(2)研究表明,合成氨反应在Fe催化剂上可能通过下图机理进行(*表示催化剂表面吸附位,N2*表示被吸附于催化剂表面的N2),其中N2的吸附分解反应活化能高,速率慢,是合成氨反应的决速步,实际生产中,N2和H2的物质的量之比并非1:3,而是1:2.8,分析说明原料气中N2适度过量的2个理由:

①___________ 、②___________ 。
(3)若在不同压强下,以投料比n(N2):n(H2)=1:3的方式进料,反应达平衡时氨的摩尔分数与温度的计算结果如图所示:(物质i的摩尔分数: )
)

①图中压强由小到大的顺序为___________ ,判断依据是___________ 。
②图3中,当P2=20MPa、x(NH3)=0.20时,氮气的转化率ɑ=___________ %(保留到小数点后一位);该温度时,反应 的平衡常数Kp=
的平衡常数Kp=___________ (MPa)-2(化为最简式,Kp为以平衡分压代替平衡浓度表示的平衡常数,分压=总压×摩尔分数)。
(1)二十世纪初,工业卜以CO2和NH3为原料在一定温度和压强下合成尿素。反应分两步:a.CO2和NH3生成NH2COONH4;b.NH2COONH4分解生成尿素,结合反应过程中能量变化示意图(如图),回答问题:

①活化能:反应a
②反应a为
③
 △H=
△H=(2)研究表明,合成氨反应在Fe催化剂上可能通过下图机理进行(*表示催化剂表面吸附位,N2*表示被吸附于催化剂表面的N2),其中N2的吸附分解反应活化能高,速率慢,是合成氨反应的决速步,实际生产中,N2和H2的物质的量之比并非1:3,而是1:2.8,分析说明原料气中N2适度过量的2个理由:

①
(3)若在不同压强下,以投料比n(N2):n(H2)=1:3的方式进料,反应达平衡时氨的摩尔分数与温度的计算结果如图所示:(物质i的摩尔分数:
 )
)
①图中压强由小到大的顺序为
②图3中,当P2=20MPa、x(NH3)=0.20时,氮气的转化率ɑ=
 的平衡常数Kp=
的平衡常数Kp=
您最近一年使用:0次
2024-01-09更新
|
132次组卷
|
2卷引用:广东省东莞市东莞中学2023-2024学年高二上学期期中考试化学试题
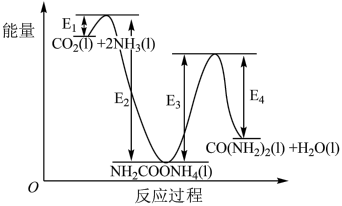
9 . 尿素[CO(NH2)2]合成的发展体现了化学科学与技术的不断进步。回答下列问题:
(1)十九世纪初,用氰酸银(AgOCN)与 在一定条件下反应制得
在一定条件下反应制得 ,实现了由无机物到有机物的合成。该反应的化学方程式是
,实现了由无机物到有机物的合成。该反应的化学方程式是___________ 。
(2)二十世纪初,工业以 和
和 为原料,在一定温度和压强下合成尿素。反应分两步进行,反应过程能量变化如图。总反应
为原料,在一定温度和压强下合成尿素。反应分两步进行,反应过程能量变化如图。总反应

___________ (用 、
、 、
、 、
、 表示);快反应的化学方程式为
表示);快反应的化学方程式为___________ 。
(3)研究发现,电催化 和含氮物质(
和含氮物质( 等)在常温常压下合成尿素,有助于实现碳中和及解决含氮废水污染问题,电解原理如图所示。b是电源的
等)在常温常压下合成尿素,有助于实现碳中和及解决含氮废水污染问题,电解原理如图所示。b是电源的___________ 极;生成尿素的电极反应为___________ ,若生成 ,经过质子交换膜的
,经过质子交换膜的 的物质的量为
的物质的量为___________ mol。

(4)尿素样品含氮量的测定方法如下。已知:溶液中 不能直接用NaOH溶液准确滴定。
不能直接用NaOH溶液准确滴定。

①“消化液”中的含氮粒子是___________ 。
②步骤iv中标准NaOH溶液的浓度和消耗的体积分别为c和V,计算样品含氮量还需要的实验数据有___________ 。

(1)十九世纪初,用氰酸银(AgOCN)与
 在一定条件下反应制得
在一定条件下反应制得 ,实现了由无机物到有机物的合成。该反应的化学方程式是
,实现了由无机物到有机物的合成。该反应的化学方程式是(2)二十世纪初,工业以
 和
和 为原料,在一定温度和压强下合成尿素。反应分两步进行,反应过程能量变化如图。总反应
为原料,在一定温度和压强下合成尿素。反应分两步进行,反应过程能量变化如图。总反应

 、
、 、
、 、
、 表示);快反应的化学方程式为
表示);快反应的化学方程式为(3)研究发现,电催化
 和含氮物质(
和含氮物质( 等)在常温常压下合成尿素,有助于实现碳中和及解决含氮废水污染问题,电解原理如图所示。b是电源的
等)在常温常压下合成尿素,有助于实现碳中和及解决含氮废水污染问题,电解原理如图所示。b是电源的 ,经过质子交换膜的
,经过质子交换膜的 的物质的量为
的物质的量为
(4)尿素样品含氮量的测定方法如下。已知:溶液中
 不能直接用NaOH溶液准确滴定。
不能直接用NaOH溶液准确滴定。
①“消化液”中的含氮粒子是
②步骤iv中标准NaOH溶液的浓度和消耗的体积分别为c和V,计算样品含氮量还需要的实验数据有
您最近一年使用:0次
名校
10 . 合成气(CO和H2)是目前化工常用的原料,下面是用甲烷制备合成气的两种方法:
①CH4(g)+H2O(g) CO(g)+3H2(g) ΔH1=+216 kJ·mol-1;
CO(g)+3H2(g) ΔH1=+216 kJ·mol-1;
②2CH4(g)+O2(g) 2CO(g)+4H2(g) ΔH2=−72 kJ·mol-1。
2CO(g)+4H2(g) ΔH2=−72 kJ·mol-1。
其中一个反应的反应过程与能量变化关系如图所示。
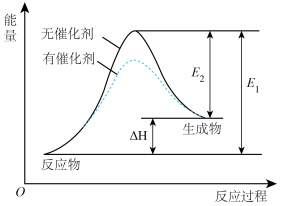
则下列说法正确的是
①CH4(g)+H2O(g)
 CO(g)+3H2(g) ΔH1=+216 kJ·mol-1;
CO(g)+3H2(g) ΔH1=+216 kJ·mol-1;②2CH4(g)+O2(g)
 2CO(g)+4H2(g) ΔH2=−72 kJ·mol-1。
2CO(g)+4H2(g) ΔH2=−72 kJ·mol-1。其中一个反应的反应过程与能量变化关系如图所示。

则下列说法正确的是
| A.E1表示2CH4(g)+O2(g) =2CO(g)+4H2(g)的活化能 |
B.E2表示CH4(g)+H2O(g) CO(g)+3H2(g)的活化能 CO(g)+3H2(g)的活化能 |
| C.该图示为反应①的反应过程与能量变化示意图,该反应为吸热反应 |
| D.一般情况下,加入催化剂,既能降低E1,也能降低E2,也能降低ΔH |
您最近一年使用:0次



