解题方法
1 . 在碳循环中,以 为原料生产尿素的反应历程与能量变化示意图如图所示。
为原料生产尿素的反应历程与能量变化示意图如图所示。
_______ 0(填“>”、“<”或“=”)。从图像分析决定生产尿素的总反应的反应速率的步骤是第_______ 步反应,并说明理由______________ 。
 为原料生产尿素的反应历程与能量变化示意图如图所示。
为原料生产尿素的反应历程与能量变化示意图如图所示。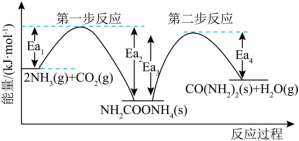

您最近一年使用:0次
2 . 下列说法正确的是
| A.升高温度,速率加快,说明升高温度反应的活化能降低 |
| B.有些反应在磁场下反应速率加快,说明活化分子数增大 |
| C.氢气在氯气中燃烧时,释放的化学能等于产生的热能 |
| D.化学反应的焓变是决定化学反应方向的唯一因素 |
您最近一年使用:0次
解题方法
3 . 碳酸二甲酯(DMC)是一种绿色化学品,具有优良的化学反应性能和广泛的应用前景。回答下列问题:
(1)工业上可采用CO低压气相法合成DMC。已知下列反应的热化学方程式:
①2NO(g)+ O2(g)
O2(g) N2O3(g) K1 △H1=akJ/mol
N2O3(g) K1 △H1=akJ/mol
②2CH3OH(g)+N2O3(g) 2CH3ONO(g)+H2O(g) K2 △H2=bkJ/mol
2CH3ONO(g)+H2O(g) K2 △H2=bkJ/mol
③CO(g)+2CH3ONO(g) (CH3O)2CO(g)+2NO(g) K3 △H=ckJ/mol
(CH3O)2CO(g)+2NO(g) K3 △H=ckJ/mol
合成反应2CH3OH(g)+CO(g)+ O2(g)
O2(g) (CH3O)2CO(g)+H2O(g)的△H=
(CH3O)2CO(g)+H2O(g)的△H=_______ kJ/mol,其平衡常数K=_______ (用K1、K2、K3表示)。
(2)甲醇气相氧化羰基化法合成DMC的总反应为:2CH3OH(g)+CO(g)+ O2(g)
O2(g)  (CH3O)2CO(g)+H2O(g)。在3.2MPa下,将物质的量之比为4∶2∶1的反应物CH3OH、CO、O2混合,按一定流速通过装有催化剂的容器,测得甲醇的转化率、DMC的产率受温度影响的曲线如图所示(该工艺的副产物主要是二甲醚和甲酸甲酯):
(CH3O)2CO(g)+H2O(g)。在3.2MPa下,将物质的量之比为4∶2∶1的反应物CH3OH、CO、O2混合,按一定流速通过装有催化剂的容器,测得甲醇的转化率、DMC的产率受温度影响的曲线如图所示(该工艺的副产物主要是二甲醚和甲酸甲酯):______ 。
②结合上图判断,下列有关该反应的说法正确的是___ (填标号)。
a.压强增大平衡正向移动 b.平衡常数随温度升高而增大
c.温度升高平衡正向移动 d.110~130℃之间,随温度升高副反应增多
③在一定条件下,物质的量之比为4:2:1的反应物CH3OH、CO、O2充分反应达到平衡后,甲醇的转化率为24%,生成DMC的选择性为90%。假设副产物只有二甲醚(2CH3OH→CH3OCH3+H2O),则平衡混合气中DMC与H2O的物质的量之比为_______ ,DMC的体积分数是________ (保留两位有效数字)。
(3)研究表明,在碱式氯化铜催化剂表面上,甲醇氧化羰基化反应的机理为:
(CH3OH)※→CH3O…H…Cl+* ①
CH3O…H…Cl+*→CH3O*+HCl ②
CH3O*+CO→CH3OCO* ③
CH3O*+CH3OCO*→CH3OCOOCH3+** ④
……
※、*代表催化剂活性中心,且*为※失去Cl的活性中心;CH3O*代表活化状态。上述四步反应中第②步速率最小,说明该反应的活化能______ (填“最大”或“最小”),其原因是_________ 。
(1)工业上可采用CO低压气相法合成DMC。已知下列反应的热化学方程式:
①2NO(g)+
 O2(g)
O2(g) N2O3(g) K1 △H1=akJ/mol
N2O3(g) K1 △H1=akJ/mol②2CH3OH(g)+N2O3(g)
 2CH3ONO(g)+H2O(g) K2 △H2=bkJ/mol
2CH3ONO(g)+H2O(g) K2 △H2=bkJ/mol③CO(g)+2CH3ONO(g)
 (CH3O)2CO(g)+2NO(g) K3 △H=ckJ/mol
(CH3O)2CO(g)+2NO(g) K3 △H=ckJ/mol合成反应2CH3OH(g)+CO(g)+
 O2(g)
O2(g) (CH3O)2CO(g)+H2O(g)的△H=
(CH3O)2CO(g)+H2O(g)的△H=(2)甲醇气相氧化羰基化法合成DMC的总反应为:2CH3OH(g)+CO(g)+
 O2(g)
O2(g)  (CH3O)2CO(g)+H2O(g)。在3.2MPa下,将物质的量之比为4∶2∶1的反应物CH3OH、CO、O2混合,按一定流速通过装有催化剂的容器,测得甲醇的转化率、DMC的产率受温度影响的曲线如图所示(该工艺的副产物主要是二甲醚和甲酸甲酯):
(CH3O)2CO(g)+H2O(g)。在3.2MPa下,将物质的量之比为4∶2∶1的反应物CH3OH、CO、O2混合,按一定流速通过装有催化剂的容器,测得甲醇的转化率、DMC的产率受温度影响的曲线如图所示(该工艺的副产物主要是二甲醚和甲酸甲酯):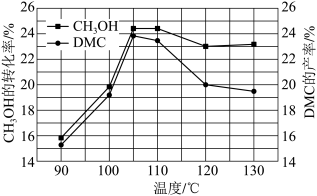
②结合上图判断,下列有关该反应的说法正确的是
a.压强增大平衡正向移动 b.平衡常数随温度升高而增大
c.温度升高平衡正向移动 d.110~130℃之间,随温度升高副反应增多
③在一定条件下,物质的量之比为4:2:1的反应物CH3OH、CO、O2充分反应达到平衡后,甲醇的转化率为24%,生成DMC的选择性为90%。假设副产物只有二甲醚(2CH3OH→CH3OCH3+H2O),则平衡混合气中DMC与H2O的物质的量之比为
(3)研究表明,在碱式氯化铜催化剂表面上,甲醇氧化羰基化反应的机理为:
(CH3OH)※→CH3O…H…Cl+* ①
CH3O…H…Cl+*→CH3O*+HCl ②
CH3O*+CO→CH3OCO* ③
CH3O*+CH3OCO*→CH3OCOOCH3+** ④
……
※、*代表催化剂活性中心,且*为※失去Cl的活性中心;CH3O*代表活化状态。上述四步反应中第②步速率最小,说明该反应的活化能
您最近一年使用:0次
2024-03-12更新
|
64次组卷
|
3卷引用:陕西省安康市高新中学2023-2024学年高三12月月考理科综合试题
陕西省安康市高新中学2023-2024学年高三12月月考理科综合试题陕西省安康市高新中学2023-2024学年高三上学期12月月考理科综合试题(已下线)提升练09 化学反应原理综合-【查漏补缺】2024年高考化学复习冲刺过关(新高考专用)
4 . 18O标记的乙酸甲酯在足量NaOH溶液中发生水解,部分反应历程可表示为如下所示:
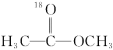 +OH-
+OH-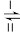
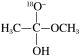
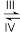
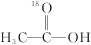 +CH3O-
+CH3O-
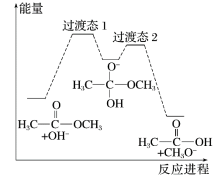
已知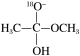

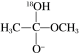 为快速平衡,下列说法正确的是
为快速平衡,下列说法正确的是
| A.反应Ⅱ、Ⅲ为决速步 |
| B.反应结束后,溶液中存在18OH- |
| C.反应结束后,溶液中存在CH318OH |
| D.反应Ⅰ与反应Ⅳ活化能的差值等于图示总反应的焓变 |
您最近一年使用:0次
名校
解题方法
5 .  催化剂光助一芬顿反应用于漂白有机染料的一种机理如图所示,其中包括①②光激发产生光电子与光生空穴(
催化剂光助一芬顿反应用于漂白有机染料的一种机理如图所示,其中包括①②光激发产生光电子与光生空穴( ,具有很强的得电子能力)、③④空穴氧化、⑥超氧自由基氧化、⑦光生电子还原铁离子等。下列说法正确的是
,具有很强的得电子能力)、③④空穴氧化、⑥超氧自由基氧化、⑦光生电子还原铁离子等。下列说法正确的是

 催化剂光助一芬顿反应用于漂白有机染料的一种机理如图所示,其中包括①②光激发产生光电子与光生空穴(
催化剂光助一芬顿反应用于漂白有机染料的一种机理如图所示,其中包括①②光激发产生光电子与光生空穴( ,具有很强的得电子能力)、③④空穴氧化、⑥超氧自由基氧化、⑦光生电子还原铁离子等。下列说法正确的是
,具有很强的得电子能力)、③④空穴氧化、⑥超氧自由基氧化、⑦光生电子还原铁离子等。下列说法正确的是
A.反应⑤每消耗1mol  ,共转移4mol ,共转移4mol  |
| B.反应⑨中双氧水将颜料直接氧化成无色物质 |
C.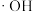 、 、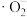 和 和 在漂白颜料时体现了强还原性 在漂白颜料时体现了强还原性 |
| D.催化剂可以降低反应活化能,提高单位体积内活化分子百分数 |
您最近一年使用:0次
2024-02-26更新
|
209次组卷
|
2卷引用:江西省五市九校协作体2023-2024学年高三上学期第一次联考化学试题
名校
解题方法
6 . 金属Ni可活化C2H6放出CH4,其反应历程如图所示:

下列说法正确的是

下列说法正确的是
| A.中间体1→中间体2的过程决定整个历程的反应速率 |
| B.加入催化剂可降低反应的活化能,加快反应速率 |
| C.整个历程中有碳碳键的断裂与形成 |
| D.中间体2→中间体3的过程是放热过程 |
您最近一年使用:0次
解题方法
7 . 以甲烷与 为原料合成“合成气”,对实现碳中和、碳达峰及生态环境保护有着重要意义。其反应历程分两步:反应①
为原料合成“合成气”,对实现碳中和、碳达峰及生态环境保护有着重要意义。其反应历程分两步:反应①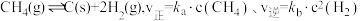 ;反应②
;反应②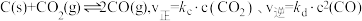 ,反应中的
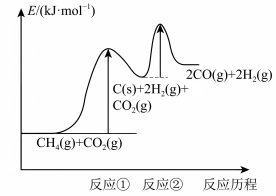
,反应中的 为纳米碳,反应历程的能量变化如图所示,下列说法错误的是
为纳米碳,反应历程的能量变化如图所示,下列说法错误的是
 为原料合成“合成气”,对实现碳中和、碳达峰及生态环境保护有着重要意义。其反应历程分两步:反应①
为原料合成“合成气”,对实现碳中和、碳达峰及生态环境保护有着重要意义。其反应历程分两步:反应①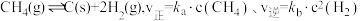 ;反应②
;反应②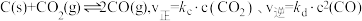 ,反应中的
,反应中的 为纳米碳,反应历程的能量变化如图所示,下列说法错误的是
为纳米碳,反应历程的能量变化如图所示,下列说法错误的是
| A.升高温度,反应①与反应②的反应速率及平衡转化率均升高 |
| B.整个反应的速率由反应①决定,两步反应均为吸热反应 |
| C.反应①的活化能比反应②的大,二者之和为总反应的活化能 |
D.反应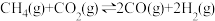 的平衡常数 的平衡常数 |
您最近一年使用:0次
名校
8 . 反应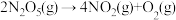 经历如下历程:
经历如下历程:
第一步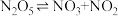 ,快速平衡;
,快速平衡;
第二步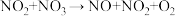 ,慢反应;
,慢反应;
第三步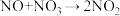 ,快反应。
,快反应。
其中可近似认为第二步反应不影响第一步的平衡。下列表述正确的是
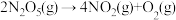 经历如下历程:
经历如下历程:第一步
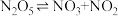 ,快速平衡;
,快速平衡;第二步
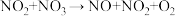 ,慢反应;
,慢反应;第三步
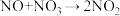 ,快反应。
,快反应。其中可近似认为第二步反应不影响第一步的平衡。下列表述正确的是
A. 此时第一步反应处于平衡状态 此时第一步反应处于平衡状态 | B.反应的中间产物只有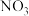 |
C.第二步中 与 与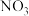 的碰撞仅部分有效 的碰撞仅部分有效 | D.第三步反应的活化能较高 |
您最近一年使用:0次
名校
解题方法
9 . 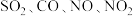 均会对环境造成污染,如何高效消除它们造成的污染是科技工作者研究的重要内容。回答下列问题:
均会对环境造成污染,如何高效消除它们造成的污染是科技工作者研究的重要内容。回答下列问题:
(1)一定条件下, 可以将
可以将 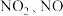 转化为
转化为  ,涉及反应如下:
,涉及反应如下:
ⅰ.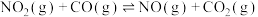
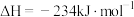 ;
;
ⅱ. ;
;
ⅲ.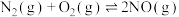
 。
。
①CO的燃烧热
___________ 。
②已知反应ⅰ是二级反应,第一步为 ;第二步为
;第二步为 ,已知
,已知  的浓度变化对反应 ⅰ速率几乎无影响,则这两步反应,活化能较大的是第
的浓度变化对反应 ⅰ速率几乎无影响,则这两步反应,活化能较大的是第___________ 步。
(2)测得反应ⅱ的 为速率常数,只与温度有关)。已知某温度下反应 ⅱ的平衡常数
为速率常数,只与温度有关)。已知某温度下反应 ⅱ的平衡常数  ,则该温度下
,则该温度下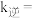
___________ ,达到平衡后,仅升高温度,若  增大20倍,则
增大20倍,则  增大的倍数
增大的倍数___________ (填“>”“<”或“=”)20。
(3)一定条件下, 也可以将
也可以将  转化为
转化为  ,反应原理为
,反应原理为 ,在恒压(4MPa)密闭容器中加入足量的活性炭和
,在恒压(4MPa)密闭容器中加入足量的活性炭和  气体,分别在Ⅰ、Ⅱ、Ⅲ三种不同催化剂催化下使其发生反应,测得经过相同时间时
气体,分别在Ⅰ、Ⅱ、Ⅲ三种不同催化剂催化下使其发生反应,测得经过相同时间时  的转化率
的转化率  随温度的变化如图所示:
随温度的变化如图所示:
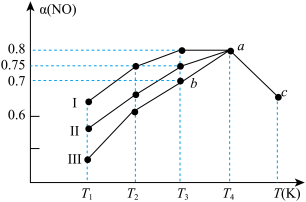
①催化效果最好的催化剂是___________ , 点
点
___________ 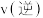 。
。
②已知:分压=总压×物质的量分数。若 反应达到平衡状态用时
反应达到平衡状态用时  ,则v(NO)=
,则v(NO)=________ MPa/min,Kp=____________ 。
(4)电化学法消除 污染的同时可获得电能,其工作原理图如图所示,负极上发生的电极反应式为
污染的同时可获得电能,其工作原理图如图所示,负极上发生的电极反应式为___________ 。

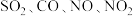 均会对环境造成污染,如何高效消除它们造成的污染是科技工作者研究的重要内容。回答下列问题:
均会对环境造成污染,如何高效消除它们造成的污染是科技工作者研究的重要内容。回答下列问题:(1)一定条件下,
 可以将
可以将 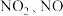 转化为
转化为  ,涉及反应如下:
,涉及反应如下:ⅰ.
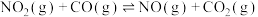
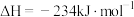 ;
;ⅱ.
 ;
;ⅲ.
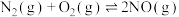
 。
。①CO的燃烧热

②已知反应ⅰ是二级反应,第一步为
 ;第二步为
;第二步为 ,已知
,已知  的浓度变化对反应 ⅰ速率几乎无影响,则这两步反应,活化能较大的是第
的浓度变化对反应 ⅰ速率几乎无影响,则这两步反应,活化能较大的是第(2)测得反应ⅱ的
 为速率常数,只与温度有关)。已知某温度下反应 ⅱ的平衡常数
为速率常数,只与温度有关)。已知某温度下反应 ⅱ的平衡常数  ,则该温度下
,则该温度下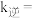
 增大20倍,则
增大20倍,则  增大的倍数
增大的倍数(3)一定条件下,
 也可以将
也可以将  转化为
转化为  ,反应原理为
,反应原理为 ,在恒压(4MPa)密闭容器中加入足量的活性炭和
,在恒压(4MPa)密闭容器中加入足量的活性炭和  气体,分别在Ⅰ、Ⅱ、Ⅲ三种不同催化剂催化下使其发生反应,测得经过相同时间时
气体,分别在Ⅰ、Ⅱ、Ⅲ三种不同催化剂催化下使其发生反应,测得经过相同时间时  的转化率
的转化率  随温度的变化如图所示:
随温度的变化如图所示:
①催化效果最好的催化剂是
 点
点
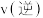 。
。②已知:分压=总压×物质的量分数。若
 反应达到平衡状态用时
反应达到平衡状态用时  ,则v(NO)=
,则v(NO)=(4)电化学法消除
 污染的同时可获得电能,其工作原理图如图所示,负极上发生的电极反应式为
污染的同时可获得电能,其工作原理图如图所示,负极上发生的电极反应式为
您最近一年使用:0次
名校
10 . 某次研究性学习活动中,实验小组用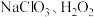 和稀硫酸制备
和稀硫酸制备 ,反应较慢。若反应开始时加入少量盐酸,
,反应较慢。若反应开始时加入少量盐酸, 的生成速率大大提高,且不含
的生成速率大大提高,且不含 ,可能的反应历程示意图如下。
,可能的反应历程示意图如下。

下列有关分析或评价不正确的是
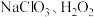 和稀硫酸制备
和稀硫酸制备 ,反应较慢。若反应开始时加入少量盐酸,
,反应较慢。若反应开始时加入少量盐酸, 的生成速率大大提高,且不含
的生成速率大大提高,且不含 ,可能的反应历程示意图如下。
,可能的反应历程示意图如下。
下列有关分析或评价不正确的是
| A.a等于37 | B. 的空间结构为平面三角形 的空间结构为平面三角形 |
C. 为总反应的催化剂 为总反应的催化剂 | D.活化能:反应I大于反应II |
您最近一年使用:0次
2024-01-29更新
|
390次组卷
|
3卷引用: 河南省洛阳市孟津区第一高级中学2023-2024学年高三上学期12月月考化学试题
河南省洛阳市孟津区第一高级中学2023-2024学年高三上学期12月月考化学试题河南省新乡市第一中学2023-2024学年高三上学期12月月考化学试题(已下线)题型10 反应微观机理分析 速率方程及其应用-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)



