名校
解题方法
1 . 对于可逆反应3H2+N2⇌2NH3,下列措施能使反应物中活化分子百分数、化学反应速率和化学平衡常数都变化的是
| A.增大压强 | B.充入更多N2 | C.使用高效催化剂 | D.降低温度 |
您最近一年使用:0次
2023-12-28更新
|
69次组卷
|
34卷引用:2015-2016学年湖北航天高中、安陆二中等五校高二上期中化学试卷
2015-2016学年湖北航天高中、安陆二中等五校高二上期中化学试卷2016-2017学年黑龙江牡丹江高级中学高二9月月考化学卷22016-2017学年河北省冀州中学高二上期中化学卷2016-2017学年黑龙江省哈尔滨市第六中学高二3月月考化学试卷河北省张家口市第一中学2016-2017学年高一(衔接班)6月月考(理)化学试题湖北省天门、仙桃、潜江三市2016-2017学年高一下学期期末考试化学试题辽宁省本溪市第一中学2017-2018学年高二上学期第一次月考化学试题西藏日喀则市第二高级中学2017-2018学年高二上学期期中考试化学试题甘肃省白银市会宁县第二中学2017-2018学年高二上学期期中考试理科化学试题河南省安阳市林州市第一中学2019-2020学年高二下学期4月月考化学试题宁夏银川市宁夏大学附属中学2019-2020学年高二线上线下教学衔接摸底暨期中考试化学试题内蒙古自治区呼和浩特市内蒙古师范大学附属中学2019-2020学年高二上学期期中考试化学试题(已下线)2.1.2 活化能(练习)-2020-2021学年上学期高二化学同步精品课堂(新教材人教版选择性必修1)河南省洛阳市孟津县第二高级中学2020-2021学年高二上学期9月月考化学试题黑龙江省大庆市东风中学2020-2021学年高二上学期10月月考化学试题天津市滨海新区汉沽第六中学2020-2021学年高二上学期期中化学试题黑龙江省嫩江市高级中学2020-2021学年高二上学期9月月考化学试题天津市和平区2017-2018学年高二上学期期中质量调查化学试题河南省原阳县2020-2021学年高二上学期期末考试化学试题湖北省武汉市江夏实验高级中学2021-2022学年高二上学期10月考试化学试题(已下线)2.3.2 影响化学反应速率因素的微观分析-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修1)黑龙江省牡丹江市第一中学2022-2023学年高二10月月考化学试题吉林省长春市部分高中2022-2023学年高二上学期10月月考化学试题(已下线)第2章能力提升测评卷-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修第一册)河南省南乐县第一高级中学2021-2022学年高二上学期9月半月考化学试题新疆喀什第二中学2022-2023学年高二上学期期中考试化学试题山东省济南市天桥区黄河双语实验学校2021-2022学年高二上学期10月月考化学试题(已下线)【2022】【高二上】【期中考】【高中化学】60(已下线)【2022】【高二化学】【期中考】-179河南省商丘市宁陵县高级中学2023-2024学年高二上学期第一次考试化学试题第二章 第一节 化学反应速率 第2课时 影响化学反应速率的因素 活化能新疆生产建设兵团第二师八一中学2023-2024学年高二上学期第一次月考化学试题陕西省西安市 周至县第四中学2023-2024学年高二上学期10月份月考化学试题安徽省芜湖市第一中学2022-2023学年高二上学期10月月考化学试卷
名校
2 . 下列说法不正确的是
| A.在其他外界条件不变的情况下,增大压强,不能增大活化分子的百分数 |
B.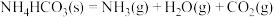 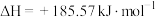 能自发进行,原因是体系有自发地向混乱度增加的方向转变的倾向 能自发进行,原因是体系有自发地向混乱度增加的方向转变的倾向 |
| C.焓变和熵变都与反应的自发性有关,因此焓变或熵变均可以单独作为反应自发性的判据 |
D. 、 、 的反应在任何温度下都能自发进行 的反应在任何温度下都能自发进行 |
您最近一年使用:0次
2023-07-18更新
|
147次组卷
|
5卷引用:2015-2016学年浙江省海宁市三校高二下学期期中化学试卷
2015-2016学年浙江省海宁市三校高二下学期期中化学试卷(已下线)2018-2019学年同步单元双基双测AB卷:第二单元化学反应速率与化学平衡单元测试B卷河北省唐山市第一中学2018-2019学年高二上学期10月月考化学试题上海市上海中学2022-2023学年高一下学期期末考试化学试题(已下线)专题04 化学反应的速率与工业合成氨-【好题汇编】备战2023-2024学年高二化学上学期期末真题分类汇编(上海专用)
解题方法
3 . 2019年9月,我国科研人员研制出Ti・H・Fe双温区催化剂,其中Ti-H区域和Fe区域的温度差可超过100℃。Ti-H-Fe双温区催化合成氨的反应历程如图所示,其中吸附在催化剂表面上的物种用*标注。下列说法错误的是
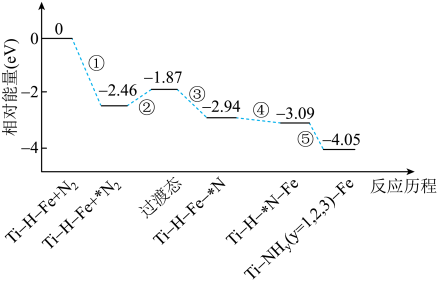

| A.①②③在Fe区域发生,④⑤在Ti-H区域发生 |
| B.在高温区加快了反应速率,低温区提高了氨的产率 |
| C.该历程中能量变化最大的是2.46eV,是氮分子中氮氮三键的断裂过程 |
| D.使用Ti-H-Fe双温区催化合成氨,不会改变合成氨反应的反应热 |
您最近一年使用:0次
名校
解题方法
4 . 金属插入 的
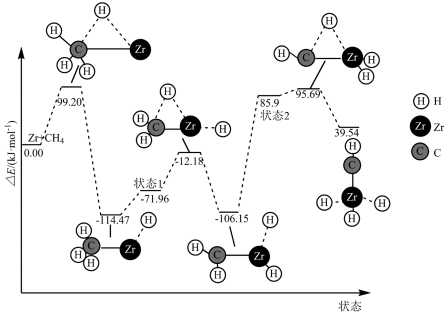
的 键形成高氧化态过渡金属化合物的反应频繁出现在光分解作用、金属有机化学等领域,如图所示是
键形成高氧化态过渡金属化合物的反应频繁出现在光分解作用、金属有机化学等领域,如图所示是 与
与 形成过渡金属化合物的过程。下列说法错误的是
形成过渡金属化合物的过程。下列说法错误的是
 的
的 键形成高氧化态过渡金属化合物的反应频繁出现在光分解作用、金属有机化学等领域,如图所示是
键形成高氧化态过渡金属化合物的反应频繁出现在光分解作用、金属有机化学等领域,如图所示是 与
与 形成过渡金属化合物的过程。下列说法错误的是
形成过渡金属化合物的过程。下列说法错误的是
A.整个反应快慢,由 状态2反应决定 状态2反应决定 |
B. |
C.在中间产物中 状态最稳定 状态最稳定 |
D. 的活化能为: 的活化能为: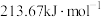 |
您最近一年使用:0次
2023-05-21更新
|
211次组卷
|
16卷引用:山东省德州市夏津第一中学2021届高三上学期10月月考化学试题
山东省德州市夏津第一中学2021届高三上学期10月月考化学试题(已下线)小题必刷23 焓变与热化学方程式——2021年高考化学一轮复习小题必刷(通用版)安徽省宣城市六校2021-2022学年高二上学期期中联考化学试题湖北省黄冈中学2022届高三适应性考试(四模)化学试题湖南省浏阳市第一中学2023届高二下学期期末考试化学试题(已下线)第17讲 化学能与热能(练)-2023年高考化学一轮复习讲练测(全国通用)四川省德阳市第五中学2022-2023学年高二上学期开学考试化学试题山东省济宁市梁山县第一中学2022-2023学年高二10月月考化学试题湖北省黄冈市蕲春县第四高级中学2021-2022学年上学期高三11月月考化学试题山东省济宁市梁山一中2022-2023学年高二上学期11月月考化学试题云南省蒙自市第一高级中学2022-2023学年高二下学期3月月考化学试题陕西省宝鸡市2022-2023学年高二上学期期末考试化学试题黑龙江省鹤岗市第一中学2022-2023学年高三上学期11月月考化学试题(已下线)专题03 化学反应速率及影响因素、活化能【考题猜想】(9大题型)-2023-2024学年高二化学期中考点大串讲(人教版2019选择性必修1)甘肃省武威市天祝一中、民勤一中、古浪一中等四校联考2023-2024学年高二上学期11月期中考试化学试题山东省淄博市淄川中学2023-2024学年高二上学期11月期中考试化学试卷
名校
解题方法
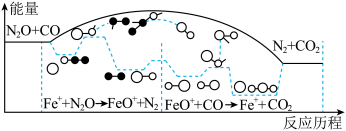
5 . 研究表明CO与 在
在 作用下发生反应的能量变化及反应历程如图所示,两步反应分别为:①
作用下发生反应的能量变化及反应历程如图所示,两步反应分别为:①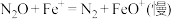 ;②
;② 。下列说法正确的是
。下列说法正确的是
 在
在 作用下发生反应的能量变化及反应历程如图所示,两步反应分别为:①
作用下发生反应的能量变化及反应历程如图所示,两步反应分别为:①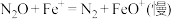 ;②
;② 。下列说法正确的是
。下列说法正确的是
| A.反应①是氧化还原反应,反应②是非氧化还原反应 |
| B.两步反应均为放热反应,总反应的化学反应速率由反应②决定 |
C.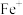 使反应的活化能减小, 使反应的活化能减小,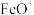 是中间产物 是中间产物 |
D.若转移1mol电子,则消耗11.2L |
您最近一年使用:0次
2022-12-03更新
|
407次组卷
|
26卷引用:【市级联考】湖南省岳阳市2019届高三上学期教学质量检测(一模)化学试题
【市级联考】湖南省岳阳市2019届高三上学期教学质量检测(一模)化学试题2020届全国II卷高考化学模拟卷(三)(已下线)专题6.1 化学能与热能(练)——2020年高考化学一轮复习讲练测宁夏回族自治区银川市第一中学2020届高三第四次模拟考试理综化学试题陕西省西安中学2020届高三仿真考试(一)化学试题河南省洛阳市新安县第一高级中学2021届高三入学测试化学试题四川省阆中中学2021届高三上学期9月月考理综化学试题湖南省永州市2021届高三第一次模拟化学试题黑龙江省鹤岗市第一中学2021届高三上学期第二次月考化学试题江西省南昌市第二中学2020-2021学年高二上学期第三次月考化学试题江西省抚州市黎川县第一中学2020-2021学年高二上学期第三次月考化学试题江西省景德镇一中2020-2021学年高一下学期期末考试化学(2班)试题甘肃省嘉峪关市第一中学2021届高三上学期二模考试化学试题福建省福州格致中学2021-2022学年高二上学期第一阶段测试化学试题(10月)(已下线)专题10 化学反应机理分析-【微专题·大素养】备战2022年高考化学讲透提分要点江西省奉新县第一中学2021-2022学年上学期高三第一次月考化学试题河南省重点高中2021-2022学年高二下学期阶段性调研联考一化学试题广东省深圳市重点中学2021-2022学年高二上学期期末考试化学试题江西省丰城市第九中学2021-2022学年高二上学期第二次月考(日新班)化学试题湖北省武汉市部分重点中学2022-2023学年高二上学期10月联考化学试题福建省龙岩市永定区坎市中学2022-2023学年高三上学期期中化学试题福建省晋江市第一中学2021-2022学年高二上学期线上学习诊断暨单元测试(第一次月考)化学试题湖北省公安县第三中学2021-2022学年高三上学期10月质量检测化学试题(已下线)题型22 反应历程—活化能—催化剂的定性和定量分析广东省广州市执信中学2021届高三第五次月考化学试题四川省凉山州宁南中学2023-2024学年高二上学期第一次月考化学试题
名校
解题方法
6 . 在催化剂中添加Na、K、Cu助剂后(助剂也起催化作用)可改变反应的选择性。用催化剂Fe3(CO)12/ZSM-5催化CO2加氢合成低碳烯烃反应,所得产物含CH4、C3H6、C4H8等副产物,反应过程如图,下列说法不正确的是
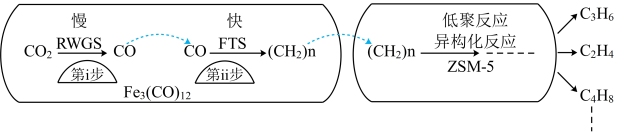

| A.第i步反应的活化能高于第ii步 |
| B.添加不同助剂后,反应的平衡常数各不相同 |
| C.第i步反应为CO2+H2⇌CO+H2O |
| D.Fe3(CO)12/ZSM-5不能改变CO2加氢合成低碳烯反应的△H |
您最近一年使用:0次
2022-10-28更新
|
85次组卷
|
2卷引用:山东省青岛第二中学2020-2021学年高二上学期期中考试化学试题
名校
解题方法
7 . 已知:NO和O2转化为NO2的反应机理如下:
①2NO(g) N2O2(g)(快) △H1<0 平衡常数K1
N2O2(g)(快) △H1<0 平衡常数K1
②N2O2(g)+O2(g) 2NO2(g)(慢) △H2<0 平衡常数K2
2NO2(g)(慢) △H2<0 平衡常数K2
下列说法正确的是
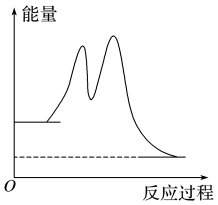
图a
①2NO(g)
 N2O2(g)(快) △H1<0 平衡常数K1
N2O2(g)(快) △H1<0 平衡常数K1②N2O2(g)+O2(g)
 2NO2(g)(慢) △H2<0 平衡常数K2
2NO2(g)(慢) △H2<0 平衡常数K2下列说法正确的是

图a
A.2NO(g)+O2(g)  2NO2(g)的△H= - (△H1+△H2) 2NO2(g)的△H= - (△H1+△H2) |
B.反应②的速率大小决定2NO(g)+O2(g)  2NO2(g)的反应速率 2NO2(g)的反应速率 |
| C.反应过程中的能量变化可用图a表示 |
D.2NO(g)+O2(g)  2NO2(g)的平衡常数 2NO2(g)的平衡常数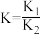 |
您最近一年使用:0次
2022-10-17更新
|
622次组卷
|
12卷引用:安徽省淮北市第一中学2017-2018学年上学期高二年级期末考试化学试题
安徽省淮北市第一中学2017-2018学年上学期高二年级期末考试化学试题江西省南昌市新建区第二中学2019-2020学年高一下学期“新星计划”体验营7月期终考试化学试题四川省成都石室中学2021-2022学年高二上学期9月测试化学试题安徽省毫州市涡阳第—中学2021-2022学年高二上学期第一次教学质量检测化学试题天津市静海区四校2021-2022学年高二上学期11月阶段性检测化学试题黑龙江省牡丹江市第三高级中学2021-2022学年高三上学期第四次月考化学试题广东省佛山市第一中学2022-2023学年高二上学期10月月考化学试题陕西省西安市第三中学2022-2023学年高二上学期10月月测评化学试题四川省广安代市中学校2021-2022学年高二上学期9月考化学试题福建省泉州第五中学2022-2023学年高二上学期期中考化学试题天津市宁河区芦台第一中学2022-2023学年高二上学期11月月考化学试题陕西省渭南市瑞泉中学2023-2024学年高二上学期第一次质量检测化学试题
名校
解题方法
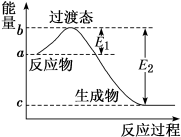
8 . 如图为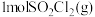 和
和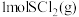 反应生成
反应生成 过程中的能量变化示意图,已知
过程中的能量变化示意图,已知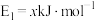 、
、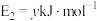 ,下列有关说法中正确的是
,下列有关说法中正确的是
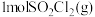 和
和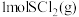 反应生成
反应生成 过程中的能量变化示意图,已知
过程中的能量变化示意图,已知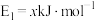 、
、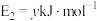 ,下列有关说法中正确的是
,下列有关说法中正确的是
| A.若在反应体系中加入催化剂,E1不变 |
| B.若在反应体系中加入催化剂,△H减小 |
C.反应的活化能等于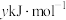 |
D.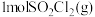 和 和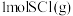 反应生成 反应生成 的 的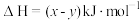 |
您最近一年使用:0次
2022-10-08更新
|
481次组卷
|
10卷引用:2017届江苏省南通市高三高考全真模拟(一)化学试卷
2017届江苏省南通市高三高考全真模拟(一)化学试卷辽宁省六校协作体2016-2017学年高一下学期期中考试化学试题吉林省延边安图第一中学2016-2017学年高二练习化学试题河北省邢台市第二中学2018届高三上学期第一次月考(开学考试)化学试题陕西省咸阳市武功县普集高中2017-2018学年高二上学期第二次月考(9月)化学试题贵州省思南中学2019-2020学年高二9月月考化学试题江苏省启东中学2020-2021学年高二上学期期初考试化学试题四川省阆中中学校2020-2021学年高一(仁智班)下学期第一次月考化学试题天津汇文中学2022-2023学年高二上学期第一次阶段性测试化学试题天津市第二中学2022-2023学年高二上学期期中检测化学试题
9 . 碳的化合物在工业上应用广泛。
(1)已知下列热化学方程式:
ⅰ.CH2=CHCH3(g)+ Cl2(g)=CH2ClCHClCH3(g) H1=-133 kJ·mol-1
ⅱ.CH2=CHCH3(g)+Cl2(g)=CH2=CHCH2Cl(g)+HCl(g) ΔH2=-100 kJ·mol-1
又已知在相同条件下,CH2=CHCH2Cl(g)+HCl(g)=CH2ClCHClCH3(g) 的正反应的活化能Ea(正)为132 kJ·mol-1,则逆反应的活化能Ea(逆)为________ kJ·mol-1。
(2)查阅资料得知,反应CH3CHO(aq)=CH4(g)+CO(g)在含有少量I2的溶液中分两步进行:
第Ⅰ步反应为CH3CHO(aq)+I2(aq)→CH3I(l)+HI(aq)+CO(g)(慢反应);
第Ⅱ步为快反应。增大I2的浓度________ (填“能”或“ 不能”)明显增大总反应的平均速率,理由为_____________________________ 。
(3)用催化剂Fe3(CO)12/ZSM5催化CO2加氢合成乙烯的反应,所得产物含CH4、C3H6、C4H8等副产物,反应过程如图。
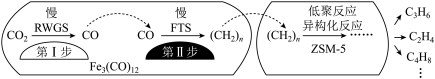
催化剂中添加Na、K、Cu助剂后(助剂也起催化作用)可改变反应的选择性,在其他条件相同时,添加不同助剂,经过相同时间后测得CO2转化率和各产物的物质的量分数如下表。
欲提高单位时间内乙烯的产量,在Fe3(CO)12/ZSM5中添加________ 助剂效果最好;加入助剂能提高单位时间内乙烯产量的根本原因是____________ 。
(4)在一密闭容器中,起始时向该容器中充入H2S和CH4且n(H2S)∶n(CH4) =2∶1,发生反应:CH4(g)+2H2S(g)=CS2(g)+4H2(g)。0.11 MPa时,温度变化对平衡时产物的物质的量分数的影响如图所示:
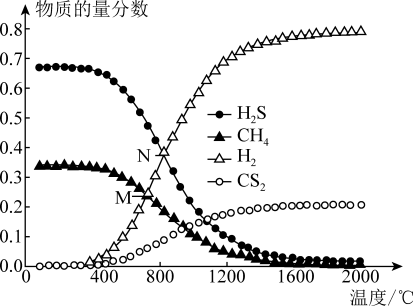
为提高H2S的平衡转化率,除改变温度外,还可采取的措施是____________________ (列举一条)。N点对应温度下,该反应的Kp=_____ (MPa)2(Kp为以分压表示的平衡常数)。
(5)合成碳酸二甲酯的工作原理如图所示。
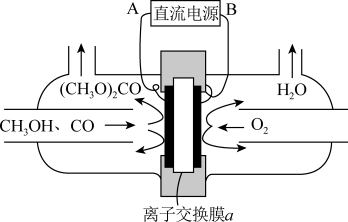
阳极的电极反应式为__________ ,离子交换膜a为________ (填“阳膜”“阴膜”)。
(1)已知下列热化学方程式:
ⅰ.CH2=CHCH3(g)+ Cl2(g)=CH2ClCHClCH3(g) H1=-133 kJ·mol-1
ⅱ.CH2=CHCH3(g)+Cl2(g)=CH2=CHCH2Cl(g)+HCl(g) ΔH2=-100 kJ·mol-1
又已知在相同条件下,CH2=CHCH2Cl(g)+HCl(g)=CH2ClCHClCH3(g) 的正反应的活化能Ea(正)为132 kJ·mol-1,则逆反应的活化能Ea(逆)为
(2)查阅资料得知,反应CH3CHO(aq)=CH4(g)+CO(g)在含有少量I2的溶液中分两步进行:
第Ⅰ步反应为CH3CHO(aq)+I2(aq)→CH3I(l)+HI(aq)+CO(g)(慢反应);
第Ⅱ步为快反应。增大I2的浓度
(3)用催化剂Fe3(CO)12/ZSM5催化CO2加氢合成乙烯的反应,所得产物含CH4、C3H6、C4H8等副产物,反应过程如图。

催化剂中添加Na、K、Cu助剂后(助剂也起催化作用)可改变反应的选择性,在其他条件相同时,添加不同助剂,经过相同时间后测得CO2转化率和各产物的物质的量分数如下表。
助剂 | CO2转化率(%) | 各产物在所有产物中的占比(%) | ||
C2H4 | C3H6 | 其他 | ||
Na | 42.5 | 35.9 | 39.6 | 24.5 |
K | 27.2 | 75.6 | 22.8 | 1.6 |
Cu | 9.8 | 80.7 | 12.5 | 6.8 |
(4)在一密闭容器中,起始时向该容器中充入H2S和CH4且n(H2S)∶n(CH4) =2∶1,发生反应:CH4(g)+2H2S(g)=CS2(g)+4H2(g)。0.11 MPa时,温度变化对平衡时产物的物质的量分数的影响如图所示:

为提高H2S的平衡转化率,除改变温度外,还可采取的措施是
(5)合成碳酸二甲酯的工作原理如图所示。

阳极的电极反应式为
您最近一年使用:0次
2022-09-26更新
|
296次组卷
|
6卷引用:湖北省武汉市2020届高三毕业生六月供题(二)理科综合化学试题
解题方法
10 . 下列说法不正确 的是
| A.能发生有效碰撞的分子叫活化分子 | B.升温,活化分子百分数增大,反应速率增大 |
| C.增大反应物浓度,活化分子百分数增大 | D.催化剂能增大活化分子百分数,速率增大 |
您最近一年使用:0次
2022-09-18更新
|
175次组卷
|
2卷引用:陕西省千阳中学2020-2021学年高二上学期期中化学(理科)试题



