1 .  是一种强还原性的高能物质,在航天、能源等领域有广泛应用。我国科学家合成的某
是一种强还原性的高能物质,在航天、能源等领域有广泛应用。我国科学家合成的某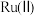 催化剂(用
催化剂(用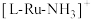 表示)能高效电催化氧化
表示)能高效电催化氧化 合成
合成 ,其反应机理如图所示。下列说法正确的是
,其反应机理如图所示。下列说法正确的是
 是一种强还原性的高能物质,在航天、能源等领域有广泛应用。我国科学家合成的某
是一种强还原性的高能物质,在航天、能源等领域有广泛应用。我国科学家合成的某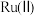 催化剂(用
催化剂(用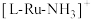 表示)能高效电催化氧化
表示)能高效电催化氧化 合成
合成 ,其反应机理如图所示。下列说法正确的是
,其反应机理如图所示。下列说法正确的是
A.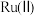 催化剂降低该反应的活化能,大大缩短达到化学平衡所需的时间 催化剂降低该反应的活化能,大大缩短达到化学平衡所需的时间 |
B.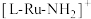 中氮原子上有孤电子对 中氮原子上有孤电子对 |
C.该过程的总反应式为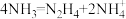 |
D.由于 中存在非极性共价键,所以 中存在非极性共价键,所以 易溶于水 易溶于水 |
您最近半年使用:0次
2 . 我国科学家实现了在铜催化条件下将DMF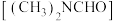 转化为三甲铵
转化为三甲铵 。计算机模拟单个DMF分子在铜催化剂表面的反应历程如图所示。下列说法错误的是
。计算机模拟单个DMF分子在铜催化剂表面的反应历程如图所示。下列说法错误的是
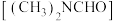 转化为三甲铵
转化为三甲铵 。计算机模拟单个DMF分子在铜催化剂表面的反应历程如图所示。下列说法错误的是
。计算机模拟单个DMF分子在铜催化剂表面的反应历程如图所示。下列说法错误的是
A.该反应的 | B.该反应在高温下能自发进行 |
| C.该历程中最大能垒为1.19eV | D.其他条件不变,增大压强可提高DMF平衡转化率 |
您最近半年使用:0次
解题方法
3 . 随着我国碳达峰、碳中和目标的确定,二氧化碳资源化利用倍受关注。
I.以 和
和 为原料合成尿素
为原料合成尿素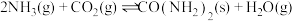
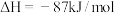 。
。
(1)有利于提高 平衡转化率的措施是___________(填序号)。
平衡转化率的措施是___________(填序号)。
(2)研究发现,合成尿素反应分两步完成,其能量变化如下图所示:
第一步: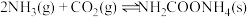

第二步: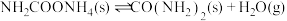


___________  。
。
②决定该反应速率是___________ 反应(填“第一步”或“第二步”),理由是___________ 。
Ⅱ.以和催化重整制备合成气: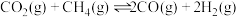 。
。
(3)在密闭容器中通入物质的量均为 的
的 和
和 ,在一定条件下发生反应
,在一定条件下发生反应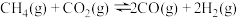 ,
, 的平衡转化率随温度、压强的变化关系如图所示。
的平衡转化率随温度、压强的变化关系如图所示。___________ (填序号)。
A.容器中混合气体的密度保持不变 B.容器内混合气体的压强保持不变
C.反应速率: D.同时断裂
D.同时断裂 键和
键和 键
键
②由图可知,压强
___________  (填“>”“<”或“=”,下同);
(填“>”“<”或“=”,下同); 点速率
点速率
___________ 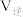 。
。
③已知气体分压=气体总压×气体的物质的量分数,用平衡分压代替平衡浓度可以得到平衡常数 ,则
,则 点对应温度下的
点对应温度下的
___________ (用含 的代数式表示)。
的代数式表示)。
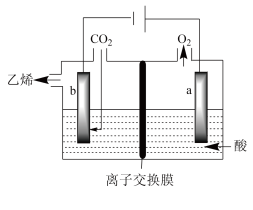
Ⅲ.电化学法还原二氧化碳制乙烯
在强酸性溶液中通入二氧化碳,用惰性电极进行电解可制得乙烯,其原理如图所示:___________ 。
I.以
 和
和 为原料合成尿素
为原料合成尿素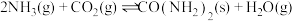
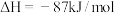 。
。(1)有利于提高
 平衡转化率的措施是___________(填序号)。
平衡转化率的措施是___________(填序号)。| A.高温低压 | B.低温高压 | C.高温高压 | D.低温低压 |
(2)研究发现,合成尿素反应分两步完成,其能量变化如下图所示:
第一步:
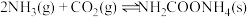

第二步:
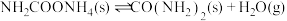

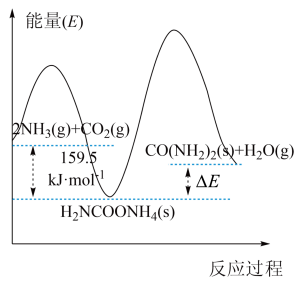

 。
。②决定该反应速率是
Ⅱ.以和催化重整制备合成气:
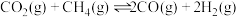 。
。(3)在密闭容器中通入物质的量均为
 的
的 和
和 ,在一定条件下发生反应
,在一定条件下发生反应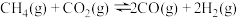 ,
, 的平衡转化率随温度、压强的变化关系如图所示。
的平衡转化率随温度、压强的变化关系如图所示。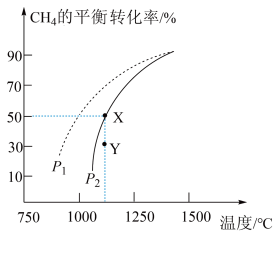
A.容器中混合气体的密度保持不变 B.容器内混合气体的压强保持不变
C.反应速率:
 D.同时断裂
D.同时断裂 键和
键和 键
键②由图可知,压强

 (填“>”“<”或“=”,下同);
(填“>”“<”或“=”,下同); 点速率
点速率
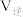 。
。③已知气体分压=气体总压×气体的物质的量分数,用平衡分压代替平衡浓度可以得到平衡常数
 ,则
,则 点对应温度下的
点对应温度下的
 的代数式表示)。
的代数式表示)。Ⅲ.电化学法还原二氧化碳制乙烯
在强酸性溶液中通入二氧化碳,用惰性电极进行电解可制得乙烯,其原理如图所示:
您最近半年使用:0次
4 . 工业上可采用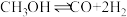 的方法来制取高纯度的
的方法来制取高纯度的 和
和 。我国学者采用量子力学方法,通过计算机模拟,研究了在钯基催化剂表面上甲醇制氢的反应历程,其中吸附在钯催化剂表面上的物种用*标注。甲醇(
。我国学者采用量子力学方法,通过计算机模拟,研究了在钯基催化剂表面上甲醇制氢的反应历程,其中吸附在钯催化剂表面上的物种用*标注。甲醇( )脱氢反应的第一步历程,有如下两种可能方式(其中
)脱氢反应的第一步历程,有如下两种可能方式(其中 、
、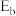 为活化能):
为活化能):
方式①: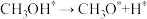
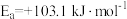
方式②: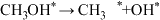
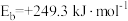
图为计算机模拟的各步反应的能量变化示意图。
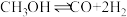 的方法来制取高纯度的
的方法来制取高纯度的 和
和 。我国学者采用量子力学方法,通过计算机模拟,研究了在钯基催化剂表面上甲醇制氢的反应历程,其中吸附在钯催化剂表面上的物种用*标注。甲醇(
。我国学者采用量子力学方法,通过计算机模拟,研究了在钯基催化剂表面上甲醇制氢的反应历程,其中吸附在钯催化剂表面上的物种用*标注。甲醇( )脱氢反应的第一步历程,有如下两种可能方式(其中
)脱氢反应的第一步历程,有如下两种可能方式(其中 、
、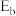 为活化能):
为活化能):方式①:
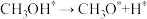
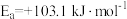
方式②:
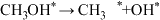
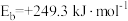
图为计算机模拟的各步反应的能量变化示意图。
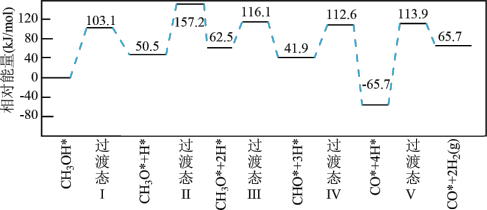
| A.主要历经方式② |
B.总反应的焓变( )大于0 )大于0 |
C.最小能垒(活化能)为 |
D.焓变最小的基元反应为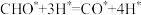 |
您最近半年使用:0次
解题方法
5 . 甲醇( )作为重要的清洁燃料和合成化学的关键前驱体,在化工行业需求旺盛。以
)作为重要的清洁燃料和合成化学的关键前驱体,在化工行业需求旺盛。以 为催化剂在水溶液中电催化二氧化碳还原为
为催化剂在水溶液中电催化二氧化碳还原为 和
和 的能量变化如图所示:
的能量变化如图所示:
 )作为重要的清洁燃料和合成化学的关键前驱体,在化工行业需求旺盛。以
)作为重要的清洁燃料和合成化学的关键前驱体,在化工行业需求旺盛。以 为催化剂在水溶液中电催化二氧化碳还原为
为催化剂在水溶液中电催化二氧化碳还原为 和
和 的能量变化如图所示:
的能量变化如图所示: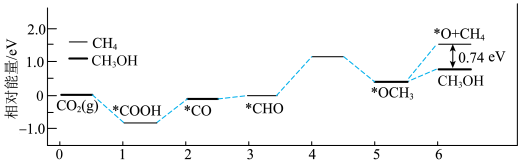
A.生成甲醇反应的决速步为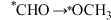 |
| B.两反应只涉及极性键的断裂和生成 |
| C.通过上图分析:甲烷比甲醇稳定 |
D.用 作催化剂可提高甲醇的选择性 作催化剂可提高甲醇的选择性 |
您最近半年使用:0次
解题方法
6 . 一定条件下,1-苯基丙炔(Ph-C=C-CH3)可与HCl发生催化加成,反应如下:不正确 的是
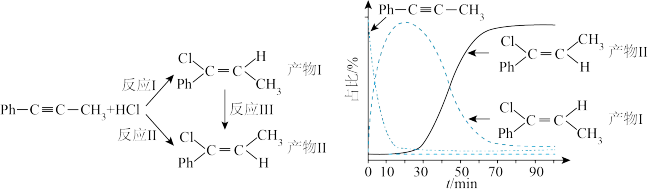
| A.反应活化能:反应I<反应Ⅱ |
| B.反应焓变:反应I<反应Ⅱ |
| C.增加HCl浓度不会改变平衡时产物Ⅱ和产物I的比例 |
| D.选择相对较短的反应时间,及时分离可获得高产率的产物Ⅰ |
您最近半年使用:0次
名校
7 . 环境科学研究发现, 也是一种温室效应气体,与
也是一种温室效应气体,与 相比,虽然
相比,虽然 在大气中的含量很低,增温潜势却是二氧化碳的298倍,对全球气候的增温效应在未来将越来越显著,已引起科学家的极大关注。
在大气中的含量很低,增温潜势却是二氧化碳的298倍,对全球气候的增温效应在未来将越来越显著,已引起科学家的极大关注。 的能量变化如上图所示,则无催化剂条件下该反应的逆反应的活化能为
的能量变化如上图所示,则无催化剂条件下该反应的逆反应的活化能为__________ ;在相同温度和压强下,1mol  和1mol CO经过相同反应时间测得如下实验数据:
和1mol CO经过相同反应时间测得如下实验数据:
试分析在相同温度时,催化剂2催化下 的转化率更高的原因是
的转化率更高的原因是___________ 。
(2)在容积均为1L的密闭容器A(起始500℃,恒温)、B(起始500℃,绝热)两个容器中分别加入0.1mol 、0.4mol CO和相同催化剂。实验测得A、B容器中
、0.4mol CO和相同催化剂。实验测得A、B容器中 的转化率随时间的变化关系如图所示:
的转化率随时间的变化关系如图所示: 的转化率随时间的变化关系是图中的
的转化率随时间的变化关系是图中的___________ 曲线(填“a”或“b”)。
②要缩短b曲线对应容器达到平衡的时间,但不改变 的平衡转化率,在催化剂一定的情况下可采取的措施是
的平衡转化率,在催化剂一定的情况下可采取的措施是___________ (答出一条即可)。
③500℃该反应的化学平衡常数K=___________ (用最简分数表示)。
④实验测定该反应的反应速率 ,
, ,
, 、
、 分别是正、逆反应速率常数,c为物质的量浓度,计算M处的
分别是正、逆反应速率常数,c为物质的量浓度,计算M处的
___________ (保留两位小数)。
 也是一种温室效应气体,与
也是一种温室效应气体,与 相比,虽然
相比,虽然 在大气中的含量很低,增温潜势却是二氧化碳的298倍,对全球气候的增温效应在未来将越来越显著,已引起科学家的极大关注。
在大气中的含量很低,增温潜势却是二氧化碳的298倍,对全球气候的增温效应在未来将越来越显著,已引起科学家的极大关注。
 的能量变化如上图所示,则无催化剂条件下该反应的逆反应的活化能为
的能量变化如上图所示,则无催化剂条件下该反应的逆反应的活化能为 和1mol CO经过相同反应时间测得如下实验数据:
和1mol CO经过相同反应时间测得如下实验数据:| 实验 | 温度/℃ | 催化剂 |  的转化率/% 的转化率/% |
| 实验1 | 400 | 催化剂1 | 9.5 |
| 400 | 催化剂2 | 10.6 | |
| 实验2 | 500 | 催化剂1 | 12.3 |
| 500 | 催化剂2 | 13.5 |
 的转化率更高的原因是
的转化率更高的原因是(2)在容积均为1L的密闭容器A(起始500℃,恒温)、B(起始500℃,绝热)两个容器中分别加入0.1mol
 、0.4mol CO和相同催化剂。实验测得A、B容器中
、0.4mol CO和相同催化剂。实验测得A、B容器中 的转化率随时间的变化关系如图所示:
的转化率随时间的变化关系如图所示:
 的转化率随时间的变化关系是图中的
的转化率随时间的变化关系是图中的②要缩短b曲线对应容器达到平衡的时间,但不改变
 的平衡转化率,在催化剂一定的情况下可采取的措施是
的平衡转化率,在催化剂一定的情况下可采取的措施是③500℃该反应的化学平衡常数K=
④实验测定该反应的反应速率
 ,
, ,
, 、
、 分别是正、逆反应速率常数,c为物质的量浓度,计算M处的
分别是正、逆反应速率常数,c为物质的量浓度,计算M处的
您最近半年使用:0次
8 . 铋基催化剂对 电化学还原制取
电化学还原制取 具有高效的选择性。其反应历程与能量变化如图所示,其中吸附在催化剂表面上的物种用*标注。
具有高效的选择性。其反应历程与能量变化如图所示,其中吸附在催化剂表面上的物种用*标注。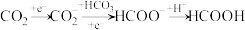
 电化学还原制取
电化学还原制取 具有高效的选择性。其反应历程与能量变化如图所示,其中吸附在催化剂表面上的物种用*标注。
具有高效的选择性。其反应历程与能量变化如图所示,其中吸附在催化剂表面上的物种用*标注。
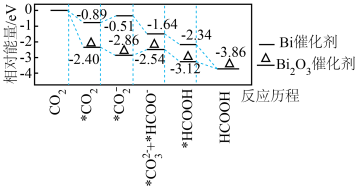
A.使用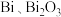 两种催化剂中 两种催化剂中 更有利于 更有利于 的吸附 的吸附 |
B. 电化学还原制取 电化学还原制取 的反应 的反应 |
C.使用 催化剂时,最大能垒是 催化剂时,最大能垒是 |
D.由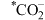 生成 生成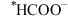 的反应为 的反应为 |
您最近半年使用:0次
9 . 空气中 含量的控制和
含量的控制和 资源利用,具有重要意义。
资源利用,具有重要意义。
(1)燃煤烟气中的 捕集可通过如下所示的物质转化实现。
捕集可通过如下所示的物质转化实现。

“吸收”后所得的 溶液与石灰乳反应的化学方程式为
溶液与石灰乳反应的化学方程式为______ ;载人航天器内,常用LiOH固体而很少用KOH固体吸收空气中的 ,其原因是
,其原因是______ 。
(2)二氧化碳催化加氢制甲醇,涉及反应有:
反应Ⅰ.

反应Ⅱ.

反应Ⅲ.

某压强下在体积固定的密闭容器中,按照 投料发生反应Ⅰ、Ⅱ、Ⅲ。
投料发生反应Ⅰ、Ⅱ、Ⅲ。
平衡时,CO、 在含碳产物中物质的量分数及
在含碳产物中物质的量分数及 转化率随温度的变化如下图一所示。
转化率随温度的变化如下图一所示。

①n曲线代表的物质为______ 。
②在150~250℃范围内, 转化率随温度升高而降低的原因是
转化率随温度升高而降低的原因是______ 。
(3) 和
和 反应制备
反应制备 的反应机理如下图二所示(带*的表示吸附在催化剂表面)
的反应机理如下图二所示(带*的表示吸附在催化剂表面)

①研究表明,图中过程ⅱ的活化能小但实际反应速率慢,是控速步骤,导致该步反应速率小的原因可能是______ 。
A. 对该反应有阻碍作用 B.其它物种的存在削弱了同一吸附位上H的吸附
对该反应有阻碍作用 B.其它物种的存在削弱了同一吸附位上H的吸附
C.温度变化导致活化能增大 D.温度变化导致平衡常数减小
②已知:图中HCOO为甲酸物种,结构是 ,
,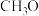 为甲氧基物种。从化学键视角将图中ⅰ与ⅱ的过程可描述为
为甲氧基物种。从化学键视角将图中ⅰ与ⅱ的过程可描述为______ 。
 含量的控制和
含量的控制和 资源利用,具有重要意义。
资源利用,具有重要意义。(1)燃煤烟气中的
 捕集可通过如下所示的物质转化实现。
捕集可通过如下所示的物质转化实现。
“吸收”后所得的
 溶液与石灰乳反应的化学方程式为
溶液与石灰乳反应的化学方程式为 ,其原因是
,其原因是(2)二氧化碳催化加氢制甲醇,涉及反应有:
反应Ⅰ.


反应Ⅱ.


反应Ⅲ.


某压强下在体积固定的密闭容器中,按照
 投料发生反应Ⅰ、Ⅱ、Ⅲ。
投料发生反应Ⅰ、Ⅱ、Ⅲ。平衡时,CO、
 在含碳产物中物质的量分数及
在含碳产物中物质的量分数及 转化率随温度的变化如下图一所示。
转化率随温度的变化如下图一所示。
①n曲线代表的物质为
②在150~250℃范围内,
 转化率随温度升高而降低的原因是
转化率随温度升高而降低的原因是(3)
 和
和 反应制备
反应制备 的反应机理如下图二所示(带*的表示吸附在催化剂表面)
的反应机理如下图二所示(带*的表示吸附在催化剂表面)
①研究表明,图中过程ⅱ的活化能小但实际反应速率慢,是控速步骤,导致该步反应速率小的原因可能是
A.
 对该反应有阻碍作用 B.其它物种的存在削弱了同一吸附位上H的吸附
对该反应有阻碍作用 B.其它物种的存在削弱了同一吸附位上H的吸附C.温度变化导致活化能增大 D.温度变化导致平衡常数减小
②已知:图中HCOO为甲酸物种,结构是
 ,
,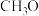 为甲氧基物种。从化学键视角将图中ⅰ与ⅱ的过程可描述为
为甲氧基物种。从化学键视角将图中ⅰ与ⅱ的过程可描述为
您最近半年使用:0次
解题方法
10 . 接触法制硫酸的工艺流程中的关键步骤是SO2的催化氧化: ,在催化剂表面的反应历程如下:
,在催化剂表面的反应历程如下:
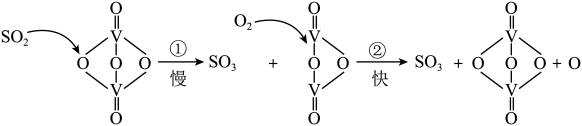
下列说法正确的是
 ,在催化剂表面的反应历程如下:
,在催化剂表面的反应历程如下:
下列说法正确的是
| A.过程中既有V-O键的断裂,又有V-O键的形成 |
| B.该反应的中间产物是V2O5 |
| C.反应①的活化能比反应②大 |
| D.反应放热,为提高SO2转化率,应尽可能在较低温度下反应 |
您最近半年使用:0次



