1 . 18O标记的乙酸甲酯在足量NaOH溶液中发生水解,部分反应历程可表示为如下所示:
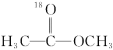 +OH-
+OH-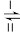
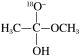
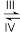
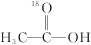 +CH3O-
+CH3O-
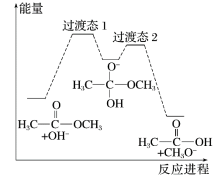
已知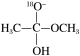

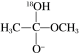 为快速平衡,下列说法正确的是
为快速平衡,下列说法正确的是
| A.反应Ⅱ、Ⅲ为决速步 |
| B.反应结束后,溶液中存在18OH- |
| C.反应结束后,溶液中存在CH318OH |
| D.反应Ⅰ与反应Ⅳ活化能的差值等于图示总反应的焓变 |
您最近一年使用:0次
2 . 乙烯和HCl加成经历2步基元反应如图甲所示,其反应过程中能量的变化情况如图乙所示。下列有关乙烯和HCl的加成反应说法错误的是


| A.总反应的速率取决于第①步 | B.第②步反应是放热反应 |
C.中间产物CH3CH 能量高、不稳定 能量高、不稳定 | D.反应物的总键能高于生成物的总键能 |
您最近一年使用:0次
名校
解题方法
3 . 催化还原 是实现“碳中和”的重要途径之一、研究表明,在催化剂作用下,
是实现“碳中和”的重要途径之一、研究表明,在催化剂作用下, 和
和 发生反应:
发生反应:
I.

Ⅱ.

(1)已知 和
和 的燃烧热分别为
的燃烧热分别为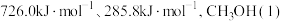 和
和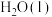 的汽化热分别为
的汽化热分别为 。则
。则
___________  。
。
(2)下列关于反应I和反应Ⅱ的说法错误的是___________ (填标号)。
A.增大 与
与 的投料比有利于提高
的投料比有利于提高 的转化率
的转化率
B.若 的浓度保持不变,则说明反应体系已达平衡状态
的浓度保持不变,则说明反应体系已达平衡状态
C.体系达到平衡后,若升高温度,两个反应重新建立平衡的时间相同
D.体系达到平衡后,若压缩体积,则反应I平衡正向移动,反应Ⅱ平衡不移动
E.及时将 液化分离,有利于提高反应I的正反应速率
液化分离,有利于提高反应I的正反应速率
(3)一般认为反应I通过如下步骤实现:
第一步:
 (慢)
(慢)
第二步:
 (快)
(快)
下列示意图中能体现上述反应能量变化的是___________(填标号)。
(4)研究发现 表面脱除
表面脱除 原子形成的
原子形成的 (氧空穴)决定了
(氧空穴)决定了 的催化效果,氧空穴越多,催化效果越好,
的催化效果,氧空穴越多,催化效果越好, 催化
催化 合成甲醇的机理如图。已知增大气体流速可带走多余的
合成甲醇的机理如图。已知增大气体流速可带走多余的 ,从而提高
,从而提高 的选择性,请结合催化机理解释其原因
的选择性,请结合催化机理解释其原因___________ 。

(5)一定温度下,向 恒容的密闭容器中充入
恒容的密闭容器中充入 和
和 。在催化剂作用下发生反应I、II,容器内气体的压强随反应时间的变化如表所示。
。在催化剂作用下发生反应I、II,容器内气体的压强随反应时间的变化如表所示。
平衡时测得 在体系中的体积分数为
在体系中的体积分数为 。则0~20min内平均反应速率
。则0~20min内平均反应速率
___________  ;该条件下,
;该条件下, 的选择性(甲醇的物质的量占消耗的
的选择性(甲醇的物质的量占消耗的 的物质的量的百分比)为
的物质的量的百分比)为___________  (结果保留三位有效数字);该温度下反应I的平衡常数
(结果保留三位有效数字);该温度下反应I的平衡常数
___________  (
( 为以平衡分压代替平衡浓度表示的平衡常数,列出计算式即可)。
为以平衡分压代替平衡浓度表示的平衡常数,列出计算式即可)。
 是实现“碳中和”的重要途径之一、研究表明,在催化剂作用下,
是实现“碳中和”的重要途径之一、研究表明,在催化剂作用下, 和
和 发生反应:
发生反应:I.


Ⅱ.


(1)已知
 和
和 的燃烧热分别为
的燃烧热分别为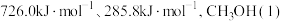 和
和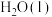 的汽化热分别为
的汽化热分别为 。则
。则
 。
。(2)下列关于反应I和反应Ⅱ的说法错误的是
A.增大
 与
与 的投料比有利于提高
的投料比有利于提高 的转化率
的转化率B.若
 的浓度保持不变,则说明反应体系已达平衡状态
的浓度保持不变,则说明反应体系已达平衡状态C.体系达到平衡后,若升高温度,两个反应重新建立平衡的时间相同
D.体系达到平衡后,若压缩体积,则反应I平衡正向移动,反应Ⅱ平衡不移动
E.及时将
 液化分离,有利于提高反应I的正反应速率
液化分离,有利于提高反应I的正反应速率(3)一般认为反应I通过如下步骤实现:
第一步:

 (慢)
(慢)第二步:

 (快)
(快)下列示意图中能体现上述反应能量变化的是___________(填标号)。
A. | B. | C. | D.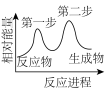 |
(4)研究发现
 表面脱除
表面脱除 原子形成的
原子形成的 (氧空穴)决定了
(氧空穴)决定了 的催化效果,氧空穴越多,催化效果越好,
的催化效果,氧空穴越多,催化效果越好, 催化
催化 合成甲醇的机理如图。已知增大气体流速可带走多余的
合成甲醇的机理如图。已知增大气体流速可带走多余的 ,从而提高
,从而提高 的选择性,请结合催化机理解释其原因
的选择性,请结合催化机理解释其原因
(5)一定温度下,向
 恒容的密闭容器中充入
恒容的密闭容器中充入 和
和 。在催化剂作用下发生反应I、II,容器内气体的压强随反应时间的变化如表所示。
。在催化剂作用下发生反应I、II,容器内气体的压强随反应时间的变化如表所示。 | 0 | 5 | 10 | 15 | 20 | 25 |
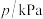 | 6.0 | 5.55 | 5.2 | 4.95 | 4.8 | 4.8 |
 在体系中的体积分数为
在体系中的体积分数为 。则0~20min内平均反应速率
。则0~20min内平均反应速率
 ;该条件下,
;该条件下, 的选择性(甲醇的物质的量占消耗的
的选择性(甲醇的物质的量占消耗的 的物质的量的百分比)为
的物质的量的百分比)为 (结果保留三位有效数字);该温度下反应I的平衡常数
(结果保留三位有效数字);该温度下反应I的平衡常数
 (
( 为以平衡分压代替平衡浓度表示的平衡常数,列出计算式即可)。
为以平衡分压代替平衡浓度表示的平衡常数,列出计算式即可)。
您最近一年使用:0次
名校
4 . 某反应过程中体系的能量变化如图所示,下列说法不正确的是
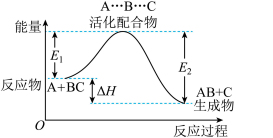

| A.催化剂能改变该反应的焓变 |
| B.该反应的逆反应为吸热反应 |
C.该反应的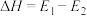 |
| D.若改变某条件时化学反应速率加快,则E1不一定减小 |
您最近一年使用:0次
解题方法
5 . 氢能是一种极具发展潜力的清洁能源,水煤气变换是一种常用的制氢方法,其反应原理为: 。
。
已知:(i)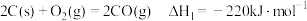
(ii)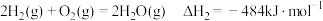
(iii)
(1)反应 的
的
_______  。
。
(2)恒定总压 和水碳比
和水碳比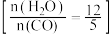 投料,在不同条件下达到平衡时
投料,在不同条件下达到平衡时 和
和 的分压(某成分分压
的分压(某成分分压 总压
总压 该成分的物质的量分数)如下表:
该成分的物质的量分数)如下表:
①在条件1下,水煤气变换反应的分压平衡常数
_______ 。
②对比条件1,条件2中 产率下降是因为发生了一个不涉及
产率下降是因为发生了一个不涉及 的副反应,写出该反应方程式
的副反应,写出该反应方程式_______ 。
(3)科学家在水煤气变换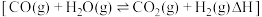 中突破了低温下高转化率与高反应速率不能兼得的难题,该过程是基于双功能催化剂(能吸附不同粒子)催化实现的。该反应历程图如下,其中吸附在催化剂表面的物种用“
中突破了低温下高转化率与高反应速率不能兼得的难题,该过程是基于双功能催化剂(能吸附不同粒子)催化实现的。该反应历程图如下,其中吸附在催化剂表面的物种用“ ”标注,
”标注, 指过渡态,部分产物用球棍模型表示。
指过渡态,部分产物用球棍模型表示。
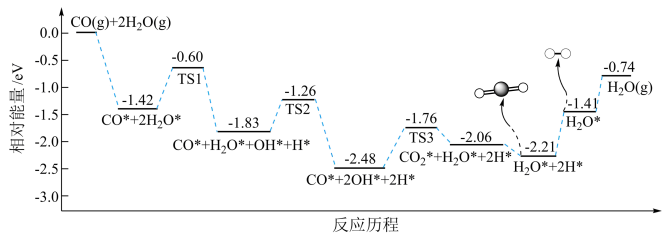
与反应历程对应的微观示意图部分 如下:

①该历程的决速步骤方程式为_______ 。
②下列说法正确的是_______ 。
A.过程Ⅱ既有化学键的断裂也有化学键的形成
B.过程Ⅲ的熵变为零
C.低温下实现高反应速率是因为该催化过程降低了水煤气变换反应的
D.过程 的微观图示为:
的微观图示为: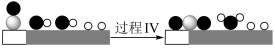
(4)实验发现,其他条件不变,在相同时间内 ,向 反应体系中投入一定量的
反应体系中投入一定量的 可以增大
可以增大 的体积分数,其实验结果如图所示:
的体积分数,其实验结果如图所示:
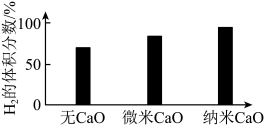
投入等质量的纳米 比微米
比微米 使
使 的体积分数增大的原因可能是
的体积分数增大的原因可能是_______ 。
 。
。已知:(i)
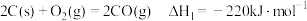
(ii)
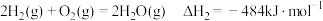
(iii)

(1)反应
 的
的
 。
。(2)恒定总压
 和水碳比
和水碳比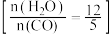 投料,在不同条件下达到平衡时
投料,在不同条件下达到平衡时 和
和 的分压(某成分分压
的分压(某成分分压 总压
总压 该成分的物质的量分数)如下表:
该成分的物质的量分数)如下表: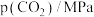 | 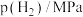 | 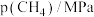 | |
| 条件1 | 0.30 | 0.30 | 0 |
| 条件2 | 0.32 | 0.26 | 0.02 |

②对比条件1,条件2中
 产率下降是因为发生了一个不涉及
产率下降是因为发生了一个不涉及 的副反应,写出该反应方程式
的副反应,写出该反应方程式(3)科学家在水煤气变换
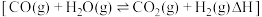 中突破了低温下高转化率与高反应速率不能兼得的难题,该过程是基于双功能催化剂(能吸附不同粒子)催化实现的。该反应历程图如下,其中吸附在催化剂表面的物种用“
中突破了低温下高转化率与高反应速率不能兼得的难题,该过程是基于双功能催化剂(能吸附不同粒子)催化实现的。该反应历程图如下,其中吸附在催化剂表面的物种用“ ”标注,
”标注, 指过渡态,部分产物用球棍模型表示。
指过渡态,部分产物用球棍模型表示。
与反应历程对应的微观示意图

①该历程的决速步骤方程式为
②下列说法正确的是
A.过程Ⅱ既有化学键的断裂也有化学键的形成
B.过程Ⅲ的熵变为零
C.低温下实现高反应速率是因为该催化过程降低了水煤气变换反应的

D.过程
 的微观图示为:
的微观图示为:
(4)实验发现,其他条件不变,在
 反应体系中投入一定量的
反应体系中投入一定量的 可以增大
可以增大 的体积分数,其实验结果如图所示:
的体积分数,其实验结果如图所示:
投入等质量的纳米
 比微米
比微米 使
使 的体积分数增大的原因可能是
的体积分数增大的原因可能是
您最近一年使用:0次
名校
解题方法
6 . 丙烯是一种重要的有机化工原料,人们一直在寻求更为广泛和经济的丙烯来源。以丙烷为原料制备丙烯的部分反应机理如图所示(图中体现了由丙烷制备丙烯的2种历程)。下列说法正确的是
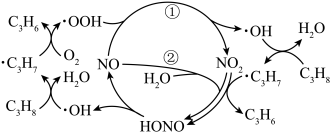

| A.消耗等量的NO时,反应①和②中转移电子的数目相等 |
| B.其他条件相同时,2种反应历程的C3H8的平衡转化率相同 |
C.丙烷制备丙烯的反应为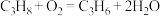 |
| D.反应过程中,N元素呈现的化合价仅有+2价、+4价 |
您最近一年使用:0次
7 . 一定条件下,1-苯基丙炔( ,Ph-表示苯基)可与HCl发生催化加成,反应如下:
,Ph-表示苯基)可与HCl发生催化加成,反应如下:
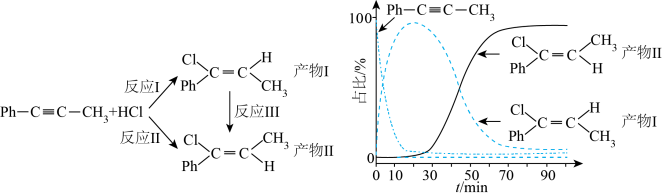
反应过程中该炔烃及反应产物的占比随时间的变化如图(已知:反应I、Ⅲ为放热反应),下列说法正确的是
 ,Ph-表示苯基)可与HCl发生催化加成,反应如下:
,Ph-表示苯基)可与HCl发生催化加成,反应如下:
反应过程中该炔烃及反应产物的占比随时间的变化如图(已知:反应I、Ⅲ为放热反应),下列说法正确的是
| A.相同条件下,产物I比产物Ⅱ稳定 |
| B.反应开始阶段,产物Ⅱ的转化率高 |
| C.一定温度下,增加HCl浓度可增加平衡时产物Ⅱ和产物I的比例 |
| D.相同条件下,生成产物I的活化能更低,生成产物Ⅱ放出的能量更多 |
您最近一年使用:0次
8 . 某反应的能量变化如图所示,下列说法正确的是


| A.过程a的反应速率比过程b快 | B.过程b第一阶段反应的活化能为 |
C.该反应的反应热 | D.该反应为吸热反应 |
您最近一年使用:0次
解题方法
9 . 工业制硫酸的关键反应为
 ,在
,在 存在时,该反应的机理为:i.
存在时,该反应的机理为:i. (快);ii.
(快);ii.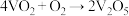 (慢)。下列说法正确的是
(慢)。下列说法正确的是

 ,在
,在 存在时,该反应的机理为:i.
存在时,该反应的机理为:i. (快);ii.
(快);ii.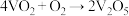 (慢)。下列说法正确的是
(慢)。下列说法正确的是| A.反应i的活化能比反应ii的活化能小 | B.反应i是决速步骤 |
| C.工业生产中应选择低温条件 | D. 是该反应的催化剂 是该反应的催化剂 |
您最近一年使用:0次
10 . 2SO2(g)+O2(g) 2SO3(g)
2SO3(g)  =-198kJ·mol-1,在V2O5存在时,该反应机理为:
=-198kJ·mol-1,在V2O5存在时,该反应机理为:
V2O5+SO2→2VO2+SO3(快)
4VO2+O2→2V2O5(慢)
下列说法正确的是
 2SO3(g)
2SO3(g)  =-198kJ·mol-1,在V2O5存在时,该反应机理为:
=-198kJ·mol-1,在V2O5存在时,该反应机理为:V2O5+SO2→2VO2+SO3(快)
4VO2+O2→2V2O5(慢)
下列说法正确的是
| A.升高温度,逆反应速率增加,正反应速率降低 |
| B.该反应逆反应的活化能大于198kJ·mol-1 |
| C.VO2是该反应的催化剂 |
| D.为提高反应速率,适当增加SO2浓度比适当增加O2浓度效果好 |
您最近一年使用:0次
2024-03-05更新
|
54次组卷
|
2卷引用:浙江省杭州第二中学东河校区2023-2024学年高二上学期期末考试化学试题



