名校
解题方法
1 . 合成氨工艺是人工固氮的重要途径,解决数亿人口生存问题。
(1)已知: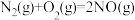
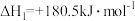




则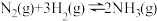 的
的
___________ 。
(2)合成氨反应在催化剂作用下的反应历程为(*表示吸附态):
第一步 ;
; (慢反应)
(慢反应)
第二步 ;
; ;
; (快反应)
(快反应)
第三步 (快反应)
(快反应)
①第一步反应的活化能E1与第二步反应的活化能E2相比:E1>E2,请写出判断理由___________ 。
②下列关于该合成氨工艺的理解正确的是___________ (填标号)。
A.合成氨实际工业生产条件是高温、高压、合适的催化剂
B.当温度、压强一定时,在原料气(N2和H2的比例不变)中添加少量惰性气体,不会改变平衡转化率
C.基于NH3有较强的分子间作用力,可将其液化,不断将液氨移去,有利于提高正反应速率
D.分离空气可得N2,通过天然气和水蒸气转化可得H2,原料气须经过净化处理,以防止催化剂中毒和安全事故发生
(3)在一定条件下,向某反应容器中投入5molN2、15molH2,在不同温度下反应,平衡体系中氨的质量分数随压强变化曲线如图所示:

①温度T1、T2、T3中,最大的是___________ ,M点H2的转化率为___________ 。
②1939年捷姆金和佩热夫推出合成氨反应在接近平衡时净速率方程式为: ,k1、k2分别为正反应和逆反应的速率常数;
,k1、k2分别为正反应和逆反应的速率常数;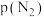 、
、 、
、 代表各组分的分压(分压=总压×物质的量分数);α为常数,工业上以铁为催化剂时,α=0.5。由M点数据计算
代表各组分的分压(分压=总压×物质的量分数);α为常数,工业上以铁为催化剂时,α=0.5。由M点数据计算
___________ MPa-2(保留两位有效数字)。
(4)将N2和H2以一定的流速,分别通过甲、乙两种催化剂进行反应,相同时间内测量逸出气体中N2的含量,从而确定N2的转化率,结果如图所示:
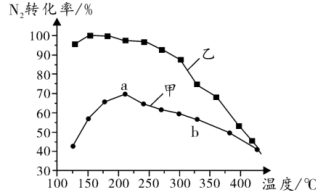
a点___________ (填“是”或“不是”)平衡状态,N2的转化率在a~b段呈现如图变化,可能的原因是___________ 。
(1)已知:
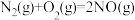
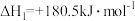




则
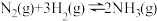 的
的
(2)合成氨反应在催化剂作用下的反应历程为(*表示吸附态):
第一步
 ;
; (慢反应)
(慢反应)第二步
 ;
; ;
; (快反应)
(快反应)第三步
 (快反应)
(快反应)①第一步反应的活化能E1与第二步反应的活化能E2相比:E1>E2,请写出判断理由
②下列关于该合成氨工艺的理解正确的是
A.合成氨实际工业生产条件是高温、高压、合适的催化剂
B.当温度、压强一定时,在原料气(N2和H2的比例不变)中添加少量惰性气体,不会改变平衡转化率
C.基于NH3有较强的分子间作用力,可将其液化,不断将液氨移去,有利于提高正反应速率
D.分离空气可得N2,通过天然气和水蒸气转化可得H2,原料气须经过净化处理,以防止催化剂中毒和安全事故发生
(3)在一定条件下,向某反应容器中投入5molN2、15molH2,在不同温度下反应,平衡体系中氨的质量分数随压强变化曲线如图所示:

①温度T1、T2、T3中,最大的是
②1939年捷姆金和佩热夫推出合成氨反应在接近平衡时净速率方程式为:
 ,k1、k2分别为正反应和逆反应的速率常数;
,k1、k2分别为正反应和逆反应的速率常数;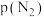 、
、 、
、 代表各组分的分压(分压=总压×物质的量分数);α为常数,工业上以铁为催化剂时,α=0.5。由M点数据计算
代表各组分的分压(分压=总压×物质的量分数);α为常数,工业上以铁为催化剂时,α=0.5。由M点数据计算
(4)将N2和H2以一定的流速,分别通过甲、乙两种催化剂进行反应,相同时间内测量逸出气体中N2的含量,从而确定N2的转化率,结果如图所示:

a点
您最近一年使用:0次
解题方法
2 . 氮的氧化物是造成大气污染的主要物质,研究氮氧化物等大气污染物对建设美丽家乡,打造宜居环境具有重要意义。NO在空气中存在:
 。该反应分两步完成,如图所示。回答下列问题:
。该反应分两步完成,如图所示。回答下列问题:

(1)写出反应①的热化学方程式___________ ( 用含物理量E的等式表示)。
用含物理量E的等式表示)。
(2)反应①和反应②中,一个是快反应,会快速建立平衡,另一个是慢反应。决定 反应速率的是
反应速率的是___________ (填“反应①”或“反应②”)
(3)T1温度,容积为2L恒容密闭容器中发生反应:
 。实验测得:v正=v(NO)消耗=2v(O2)消耗=
。实验测得:v正=v(NO)消耗=2v(O2)消耗= ,v逆=v(NO2)消耗=
,v逆=v(NO2)消耗=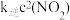 ,k正、k逆为速率常数,只受温度影响。不同时刻测得容器中n(NO)、n(O2)如下表:
,k正、k逆为速率常数,只受温度影响。不同时刻测得容器中n(NO)、n(O2)如下表:
①0~2s内该反应的平均速率v(NO)= ___________  。
。
②T1温度时,化学平衡常数K=___________ (结果保留三位有效数字)。
③若将容器的温度改变为T2时其k正=k逆,则T2___________ T1 (填“>”“=”或“<”)。
(4)工业上利用NH3在催化剂 (V2O5是活性组分)作用下处理NO
(V2O5是活性组分)作用下处理NO
主反应: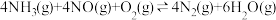

副反应: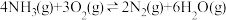

在石英微型反应器中以一定流速通过烟气[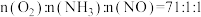 ],不同温度下V2O5的质量分数对单位时间内NO去除率的影响如图所示。
],不同温度下V2O5的质量分数对单位时间内NO去除率的影响如图所示。

①从起始至对应A、B、C三点的平均反应速率由大到小的顺序为___________ 。
②V2O5的质量分数对该催化剂活性的影响是___________ 。
③若烟气中O2含量一定,在催化剂适宜温度范围内,当 时,随着该比值的增大,NO去除率无明显变化,可能的原因是
时,随着该比值的增大,NO去除率无明显变化,可能的原因是___________ 。

 。该反应分两步完成,如图所示。回答下列问题:
。该反应分两步完成,如图所示。回答下列问题:
(1)写出反应①的热化学方程式
 用含物理量E的等式表示)。
用含物理量E的等式表示)。(2)反应①和反应②中,一个是快反应,会快速建立平衡,另一个是慢反应。决定
 反应速率的是
反应速率的是(3)T1温度,容积为2L恒容密闭容器中发生反应:

 。实验测得:v正=v(NO)消耗=2v(O2)消耗=
。实验测得:v正=v(NO)消耗=2v(O2)消耗= ,v逆=v(NO2)消耗=
,v逆=v(NO2)消耗=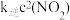 ,k正、k逆为速率常数,只受温度影响。不同时刻测得容器中n(NO)、n(O2)如下表:
,k正、k逆为速率常数,只受温度影响。不同时刻测得容器中n(NO)、n(O2)如下表:| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)/mol | 0.20 | 0.10 | 0.08 | 0.07 | 0.06 | 0.06 |
| n(O2)/mol | 0.10 | 0.05 | 0.04 | 0.035 | 0.03 | 0.03 |
 。
。②T1温度时,化学平衡常数K=
③若将容器的温度改变为T2时其k正=k逆,则T2
(4)工业上利用NH3在催化剂
 (V2O5是活性组分)作用下处理NO
(V2O5是活性组分)作用下处理NO主反应:
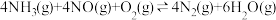

副反应:
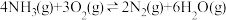

在石英微型反应器中以一定流速通过烟气[
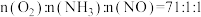 ],不同温度下V2O5的质量分数对单位时间内NO去除率的影响如图所示。
],不同温度下V2O5的质量分数对单位时间内NO去除率的影响如图所示。
①从起始至对应A、B、C三点的平均反应速率由大到小的顺序为
②V2O5的质量分数对该催化剂活性的影响是
③若烟气中O2含量一定,在催化剂适宜温度范围内,当
 时,随着该比值的增大,NO去除率无明显变化,可能的原因是
时,随着该比值的增大,NO去除率无明显变化,可能的原因是
您最近一年使用:0次
名校
解题方法
3 . Ⅰ.合成氨厂和硝酸厂的烟气中含有大量的氮氧化物,脱硝是指将烟气中的氮氧化物转化为无毒无害物质的化学过程。回答下列问题:
(1) 是一种强温室气体,且易形成颗粒性污染物,研究
是一种强温室气体,且易形成颗粒性污染物,研究 O的分解对环境保护有重要意义。碘蒸气的存在能大幅度提高
O的分解对环境保护有重要意义。碘蒸气的存在能大幅度提高 的分解速率,反应历程如下:
的分解速率,反应历程如下:
第一步: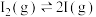 (快反应)
(快反应)
第二步: (慢反应)
(慢反应)
第三步: (快反应)
(快反应)
下列表述正确的是___________ (填标号)。
A.第二步反应是总反应的决速步骤
B. 的分解速率与
的分解速率与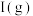 的浓度有关
的浓度有关
C.第二步反应的活化能比第一步反应的小
Ⅱ.在一定条件下,向某密闭容器中加入 、
、 ,在不同温度下发生反应
,在不同温度下发生反应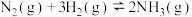
 ,平衡体系中
,平衡体系中 的质量分数随平衡时气体总压强变化的曲线如图所示。
的质量分数随平衡时气体总压强变化的曲线如图所示。
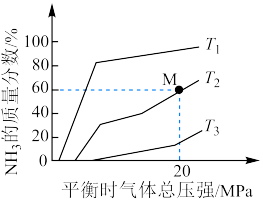
(2) 、
、 、
、 中温度最高的是
中温度最高的是___________ ;若 、
、 时该反应的平衡常数分别为
时该反应的平衡常数分别为 、
、 ,则K1
,则K1___________ (填“<”或“>”) 。
。
(3)M点 的转化率为
的转化率为___________ 。
Ⅲ.若在300℃、体积为2L的恒容密闭容器中,充入2molCO和2molNO,初始压强为 下进行反应
下进行反应 ,反应过程中,总压强随时间的变化关系如图所示。
,反应过程中,总压强随时间的变化关系如图所示。
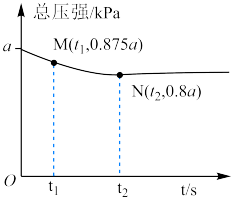
(4)M点时,NO的转化率为___________ ,
___________  。
。
(5)300℃下该反应的平衡常数
___________ 。
(6)平衡后保持其他条件不变,若再充入1.2molCO、1.2mol ,则平衡向
,则平衡向___________ (填“正”或“逆”)反应方向移动。
(1)
 是一种强温室气体,且易形成颗粒性污染物,研究
是一种强温室气体,且易形成颗粒性污染物,研究 O的分解对环境保护有重要意义。碘蒸气的存在能大幅度提高
O的分解对环境保护有重要意义。碘蒸气的存在能大幅度提高 的分解速率,反应历程如下:
的分解速率,反应历程如下:第一步:
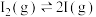 (快反应)
(快反应)第二步:
 (慢反应)
(慢反应)第三步:
 (快反应)
(快反应)下列表述正确的是
A.第二步反应是总反应的决速步骤
B.
 的分解速率与
的分解速率与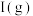 的浓度有关
的浓度有关C.第二步反应的活化能比第一步反应的小
Ⅱ.在一定条件下,向某密闭容器中加入
 、
、 ,在不同温度下发生反应
,在不同温度下发生反应
 ,平衡体系中
,平衡体系中 的质量分数随平衡时气体总压强变化的曲线如图所示。
的质量分数随平衡时气体总压强变化的曲线如图所示。
(2)
 、
、 、
、 中温度最高的是
中温度最高的是 、
、 时该反应的平衡常数分别为
时该反应的平衡常数分别为 、
、 ,则K1
,则K1 。
。(3)M点
 的转化率为
的转化率为Ⅲ.若在300℃、体积为2L的恒容密闭容器中,充入2molCO和2molNO,初始压强为
 下进行反应
下进行反应 ,反应过程中,总压强随时间的变化关系如图所示。
,反应过程中,总压强随时间的变化关系如图所示。
(4)M点时,NO的转化率为

 。
。(5)300℃下该反应的平衡常数

(6)平衡后保持其他条件不变,若再充入1.2molCO、1.2mol
 ,则平衡向
,则平衡向
您最近一年使用:0次
2023-10-05更新
|
19次组卷
|
2卷引用:河北省邢台市四校质检联盟2023-2024学年高二上学期第一次月考化学试题
名校
解题方法
4 . 萘与三氧化硫反应,同时生成α-萘磺酸(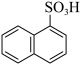 )与β-萘磺酸(
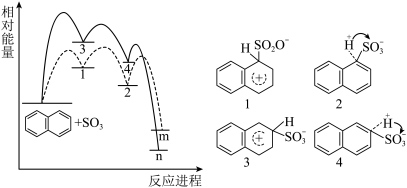
)与β-萘磺酸(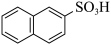 ),反应过程中的能量变化如图所示,1、2、3、4是中间产物,m、n各代表一种产物(已知速率常数k与温度T的关系式为k=A
),反应过程中的能量变化如图所示,1、2、3、4是中间产物,m、n各代表一种产物(已知速率常数k与温度T的关系式为k=A ,其中A、R为常数,Ea为活化能)。下列说法错误的是
,其中A、R为常数,Ea为活化能)。下列说法错误的是
 )与β-萘磺酸(
)与β-萘磺酸( ),反应过程中的能量变化如图所示,1、2、3、4是中间产物,m、n各代表一种产物(已知速率常数k与温度T的关系式为k=A
),反应过程中的能量变化如图所示,1、2、3、4是中间产物,m、n各代表一种产物(已知速率常数k与温度T的关系式为k=A ,其中A、R为常数,Ea为活化能)。下列说法错误的是
,其中A、R为常数,Ea为活化能)。下列说法错误的是
| A.m代表α-萘磺酸,n代表β-萘磺酸 |
| B.稳定性:β-萘磺酸>α-萘磺酸 |
| C.升高相同温度,生成α-萘磺酸的反应速率变化更大 |
| D.平衡时,适当降低温度有利于提高混合物中β-萘磺酸的含量 |
您最近一年使用:0次
名校
解题方法
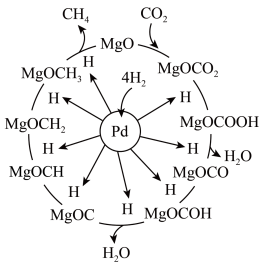
5 .  催化剂上
催化剂上 甲烷化反应机理如图所示,下列说法不正确的是
甲烷化反应机理如图所示,下列说法不正确的是
 催化剂上
催化剂上 甲烷化反应机理如图所示,下列说法不正确的是
甲烷化反应机理如图所示,下列说法不正确的是
A.增大 的浓度,能增大活化分子百分含量,加快反应速率 的浓度,能增大活化分子百分含量,加快反应速率 |
B.整个甲烷化过程真正起催化作用的物质为 和MgO 和MgO |
C.上述甲烷化过程总反应可表示为 |
D.经过一个加氢循环后MgO再次与 结合形成碳酸盐,继续一个新的加氢循环 结合形成碳酸盐,继续一个新的加氢循环 |
您最近一年使用:0次
6 . 为早日实现“双碳”目标,科学家提出以TiO2为催化剂,用光热化学循环分解法减少大气中CO2含量,反应机理如图所示。下列说法正确的是
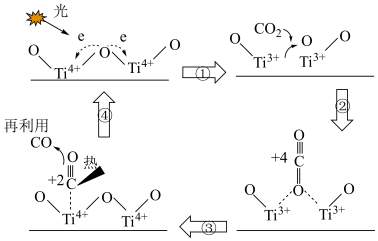

| A.反应过程中只有一种元素化合价发生变化 |
| B.图示中涉及到光能、热能、化学能的转化 |
| C.TiO2在降低了反应活化能的同时,提高了反应物的平衡转化率 |
| D.每分解4.4gCO2能产生3.36L气体 |
您最近一年使用:0次
名校
7 . 环境科学研究发现, 也是一种温室效应气体,与
也是一种温室效应气体,与 相比,虽然
相比,虽然 在大气中的含量很低,增温潜势却是二氧化碳的298倍,对全球气候的增温效应在未来将越来越显著,已引起科学家的极大关注。
在大气中的含量很低,增温潜势却是二氧化碳的298倍,对全球气候的增温效应在未来将越来越显著,已引起科学家的极大关注。 的能量变化如上图所示,则无催化剂条件下该反应的逆反应的活化能为
的能量变化如上图所示,则无催化剂条件下该反应的逆反应的活化能为__________ ;在相同温度和压强下,1mol  和1mol CO经过相同反应时间测得如下实验数据:
和1mol CO经过相同反应时间测得如下实验数据:
试分析在相同温度时,催化剂2催化下 的转化率更高的原因是
的转化率更高的原因是___________ 。
(2)在容积均为1L的密闭容器A(起始500℃,恒温)、B(起始500℃,绝热)两个容器中分别加入0.1mol 、0.4mol CO和相同催化剂。实验测得A、B容器中
、0.4mol CO和相同催化剂。实验测得A、B容器中 的转化率随时间的变化关系如图所示:
的转化率随时间的变化关系如图所示: 的转化率随时间的变化关系是图中的
的转化率随时间的变化关系是图中的___________ 曲线(填“a”或“b”)。
②要缩短b曲线对应容器达到平衡的时间,但不改变 的平衡转化率,在催化剂一定的情况下可采取的措施是
的平衡转化率,在催化剂一定的情况下可采取的措施是___________ (答出一条即可)。
③500℃该反应的化学平衡常数K=___________ (用最简分数表示)。
④实验测定该反应的反应速率 ,
, ,
, 、
、 分别是正、逆反应速率常数,c为物质的量浓度,计算M处的
分别是正、逆反应速率常数,c为物质的量浓度,计算M处的
___________ (保留两位小数)。
 也是一种温室效应气体,与
也是一种温室效应气体,与 相比,虽然
相比,虽然 在大气中的含量很低,增温潜势却是二氧化碳的298倍,对全球气候的增温效应在未来将越来越显著,已引起科学家的极大关注。
在大气中的含量很低,增温潜势却是二氧化碳的298倍,对全球气候的增温效应在未来将越来越显著,已引起科学家的极大关注。
 的能量变化如上图所示,则无催化剂条件下该反应的逆反应的活化能为
的能量变化如上图所示,则无催化剂条件下该反应的逆反应的活化能为 和1mol CO经过相同反应时间测得如下实验数据:
和1mol CO经过相同反应时间测得如下实验数据:| 实验 | 温度/℃ | 催化剂 |  的转化率/% 的转化率/% |
| 实验1 | 400 | 催化剂1 | 9.5 |
| 400 | 催化剂2 | 10.6 | |
| 实验2 | 500 | 催化剂1 | 12.3 |
| 500 | 催化剂2 | 13.5 |
 的转化率更高的原因是
的转化率更高的原因是(2)在容积均为1L的密闭容器A(起始500℃,恒温)、B(起始500℃,绝热)两个容器中分别加入0.1mol
 、0.4mol CO和相同催化剂。实验测得A、B容器中
、0.4mol CO和相同催化剂。实验测得A、B容器中 的转化率随时间的变化关系如图所示:
的转化率随时间的变化关系如图所示:
 的转化率随时间的变化关系是图中的
的转化率随时间的变化关系是图中的②要缩短b曲线对应容器达到平衡的时间,但不改变
 的平衡转化率,在催化剂一定的情况下可采取的措施是
的平衡转化率,在催化剂一定的情况下可采取的措施是③500℃该反应的化学平衡常数K=
④实验测定该反应的反应速率
 ,
, ,
, 、
、 分别是正、逆反应速率常数,c为物质的量浓度,计算M处的
分别是正、逆反应速率常数,c为物质的量浓度,计算M处的
您最近一年使用:0次
8 . 一定条件下,利用 制备
制备 ,反应为①
,反应为① ,过程中发生②
,过程中发生② 和③
和③ 两个副反应,反应历程如图所示,下列说法正确的是
两个副反应,反应历程如图所示,下列说法正确的是
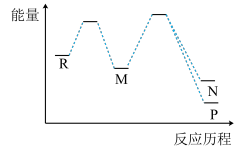
 制备
制备 ,反应为①
,反应为① ,过程中发生②
,过程中发生② 和③
和③ 两个副反应,反应历程如图所示,下列说法正确的是
两个副反应,反应历程如图所示,下列说法正确的是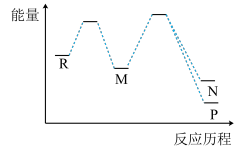
| A.反应③比反应①更快达到平衡 |
| B.温度越高,M的产率一定越高 |
| C.一定时间内,使用合适的催化剂可减少体系中P的含量 |
D.增大R的浓度,反应①②③的 增大、 增大、 减小 减小 |
您最近一年使用:0次
解题方法
9 . 氨气 是一种重要的含氮化合物,目前主要由
是一种重要的含氮化合物,目前主要由 和
和 在高温高压和铁触媒催化作用下合成(哈伯-博施法)。
在高温高压和铁触媒催化作用下合成(哈伯-博施法)。 主要来自煤炭的催化重整。揭示合成氨反应的机理,实现温和条件下制取氨气,一直是化学工作者孜孜以求的目标。研究表明,通入总物质的量一定的
主要来自煤炭的催化重整。揭示合成氨反应的机理,实现温和条件下制取氨气,一直是化学工作者孜孜以求的目标。研究表明,通入总物质的量一定的 和
和 ,合成氨反应在
,合成氨反应在 催化剂上可能通过如图所示机理进行(*表示催化剂表面的吸附位,
催化剂上可能通过如图所示机理进行(*表示催化剂表面的吸附位, 表示被吸附于催化剂表面的
表示被吸附于催化剂表面的 ),其中步骤(ⅱ)是控制总反应速率的步骤。下列相关说法
),其中步骤(ⅱ)是控制总反应速率的步骤。下列相关说法不正确 的是

 是一种重要的含氮化合物,目前主要由
是一种重要的含氮化合物,目前主要由 和
和 在高温高压和铁触媒催化作用下合成(哈伯-博施法)。
在高温高压和铁触媒催化作用下合成(哈伯-博施法)。 主要来自煤炭的催化重整。揭示合成氨反应的机理,实现温和条件下制取氨气,一直是化学工作者孜孜以求的目标。研究表明,通入总物质的量一定的
主要来自煤炭的催化重整。揭示合成氨反应的机理,实现温和条件下制取氨气,一直是化学工作者孜孜以求的目标。研究表明,通入总物质的量一定的 和
和 ,合成氨反应在
,合成氨反应在 催化剂上可能通过如图所示机理进行(*表示催化剂表面的吸附位,
催化剂上可能通过如图所示机理进行(*表示催化剂表面的吸附位, 表示被吸附于催化剂表面的
表示被吸附于催化剂表面的 ),其中步骤(ⅱ)是控制总反应速率的步骤。下列相关说法
),其中步骤(ⅱ)是控制总反应速率的步骤。下列相关说法
| A.在步骤(ⅱ)中,有非极性共价键发生断裂 |
B.在步骤(ⅴ)中,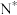 与 与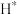 结合生成 结合生成 ,同时释放出1个吸附位 ,同时释放出1个吸附位 |
C.步骤(ⅵ)对应的机理可能为 |
D.其他条件不变时,提高 的含量一定能加快合成氨的速率 的含量一定能加快合成氨的速率 |
您最近一年使用:0次
10 . H2与ICl的反应分两步完成,其能量曲线如图所示。
反应①: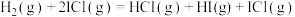


反应②: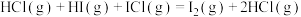


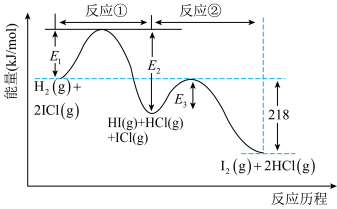
下列有关说法不正确的是
反应①:
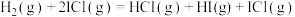


反应②:
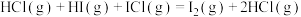



下列有关说法不正确的是
A.反应①的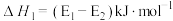 |
B.总反应的活化能为 |
| C.反应过程中,HI在混合气体中的百分含量会先变大再变小 |
D. 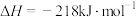  |
您最近一年使用:0次



