名校
解题方法
1 . Ⅰ.合成氨厂和硝酸厂的烟气中含有大量的氮氧化物,脱硝是指将烟气中的氮氧化物转化为无毒无害物质的化学过程。回答下列问题:
(1) 是一种强温室气体,且易形成颗粒性污染物,研究
是一种强温室气体,且易形成颗粒性污染物,研究 O的分解对环境保护有重要意义。碘蒸气的存在能大幅度提高
O的分解对环境保护有重要意义。碘蒸气的存在能大幅度提高 的分解速率,反应历程如下:
的分解速率,反应历程如下:
第一步: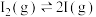 (快反应)
(快反应)
第二步: (慢反应)
(慢反应)
第三步: (快反应)
(快反应)
下列表述正确的是___________ (填标号)。
A.第二步反应是总反应的决速步骤
B. 的分解速率与
的分解速率与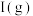 的浓度有关
的浓度有关
C.第二步反应的活化能比第一步反应的小
Ⅱ.在一定条件下,向某密闭容器中加入 、
、 ,在不同温度下发生反应
,在不同温度下发生反应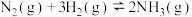
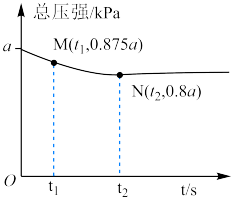
 ,平衡体系中
,平衡体系中 的质量分数随平衡时气体总压强变化的曲线如图所示。
的质量分数随平衡时气体总压强变化的曲线如图所示。
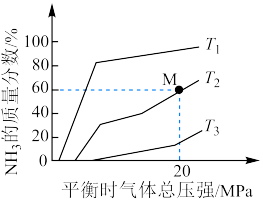
(2) 、
、 、
、 中温度最高的是
中温度最高的是___________ ;若 、
、 时该反应的平衡常数分别为
时该反应的平衡常数分别为 、
、 ,则K1
,则K1___________ (填“<”或“>”) 。
。
(3)M点 的转化率为
的转化率为___________ 。
Ⅲ.若在300℃、体积为2L的恒容密闭容器中,充入2molCO和2molNO,初始压强为 下进行反应
下进行反应 ,反应过程中,总压强随时间的变化关系如图所示。
,反应过程中,总压强随时间的变化关系如图所示。
(4)M点时,NO的转化率为___________ ,
___________  。
。
(5)300℃下该反应的平衡常数
___________ 。
(6)平衡后保持其他条件不变,若再充入1.2molCO、1.2mol ,则平衡向
,则平衡向___________ (填“正”或“逆”)反应方向移动。
(1)
 是一种强温室气体,且易形成颗粒性污染物,研究
是一种强温室气体,且易形成颗粒性污染物,研究 O的分解对环境保护有重要意义。碘蒸气的存在能大幅度提高
O的分解对环境保护有重要意义。碘蒸气的存在能大幅度提高 的分解速率,反应历程如下:
的分解速率,反应历程如下:第一步:
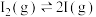 (快反应)
(快反应)第二步:
 (慢反应)
(慢反应)第三步:
 (快反应)
(快反应)下列表述正确的是
A.第二步反应是总反应的决速步骤
B.
 的分解速率与
的分解速率与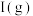 的浓度有关
的浓度有关C.第二步反应的活化能比第一步反应的小
Ⅱ.在一定条件下,向某密闭容器中加入
 、
、 ,在不同温度下发生反应
,在不同温度下发生反应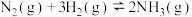
 ,平衡体系中
,平衡体系中 的质量分数随平衡时气体总压强变化的曲线如图所示。
的质量分数随平衡时气体总压强变化的曲线如图所示。
(2)
 、
、 、
、 中温度最高的是
中温度最高的是 、
、 时该反应的平衡常数分别为
时该反应的平衡常数分别为 、
、 ,则K1
,则K1 。
。(3)M点
 的转化率为
的转化率为Ⅲ.若在300℃、体积为2L的恒容密闭容器中,充入2molCO和2molNO,初始压强为
 下进行反应
下进行反应 ,反应过程中,总压强随时间的变化关系如图所示。
,反应过程中,总压强随时间的变化关系如图所示。
(4)M点时,NO的转化率为

 。
。(5)300℃下该反应的平衡常数

(6)平衡后保持其他条件不变,若再充入1.2molCO、1.2mol
 ,则平衡向
,则平衡向
您最近一年使用:0次
2023-10-05更新
|
19次组卷
|
2卷引用:河北省邢台市四校质检联盟2023-2024学年高二上学期第一次月考化学试题
名校
解题方法
2 . 萘与三氧化硫反应,同时生成α-萘磺酸(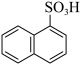 )与β-萘磺酸(
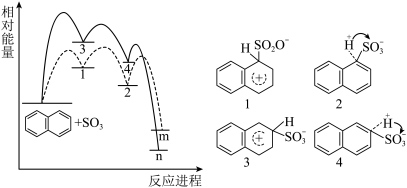
)与β-萘磺酸(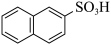 ),反应过程中的能量变化如图所示,1、2、3、4是中间产物,m、n各代表一种产物(已知速率常数k与温度T的关系式为k=A
),反应过程中的能量变化如图所示,1、2、3、4是中间产物,m、n各代表一种产物(已知速率常数k与温度T的关系式为k=A ,其中A、R为常数,Ea为活化能)。下列说法错误的是
,其中A、R为常数,Ea为活化能)。下列说法错误的是
 )与β-萘磺酸(
)与β-萘磺酸( ),反应过程中的能量变化如图所示,1、2、3、4是中间产物,m、n各代表一种产物(已知速率常数k与温度T的关系式为k=A
),反应过程中的能量变化如图所示,1、2、3、4是中间产物,m、n各代表一种产物(已知速率常数k与温度T的关系式为k=A ,其中A、R为常数,Ea为活化能)。下列说法错误的是
,其中A、R为常数,Ea为活化能)。下列说法错误的是
| A.m代表α-萘磺酸,n代表β-萘磺酸 |
| B.稳定性:β-萘磺酸>α-萘磺酸 |
| C.升高相同温度,生成α-萘磺酸的反应速率变化更大 |
| D.平衡时,适当降低温度有利于提高混合物中β-萘磺酸的含量 |
您最近一年使用:0次
3 . 为早日实现“双碳”目标,科学家提出以TiO2为催化剂,用光热化学循环分解法减少大气中CO2含量,反应机理如图所示。下列说法正确的是
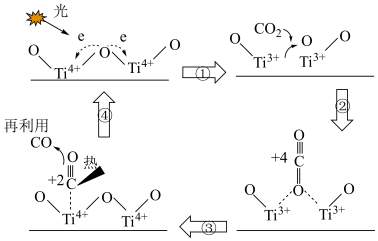

| A.反应过程中只有一种元素化合价发生变化 |
| B.图示中涉及到光能、热能、化学能的转化 |
| C.TiO2在降低了反应活化能的同时,提高了反应物的平衡转化率 |
| D.每分解4.4gCO2能产生3.36L气体 |
您最近一年使用:0次
4 . 一定条件下,利用 制备
制备 ,反应为①
,反应为① ,过程中发生②
,过程中发生② 和③
和③ 两个副反应,反应历程如图所示,下列说法正确的是
两个副反应,反应历程如图所示,下列说法正确的是
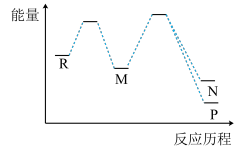
 制备
制备 ,反应为①
,反应为① ,过程中发生②
,过程中发生② 和③
和③ 两个副反应,反应历程如图所示,下列说法正确的是
两个副反应,反应历程如图所示,下列说法正确的是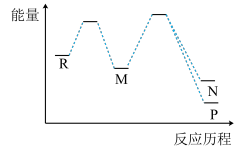
| A.反应③比反应①更快达到平衡 |
| B.温度越高,M的产率一定越高 |
| C.一定时间内,使用合适的催化剂可减少体系中P的含量 |
D.增大R的浓度,反应①②③的 增大、 增大、 减小 减小 |
您最近一年使用:0次
5 . 合成淀粉的重要反应包括二氧化碳制备甲醇的反应,该反应为:CO2(g)+3H2(g) CH3OH(g)+H2O(g)。该反应在有催化剂和无催化剂作用下的反应机理如图所示(其中标有*的为吸附在催化剂表面上的物种,TS为过渡态),下列说法错误的是
CH3OH(g)+H2O(g)。该反应在有催化剂和无催化剂作用下的反应机理如图所示(其中标有*的为吸附在催化剂表面上的物种,TS为过渡态),下列说法错误的是

 CH3OH(g)+H2O(g)。该反应在有催化剂和无催化剂作用下的反应机理如图所示(其中标有*的为吸附在催化剂表面上的物种,TS为过渡态),下列说法错误的是
CH3OH(g)+H2O(g)。该反应在有催化剂和无催化剂作用下的反应机理如图所示(其中标有*的为吸附在催化剂表面上的物种,TS为过渡态),下列说法错误的是
| A.曲线甲中过渡态中TS3最稳定 |
| B.催化剂可使反应历程中决速步骤的活化能降低0.2eV |
| C.化学平衡后,降低温度达新的平衡后甲醇的百分含量会增大 |
| D.图中使用催化剂的曲线是曲线乙 |
您最近一年使用:0次
名校
解题方法
6 . 煤制甲醇工艺是煤高效利用的途径之一,生产工艺如图所示:
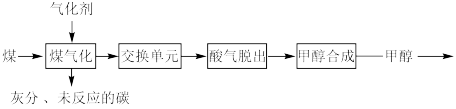
(1)“煤气化”涉及反应:C(s)+2H2O(g)⇌CO2(g)+2H2(g) ΔH=+135 kJ·mol-1,气化剂为H2O(g)和O2(g),关于“煤气化”说法正确的是_______(填序号)。
(2)甲醇合成过程中涉及的主要反应如下:
反应I:CO(g)+2H2(g)⇌CH3OH(g) ΔH1=‒90.94 kJ·mol-1
反应Ⅱ:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ΔH2=‒49.7 kJ·mol-1
反应Ⅲ:CO(g)+H2O(g)⇌CO2(g)+H2(g) ΔH3
①反应Ⅰ在_______ (填“高温”或“低温”)下能自发进行。
②
_______ kJ/mol。
③若要大幅度提高单位时间内反应Ⅱ的选择性,可采取的最佳措施是_______ 。
④反应Ⅲ中,调控反应条件,CO和OH(羟基自由基)在催化剂上相互作用得到CO2和H的氧化还原机理和羒基机理如图所示:

若仅从第一步来看,_______ (填“氧化还原机理”或“羧基机理”)对合成更有利,但最终选择另一反应机理途径的原因是_______ 。
⑤在一定温度下,向2 L刚性容器中充入1 mol CO2和3 mol H2初始压强为3.2MPa,5min后体系达到平衡态,此时容器中含有0.5mol CH3OH和0.3molCO,则5min时,H2O的浓度是_______ mol/L,反应Ⅰ的压强平衡常数Kp为_______ 。

(1)“煤气化”涉及反应:C(s)+2H2O(g)⇌CO2(g)+2H2(g) ΔH=+135 kJ·mol-1,气化剂为H2O(g)和O2(g),关于“煤气化”说法正确的是_______(填序号)。
| A.适量的氧气浓度有利于水煤气的生成 |
| B.适当降低水氧比有利于提高碳的转化率 |
| C.氧气的百分含量越高,对煤气化反应越有利 |
| D.煤气化反应会产生灰分和未反应的碳粉,故煤气化反应过程不适合使用催化剂 |
反应I:CO(g)+2H2(g)⇌CH3OH(g) ΔH1=‒90.94 kJ·mol-1
反应Ⅱ:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ΔH2=‒49.7 kJ·mol-1
反应Ⅲ:CO(g)+H2O(g)⇌CO2(g)+H2(g) ΔH3
①反应Ⅰ在
②

③若要大幅度提高单位时间内反应Ⅱ的选择性,可采取的最佳措施是
④反应Ⅲ中,调控反应条件,CO和OH(羟基自由基)在催化剂上相互作用得到CO2和H的氧化还原机理和羒基机理如图所示:

若仅从第一步来看,
⑤在一定温度下,向2 L刚性容器中充入1 mol CO2和3 mol H2初始压强为3.2MPa,5min后体系达到平衡态,此时容器中含有0.5mol CH3OH和0.3molCO,则5min时,H2O的浓度是
您最近一年使用:0次



