1 . H2与ICl的反应分两步完成,其能量曲线如图所示。
反应①: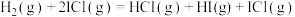


反应②: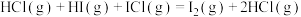


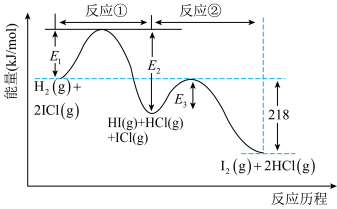
下列有关说法不正确的是
反应①:
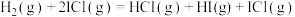


反应②:
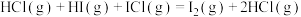



下列有关说法不正确的是
A.反应①的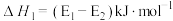 |
B.总反应的活化能为 |
| C.反应过程中,HI在混合气体中的百分含量会先变大再变小 |
D. 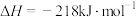  |
您最近一年使用:0次
解题方法
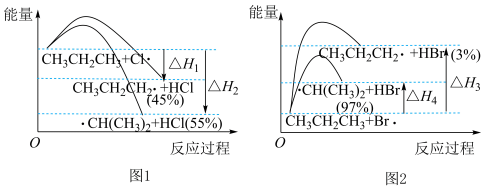
2 . 一定温度下, 的氯化、溴化过程中决速步反应能量图及一段时间后产物的选择性如图所示,下列叙述
的氯化、溴化过程中决速步反应能量图及一段时间后产物的选择性如图所示,下列叙述不正确 的是
 的氯化、溴化过程中决速步反应能量图及一段时间后产物的选择性如图所示,下列叙述
的氯化、溴化过程中决速步反应能量图及一段时间后产物的选择性如图所示,下列叙述
A. |
| B.升高温度,体系中n(1-氯丙烷)与n(2-氯丙烷)的比值增大 |
C.在该温度下,丙烷与体积比1:1的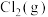 和 和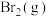 的混合气体反应,产物中2-溴丙烷含量最高 的混合气体反应,产物中2-溴丙烷含量最高 |
| D.以丙烷为原料合成丙醇时,“先溴代再水解”有利于提高2-丙醇的含量 |
您最近一年使用:0次
3 . 自由基是化学键断裂时产生的含未成对电子的中间体,HNO自由基与 反应过程的能量变化如图所示,下列说法正确的是
反应过程的能量变化如图所示,下列说法正确的是
 反应过程的能量变化如图所示,下列说法正确的是
反应过程的能量变化如图所示,下列说法正确的是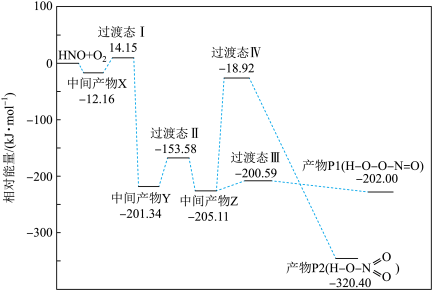
A.反应过程中,产物 的浓度先增大,后减小 的浓度先增大,后减小 |
B.过渡态能量越高,反应的活化能越高,反应的 越小 越小 |
C.其它条件相同,升高温度,达到平衡时,生成的产物中 的百分含量增大 的百分含量增大 |
D.反应过程中,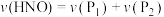 |
您最近一年使用:0次
4 . 自由基是化学键断裂时产生的含未成对电子的中间体,活泼自由基与氧气的反应一直是科研人员的关注点。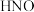 自由基与
自由基与 反应过程的能量变化如图所示,下列说法正确的是
反应过程的能量变化如图所示,下列说法正确的是

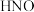 自由基与
自由基与 反应过程的能量变化如图所示,下列说法正确的是
反应过程的能量变化如图所示,下列说法正确的是
| A.反应物的键能总和大于生成物的键能总和 |
B.该历程中最大正反应的活化能 |
C.相同条件下 转化为产物的速率: 转化为产物的速率: |
| D.可以通过选择合适的催化剂,提高产物中P1的含量 |
您最近一年使用:0次
名校
解题方法
5 . 1909年哈伯(P•Haber)在实验室中首次利用氮气与氢气反应合成氨,实现了人工固氮,对人类的生存和发展有着重要意义,因此获得了诺贝尔奖。请回答:
(1)已知:①N2(g)+O2(g) 2NO(g) K(298K)=5×10-31
2NO(g) K(298K)=5×10-31
②N2(g)+3H2(g 2NH3(g) K(298K)=4×106
2NH3(g) K(298K)=4×106
分析以上数据,说明工业固氮选择反应②而非反应①的原因是_____ 。
(2)在铁触媒催化和30MPa下,合成氨反应平衡体系中氨的含量随温度的变化如下表所示。
目前工业实际生产一般选择500℃,其主要原因是_____ 。
(3)化学家GethardErtl证实了氮气与氢气在固体催化剂表面合成氨的过程,示意图如下:

下列说法正确的是_____
(4)在如图密闭容器中充入2molN2和6molH2,固定活塞保持容器体积为5L,在一定温度下催化反应,NH3的物质的量浓度随时间的变化如图所示。求:
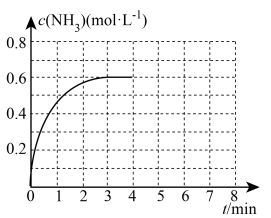
①前3min内平均反应速率:v(H2)=_____ 。
②平衡常数:K=_____ 。
③若在4min时,开启活塞保持恒温恒压,从容器中快速分离出2molNH3,在6min时,反应重新达到化学平衡,在下图1中画出4~8min内氨气的浓度变化曲线_____ 。
(5)我国科学家研制了Ti-H-Fe双温区催化剂(温差达100℃)合成氨,其主反应历程如图所示,其中吸附在催化剂表面上的物种用*标注。
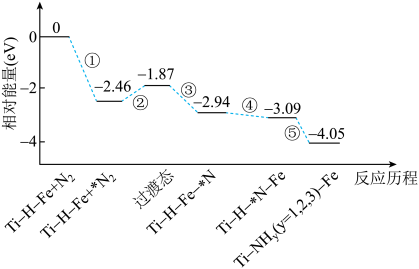
①②③所在Fe区域为_____ 温区(填:高或低),有利于_____ ;
④⑤所在Ti-H区域的温度有利于_____ 。
(1)已知:①N2(g)+O2(g)
 2NO(g) K(298K)=5×10-31
2NO(g) K(298K)=5×10-31②N2(g)+3H2(g
 2NH3(g) K(298K)=4×106
2NH3(g) K(298K)=4×106分析以上数据,说明工业固氮选择反应②而非反应①的原因是
(2)在铁触媒催化和30MPa下,合成氨反应平衡体系中氨的含量随温度的变化如下表所示。
| 温度/℃ | 200 | 300 | 400 | 500 |
| 氨的平衡含量 | 89.9% | 71.0% | 47.0% | 26.4% |
(3)化学家GethardErtl证实了氮气与氢气在固体催化剂表面合成氨的过程,示意图如下:

下列说法正确的是_____
| A.①→②吸附过程放热,有利于化学键的断裂,从而降低反应的活化能 |
| B.整个反应过程中,能量状态最低的是⑤处 |
| C.适时从反应体系中分离出氨气,有利于提高氨的解吸速率 |
| D.氮气和氢气以一定流速通过反应器,是否使用催化剂,对反应物的转化率无影响 |

①前3min内平均反应速率:v(H2)=
②平衡常数:K=
③若在4min时,开启活塞保持恒温恒压,从容器中快速分离出2molNH3,在6min时,反应重新达到化学平衡,在下图1中画出4~8min内氨气的浓度变化曲线
(5)我国科学家研制了Ti-H-Fe双温区催化剂(温差达100℃)合成氨,其主反应历程如图所示,其中吸附在催化剂表面上的物种用*标注。

①②③所在Fe区域为
④⑤所在Ti-H区域的温度有利于
您最近一年使用:0次
6 . 定温度下,丙烷与 、
、 发生氯化和溴化反应方程式及产物含量如下:
发生氯化和溴化反应方程式及产物含量如下:不正确 的是
 、
、 发生氯化和溴化反应方程式及产物含量如下:
发生氯化和溴化反应方程式及产物含量如下:氯化:2CH3CH2CH3+2Cl2
 +2HCl
+2HCl
溴化:2CH3CH2CH3+2Br2
 +2HBr
+2HBr

A.HCl和HBr的键能差为 |
B.丙烷中仲氢(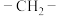 )比伯氢( )比伯氢( )活性强 )活性强 |
| C.升高温度可以提高体系中2-氯丙烷的含量 |
D.反应产物含量主要与 、 、 与 与 反应的活化能相对大小有关 反应的活化能相对大小有关 |
您最近一年使用:0次
7 . 苯与卤素发生取代反应可细分为:
①C6H6(苯)+∙X+X2→C6H5∙+X2+HX △H1
②C6H5∙+X2+HX→C6H5X+HX+∙X △H2
下图1、2表示反应中部分物质的含量(测量反应过程中多个时间点的各物质含量,去除开始时与结束前的极端值后取平均值),已知图1为使用催化剂前,图2为使用催化剂后,下表为相关△H的数据。
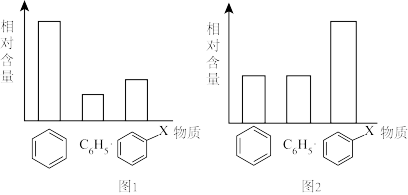
下列说法正确的是
①C6H6(苯)+∙X+X2→C6H5∙+X2+HX △H1
②C6H5∙+X2+HX→C6H5X+HX+∙X △H2
下图1、2表示反应中部分物质的含量(测量反应过程中多个时间点的各物质含量,去除开始时与结束前的极端值后取平均值),已知图1为使用催化剂前,图2为使用催化剂后,下表为相关△H的数据。

X | Cl | Br |
△H1(kJ∙mol-1) | 10 | 20 |
△H2(kJ∙mol-1) | -111 | -100 |
| A.可推知H-Cl键的键能比H-Br键的键能大10 kJ∙mol-1 |
| B.1mol苯与1mol氯气反应将会向环境释放101kJ热量 |
| C.使用催化剂后会改变△H1,但不会改变△H1+△H2 |
| D.反应②为总反应的决速步,催化剂的机理为降低反应②的活化能 |
您最近一年使用:0次
2022-11-10更新
|
586次组卷
|
5卷引用:浙江省普通高校招生2022-2023学年高三上学期10月化学(选考)模拟试题
浙江省普通高校招生2022-2023学年高三上学期10月化学(选考)模拟试题浙江七彩阳光联盟2022-2023学年高二下学期4月期中考试化学试题(已下线)热点情景汇编-专题六 化学反应中的热能(已下线)素养卷03 化学反应与能量变化图象-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)(已下线)考点17 化学反应的热效应(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)
8 . 二氧化碳的资源化利用有助于实现“双碳目标”。
(1)二氧化碳的甲烷化涉及的主要反应有
反应I:
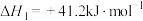
反应II:

反应III:

反应IV:

①结合上述反应,计算可得
_______ 。
②有利于提高体系中 平衡产率的条件是
平衡产率的条件是_______ 。
A.高温高压 B.低温低压 C.高温低压 D.低温高压
(2)二氧化碳的甲醇化:
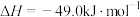 。工业按此法生产甲醇时,通常会向反应体系中加入适量炭粉,可能的理由是
。工业按此法生产甲醇时,通常会向反应体系中加入适量炭粉,可能的理由是_______ 。
(3)二氧化碳催化加氢合成 的过程中,常伴有
的过程中,常伴有 、
、 、CO等副产物。向催化剂中添加某些助剂(助剂也有催化作用)可改变
、CO等副产物。向催化剂中添加某些助剂(助剂也有催化作用)可改变 转化率和反应选择性。其他实验条件一定,不同类型助剂的加入(或不加)在相同反应时间下测得的数据对比如下:
转化率和反应选择性。其他实验条件一定,不同类型助剂的加入(或不加)在相同反应时间下测得的数据对比如下:
若要提升乙烯在产物混合气中的含量及单位时间内的产量,上述助剂中添加_______ 的效果最好,结合过渡态理论分析助剂加入能提高乙烯选择性的原因是_______ 。
(4)如图是含铱-氮配合物的高效水相体系催化二氧化碳还原为甲酸的反应机理:

图中转化涉及到碳原子间 键生成的步骤是
键生成的步骤是_______ (填“①”“②”或“③”)。该化学过程的总反应方程式为_______ 。
(1)二氧化碳的甲烷化涉及的主要反应有
反应I:

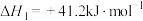
反应II:


反应III:


反应IV:


①结合上述反应,计算可得

②有利于提高体系中
 平衡产率的条件是
平衡产率的条件是A.高温高压 B.低温低压 C.高温低压 D.低温高压
(2)二氧化碳的甲醇化:

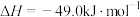 。工业按此法生产甲醇时,通常会向反应体系中加入适量炭粉,可能的理由是
。工业按此法生产甲醇时,通常会向反应体系中加入适量炭粉,可能的理由是(3)二氧化碳催化加氢合成
 的过程中,常伴有
的过程中,常伴有 、
、 、CO等副产物。向催化剂中添加某些助剂(助剂也有催化作用)可改变
、CO等副产物。向催化剂中添加某些助剂(助剂也有催化作用)可改变 转化率和反应选择性。其他实验条件一定,不同类型助剂的加入(或不加)在相同反应时间下测得的数据对比如下:
转化率和反应选择性。其他实验条件一定,不同类型助剂的加入(或不加)在相同反应时间下测得的数据对比如下:| 助剂种类 |  转化率(%) 转化率(%) | 各产物在所有产物中的占比(%) | ||
 |  | 其他 | ||
| 钠型 | 31.6 | 45.8 | 29.7 | 24.5 |
| 钾型 | 27.5 | 75.7 | 22.9 | 1.4 |
| 铜型 | 9.8 | 80.4 | 12.5 | 7.1 |
| 不加 | 12.4 | 37.3 | 25.9 | 36.8 |
若要提升乙烯在产物混合气中的含量及单位时间内的产量,上述助剂中添加
(4)如图是含铱-氮配合物的高效水相体系催化二氧化碳还原为甲酸的反应机理:

图中转化涉及到碳原子间
 键生成的步骤是
键生成的步骤是
您最近一年使用:0次
名校
9 . 下列说法正确的是
A.从 (g)→ (g)→ (l)→ (l)→ (s),熵依次增加 (s),熵依次增加 |
| B.可逆反应都有一定的限度,限度越大反应物的转化率一定越高 |
| C.可逆反应,若总键能:反应物>生成物,则升高温度不利于提高反应物的转化率 |
| D.对于气体反应,其他条件不变,增大压强反应速率加快,与活化分子的百分含量无关 |
您最近一年使用:0次
2021-11-19更新
|
664次组卷
|
7卷引用:浙江省台州市2021-2022学年上学期高三11月选考科目教学质量评估化学试题
浙江省台州市2021-2022学年上学期高三11月选考科目教学质量评估化学试题浙江省嘉兴市2021-2022学年高二上学期期末检测化学试题(已下线)解密09 化学反应速率与化学平衡(分层训练)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)三轮冲刺卷2-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(浙江专用)浙江乐清市知临中学2022-2023学年高二上学期期中考试化学试题黑龙江省哈尔滨师范大学附属中学2022-2023学年高二上学期10月月考化学试题第二章 章末训练
名校
解题方法
10 . 丙烷与溴原子能发生以下两种反应:
① CH3CH2CH3(g) + Br·(g) → CH3CH2CH2·(g) + HBr(g)
② CH3CH2CH3(g) + Br·(g) → CH3CH·CH3 (g) + HBr(g)
反应过程的能量变化如图所示。下列说法正确的是
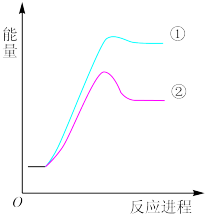
① CH3CH2CH3(g) + Br·(g) → CH3CH2CH2·(g) + HBr(g)
② CH3CH2CH3(g) + Br·(g) → CH3CH·CH3 (g) + HBr(g)
反应过程的能量变化如图所示。下列说法正确的是

| A.反应①是放热反应 |
| B.反应②使用了催化剂 |
| C.产物中 CH3CH2CH2·(g)含量比 CH3CH·CH3(g)低 |
| D.CH3CH2CH2·(g)转变为 CH3CH·CH3(g)时需要吸热 |
您最近一年使用:0次
2020-12-23更新
|
2367次组卷
|
9卷引用:解密08 化学反应与能量(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)
(已下线)解密08 化学反应与能量(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)考点20 化学能与热能-备战2022年高考化学一轮复习考点帮(浙江专用)上海市闵行区2021届高三一模化学试题(已下线)解密08 化学反应与能量(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)考点20 化学能与热能-备战2022年高考化学一轮复习考点帮(全国通用)黑龙江省大庆市实验中学2021-2022学年高三上学期开学考试化学试题2021年辽宁高考化学试题变式题11-19上海市徐汇区2023届高三一模化学试题(已下线)专题12 反应机理和能量变化



