1 . 为早日实现“双碳”目标,科学家提出以TiO2为催化剂,用光热化学循环分解法减少大气中CO2含量,反应机理如图所示。下列说法正确的是
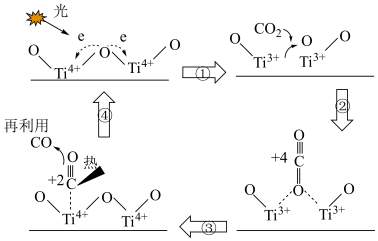

| A.反应过程中只有一种元素化合价发生变化 |
| B.图示中涉及到光能、热能、化学能的转化 |
| C.TiO2在降低了反应活化能的同时,提高了反应物的平衡转化率 |
| D.每分解4.4gCO2能产生3.36L气体 |
您最近一年使用:0次
2 . 合成淀粉的重要反应包括二氧化碳制备甲醇的反应,该反应为:CO2(g)+3H2(g) CH3OH(g)+H2O(g)。该反应在有催化剂和无催化剂作用下的反应机理如图所示(其中标有*的为吸附在催化剂表面上的物种,TS为过渡态),下列说法错误的是
CH3OH(g)+H2O(g)。该反应在有催化剂和无催化剂作用下的反应机理如图所示(其中标有*的为吸附在催化剂表面上的物种,TS为过渡态),下列说法错误的是

 CH3OH(g)+H2O(g)。该反应在有催化剂和无催化剂作用下的反应机理如图所示(其中标有*的为吸附在催化剂表面上的物种,TS为过渡态),下列说法错误的是
CH3OH(g)+H2O(g)。该反应在有催化剂和无催化剂作用下的反应机理如图所示(其中标有*的为吸附在催化剂表面上的物种,TS为过渡态),下列说法错误的是
| A.曲线甲中过渡态中TS3最稳定 |
| B.催化剂可使反应历程中决速步骤的活化能降低0.2eV |
| C.化学平衡后,降低温度达新的平衡后甲醇的百分含量会增大 |
| D.图中使用催化剂的曲线是曲线乙 |
您最近一年使用:0次
名校
解题方法
3 . 催化剂Ⅰ和Ⅱ均能催化反应 ,反应历程如图所示,M为中间产物。其他条件相同时,下列说法不正确的是
,反应历程如图所示,M为中间产物。其他条件相同时,下列说法不正确的是
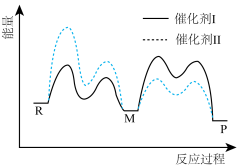
 ,反应历程如图所示,M为中间产物。其他条件相同时,下列说法不正确的是
,反应历程如图所示,M为中间产物。其他条件相同时,下列说法不正确的是
| A.使用Ⅰ和Ⅱ,不影响P的平衡体积百分含量 |
| B.反应达平衡时,升高温度,R的浓度增大 |
| C.使用Ⅰ时,反应体系更快达到平衡 |
| D.使用Ⅱ时,反应过程中M所能达到的最高浓度更大 |
您最近一年使用:0次
2023-11-29更新
|
150次组卷
|
5卷引用:北京师范大学附属实验中学2023-2024学年高二上学期期中考试化学试题
北京师范大学附属实验中学2023-2024学年高二上学期期中考试化学试题 北京师范大学附属实验中学2023-2024学年高二上学期期中考试化学试题北京师范大学附属实验中学2023-2024学年高二上学期期中考试化学试题(已下线)寒假作业02 化学反应速率-【寒假分层作业】2024年高二化学寒假培优练(人教版2019)四川省广安市华蓥中学2023-2024学年高二上学期12月月考化学试题
解题方法
4 . 以某金属氧化物(用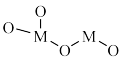 表示)为催化剂,同时消除
表示)为催化剂,同时消除 、NO污染的反应历程如图所示。下列说法错误的是
、NO污染的反应历程如图所示。下列说法错误的是
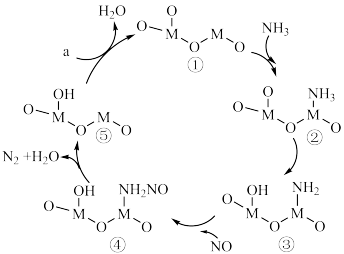
 表示)为催化剂,同时消除
表示)为催化剂,同时消除 、NO污染的反应历程如图所示。下列说法错误的是
、NO污染的反应历程如图所示。下列说法错误的是
A.在相同条件下, 比NO更易与M成键 比NO更易与M成键 |
| B.上述反应历程涉及极性键的断裂和形成 |
| C.通过定量测定发现,反应历程中物质④含量最少,其可能原因是③→④为快反应 |
D.若a为常见非金属单质,则⑤→①的反应可能为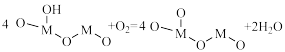 |
您最近一年使用:0次
2023-11-22更新
|
94次组卷
|
2卷引用:江西省赣州市部分学校联考2023-2024学年高三上学期11月期中(一轮总复习调研)化学试题
5 . 下列说法正确的是
| A.增大反应物浓度,有利于提高活化分子的百分含量,使反应加快 |
| B.催化剂能选择性地改变可逆反应正(或逆)反应方向速率,使化学平衡发生移动 |
| C.增大反应物浓度,平衡正向移动,但平衡常数不发生改变 |
| D.用反应的△H或△S均能准确判断一个化学反应能否自发进行 |
您最近一年使用:0次
2023-11-03更新
|
160次组卷
|
2卷引用:四川省成都市彭州市2023-2024学年高二上学期期中考试化学试题
6 . 自由基是化学键断裂时产生的含未成对电子的中间体,活泼自由基与氧气的反应一直是科研人员的关注点。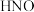 自由基与
自由基与 反应过程的能量变化如图所示,下列说法正确的是
反应过程的能量变化如图所示,下列说法正确的是

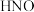 自由基与
自由基与 反应过程的能量变化如图所示,下列说法正确的是
反应过程的能量变化如图所示,下列说法正确的是
| A.反应物的键能总和大于生成物的键能总和 |
B.该历程中最大正反应的活化能 |
C.相同条件下 转化为产物的速率: 转化为产物的速率: |
| D.可以通过选择合适的催化剂,提高产物中P1的含量 |
您最近一年使用:0次
7 . 定温度下,丙烷与 、
、 发生氯化和溴化反应方程式及产物含量如下:
发生氯化和溴化反应方程式及产物含量如下:不正确 的是
 、
、 发生氯化和溴化反应方程式及产物含量如下:
发生氯化和溴化反应方程式及产物含量如下:氯化:2CH3CH2CH3+2Cl2
 +2HCl
+2HCl
溴化:2CH3CH2CH3+2Br2
 +2HBr
+2HBr

A.HCl和HBr的键能差为 |
B.丙烷中仲氢(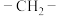 )比伯氢( )比伯氢( )活性强 )活性强 |
| C.升高温度可以提高体系中2-氯丙烷的含量 |
D.反应产物含量主要与 、 、 与 与 反应的活化能相对大小有关 反应的活化能相对大小有关 |
您最近一年使用:0次
名校
解题方法
8 . 煤制甲醇工艺是煤高效利用的途径之一,生产工艺如图所示:
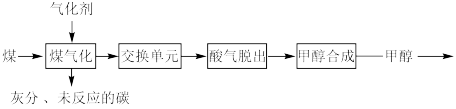
(1)“煤气化”涉及反应:C(s)+2H2O(g)⇌CO2(g)+2H2(g) ΔH=+135 kJ·mol-1,气化剂为H2O(g)和O2(g),关于“煤气化”说法正确的是_______(填序号)。
(2)甲醇合成过程中涉及的主要反应如下:
反应I:CO(g)+2H2(g)⇌CH3OH(g) ΔH1=‒90.94 kJ·mol-1
反应Ⅱ:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ΔH2=‒49.7 kJ·mol-1
反应Ⅲ:CO(g)+H2O(g)⇌CO2(g)+H2(g) ΔH3
①反应Ⅰ在_______ (填“高温”或“低温”)下能自发进行。
②
_______ kJ/mol。
③若要大幅度提高单位时间内反应Ⅱ的选择性,可采取的最佳措施是_______ 。
④反应Ⅲ中,调控反应条件,CO和OH(羟基自由基)在催化剂上相互作用得到CO2和H的氧化还原机理和羒基机理如图所示:

若仅从第一步来看,_______ (填“氧化还原机理”或“羧基机理”)对合成更有利,但最终选择另一反应机理途径的原因是_______ 。
⑤在一定温度下,向2 L刚性容器中充入1 mol CO2和3 mol H2初始压强为3.2MPa,5min后体系达到平衡态,此时容器中含有0.5mol CH3OH和0.3molCO,则5min时,H2O的浓度是_______ mol/L,反应Ⅰ的压强平衡常数Kp为_______ 。

(1)“煤气化”涉及反应:C(s)+2H2O(g)⇌CO2(g)+2H2(g) ΔH=+135 kJ·mol-1,气化剂为H2O(g)和O2(g),关于“煤气化”说法正确的是_______(填序号)。
| A.适量的氧气浓度有利于水煤气的生成 |
| B.适当降低水氧比有利于提高碳的转化率 |
| C.氧气的百分含量越高,对煤气化反应越有利 |
| D.煤气化反应会产生灰分和未反应的碳粉,故煤气化反应过程不适合使用催化剂 |
反应I:CO(g)+2H2(g)⇌CH3OH(g) ΔH1=‒90.94 kJ·mol-1
反应Ⅱ:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ΔH2=‒49.7 kJ·mol-1
反应Ⅲ:CO(g)+H2O(g)⇌CO2(g)+H2(g) ΔH3
①反应Ⅰ在
②

③若要大幅度提高单位时间内反应Ⅱ的选择性,可采取的最佳措施是
④反应Ⅲ中,调控反应条件,CO和OH(羟基自由基)在催化剂上相互作用得到CO2和H的氧化还原机理和羒基机理如图所示:

若仅从第一步来看,
⑤在一定温度下,向2 L刚性容器中充入1 mol CO2和3 mol H2初始压强为3.2MPa,5min后体系达到平衡态,此时容器中含有0.5mol CH3OH和0.3molCO,则5min时,H2O的浓度是
您最近一年使用:0次
9 . 我国提出2060年前实现碳中和,为有效降低大气中 含量,科学家利用
含量,科学家利用 与
与 合成
合成 ,发生反应包含:
,发生反应包含:
Ⅰ主反应: △H
△H
Ⅱ副反应:

回答下列问题:
(1)已知反应Ⅲ
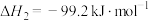 ,则△H=
,则△H=_______ 。相同条件下,C=O键键能为803 ,H-H键键能为436
,H-H键键能为436 ,则
,则
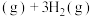 的活化能为
的活化能为_______ 。
(2)我国科学家在发展非金属催化剂实现 电催化还原制备甲醇方向取得重要进展,该反应历程如图所示(部分物质未画出)。
电催化还原制备甲醇方向取得重要进展,该反应历程如图所示(部分物质未画出)。
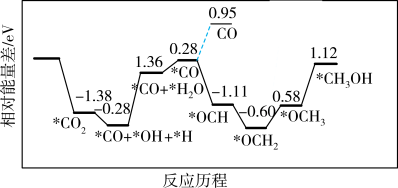
①下列说法正确的是_______ 。
A.催化剂可同时降低主副反应的活化能从而降低反应热
B.副反应所需活化能高于主反应
C. 与
与 结合形成
结合形成
D.反应过程中包含极性键和非极性键的断裂与生成
②要加快合成甲醇的反应速率,主要降低历程中_______ 的能量变化(用历程中符号表示即可,如:( )。
)。
(3)在恒温1L密闭容器中充入4mol 和6mol
和6mol ,初始压强为p,10min时主副反应都达到平衡状态,体系压强为0.8p,测得
,初始压强为p,10min时主副反应都达到平衡状态,体系压强为0.8p,测得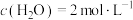 。
。
①0~10min内
_______ 。
②主反应的化学平衡常数
_______ (用含p的代数式表示)。
③平衡时, 的选择性
的选择性_______ ( )。
)。
 含量,科学家利用
含量,科学家利用 与
与 合成
合成 ,发生反应包含:
,发生反应包含:Ⅰ主反应:
 △H
△HⅡ副反应:


回答下列问题:
(1)已知反应Ⅲ

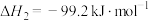 ,则△H=
,则△H= ,H-H键键能为436
,H-H键键能为436 ,则
,则
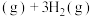 的活化能为
的活化能为(2)我国科学家在发展非金属催化剂实现
 电催化还原制备甲醇方向取得重要进展,该反应历程如图所示(部分物质未画出)。
电催化还原制备甲醇方向取得重要进展,该反应历程如图所示(部分物质未画出)。
①下列说法正确的是
A.催化剂可同时降低主副反应的活化能从而降低反应热
B.副反应所需活化能高于主反应
C.
 与
与 结合形成
结合形成
D.反应过程中包含极性键和非极性键的断裂与生成
②要加快合成甲醇的反应速率,主要降低历程中
 )。
)。(3)在恒温1L密闭容器中充入4mol
 和6mol
和6mol ,初始压强为p,10min时主副反应都达到平衡状态,体系压强为0.8p,测得
,初始压强为p,10min时主副反应都达到平衡状态,体系压强为0.8p,测得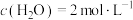 。
。①0~10min内

②主反应的化学平衡常数

③平衡时,
 的选择性
的选择性 )。
)。
您最近一年使用:0次
10 . 苯与卤素发生取代反应可细分为:
①C6H6(苯)+∙X+X2→C6H5∙+X2+HX △H1
②C6H5∙+X2+HX→C6H5X+HX+∙X △H2
下图1、2表示反应中部分物质的含量(测量反应过程中多个时间点的各物质含量,去除开始时与结束前的极端值后取平均值),已知图1为使用催化剂前,图2为使用催化剂后,下表为相关△H的数据。
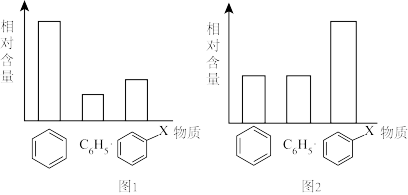
下列说法正确的是
①C6H6(苯)+∙X+X2→C6H5∙+X2+HX △H1
②C6H5∙+X2+HX→C6H5X+HX+∙X △H2
下图1、2表示反应中部分物质的含量(测量反应过程中多个时间点的各物质含量,去除开始时与结束前的极端值后取平均值),已知图1为使用催化剂前,图2为使用催化剂后,下表为相关△H的数据。

X | Cl | Br |
△H1(kJ∙mol-1) | 10 | 20 |
△H2(kJ∙mol-1) | -111 | -100 |
| A.可推知H-Cl键的键能比H-Br键的键能大10 kJ∙mol-1 |
| B.1mol苯与1mol氯气反应将会向环境释放101kJ热量 |
| C.使用催化剂后会改变△H1,但不会改变△H1+△H2 |
| D.反应②为总反应的决速步,催化剂的机理为降低反应②的活化能 |
您最近一年使用:0次
2022-11-10更新
|
586次组卷
|
5卷引用:浙江七彩阳光联盟2022-2023学年高二下学期4月期中考试化学试题
浙江七彩阳光联盟2022-2023学年高二下学期4月期中考试化学试题浙江省普通高校招生2022-2023学年高三上学期10月化学(选考)模拟试题(已下线)热点情景汇编-专题六 化学反应中的热能(已下线)素养卷03 化学反应与能量变化图象-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)(已下线)考点17 化学反应的热效应(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)



