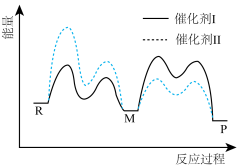
催化剂Ⅰ和Ⅱ均能催化反应 ,反应历程如图所示,M为中间产物。其他条件相同时,下列说法不正确的是
,反应历程如图所示,M为中间产物。其他条件相同时,下列说法不正确的是
 ,反应历程如图所示,M为中间产物。其他条件相同时,下列说法不正确的是
,反应历程如图所示,M为中间产物。其他条件相同时,下列说法不正确的是
| A.使用Ⅰ和Ⅱ,不影响P的平衡体积百分含量 |
| B.反应达平衡时,升高温度,R的浓度增大 |
| C.使用Ⅰ时,反应体系更快达到平衡 |
| D.使用Ⅱ时,反应过程中M所能达到的最高浓度更大 |
23-24高二上·北京西城·期中 查看更多[5]
北京师范大学附属实验中学2023-2024学年高二上学期期中考试化学试题 北京师范大学附属实验中学2023-2024学年高二上学期期中考试化学试题(已下线)寒假作业02 化学反应速率-【寒假分层作业】2024年高二化学寒假培优练(人教版2019)北京师范大学附属实验中学2023-2024学年高二上学期期中考试化学试题四川省广安市华蓥中学2023-2024学年高二上学期12月月考化学试题
更新时间:2023-11-29 18:02:17
|
相似题推荐
【推荐1】反应历程是指化学反应中的反应物转化为最终产物通过的途径。我国学者采用量子力学方法,通过计算机模拟,研究了在钯基催化剂表面上甲醇制氢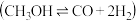 的反应历程,其中吸附在钯催化剂表面上的物种用“
的反应历程,其中吸附在钯催化剂表面上的物种用“ ”标注。如图为计算机模拟的各步反应的能量变化示意图。
”标注。如图为计算机模拟的各步反应的能量变化示意图。

下列说法正确的是
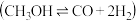 的反应历程,其中吸附在钯催化剂表面上的物种用“
的反应历程,其中吸附在钯催化剂表面上的物种用“ ”标注。如图为计算机模拟的各步反应的能量变化示意图。
”标注。如图为计算机模拟的各步反应的能量变化示意图。
下列说法正确的是
A.甲醇 脱氢反应的第一步历程: 脱氢反应的第一步历程: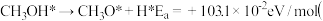 其中 其中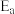 为活化能 为活化能 |
B.由图可知甲醇制氢的反应历程: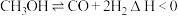 |
C.①②都为 键的断裂过程 键的断裂过程 |
D.该历程中,放热最多的步骤的化学方程式为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法正确的有几项
①活化分子间的碰撞一定能发生化学反应
②普通分子不会发生碰撞
③升高温度会加快反应速率,原因是增加了活化分子的有效碰撞次数
④增大反应物浓度会加快反应速率的原因是单位体积内有效碰撞的次数增多
⑤使用催化剂能加快反应速率,原因是提高了分子的能量,使有效碰撞频率增大
⑥化学反应的实质是活化分子有合适取向时的有效碰撞
①活化分子间的碰撞一定能发生化学反应
②普通分子不会发生碰撞
③升高温度会加快反应速率,原因是增加了活化分子的有效碰撞次数
④增大反应物浓度会加快反应速率的原因是单位体积内有效碰撞的次数增多
⑤使用催化剂能加快反应速率,原因是提高了分子的能量,使有效碰撞频率增大
⑥化学反应的实质是活化分子有合适取向时的有效碰撞
| A.1项 | B.2项 | C.3项 | D.4项 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】反应CO(g)+H2O(g)=CO2(g)+H2(g)在金催化剂表面上的历程如下图所示(吸附在金催化剂表面上的物种用*标注)。

下列说法正确的是

下列说法正确的是
| A.该历程共包括8个基元反应 |
| B.CO(g)和H2O(g)被吸附在催化剂表面时吸收能量 |
| C.决速步骤的化学方程式为H2O*=OH*+H* |
| D.放热最多的步骤只有极性键的断裂与形成 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列装置或操作能达到实验目的的是


| A.图1装置用于中和热的测定 |
| B.图2装置用于高锰酸钾溶液滴定草酸 |
| C.图3装置用于测定氢气的反应速率(单位mL/s) |
| D.图4装置用于研究不同催化剂对反应速率的影响 |
您最近一年使用:0次




