随着我国碳达峰、碳中和目标的确定,二氧化碳资源化利用倍受关注。
I.以 和
和 为原料合成尿素
为原料合成尿素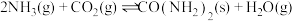
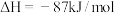 。
。
(1)有利于提高 平衡转化率的措施是___________(填序号)。
平衡转化率的措施是___________(填序号)。
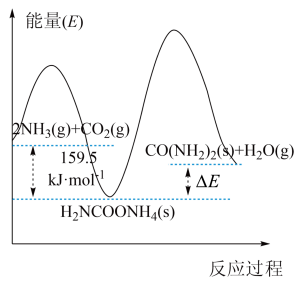
(2)研究发现,合成尿素反应分两步完成,其能量变化如下图所示:
第一步: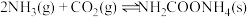

第二步: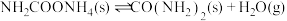


___________  。
。
②决定该反应速率是___________ 反应(填“第一步”或“第二步”),理由是___________ 。
Ⅱ.以和催化重整制备合成气: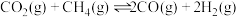 。
。
(3)在密闭容器中通入物质的量均为 的
的 和
和 ,在一定条件下发生反应
,在一定条件下发生反应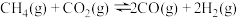 ,
, 的平衡转化率随温度、压强的变化关系如图所示。
的平衡转化率随温度、压强的变化关系如图所示。___________ (填序号)。
A.容器中混合气体的密度保持不变 B.容器内混合气体的压强保持不变
C.反应速率: D.同时断裂
D.同时断裂 键和
键和 键
键
②由图可知,压强
___________  (填“>”“<”或“=”,下同);
(填“>”“<”或“=”,下同); 点速率
点速率
___________ 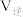 。
。
③已知气体分压=气体总压×气体的物质的量分数,用平衡分压代替平衡浓度可以得到平衡常数 ,则
,则 点对应温度下的
点对应温度下的
___________ (用含 的代数式表示)。
的代数式表示)。
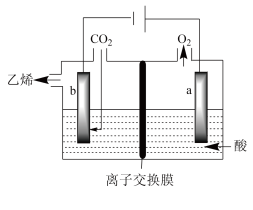
Ⅲ.电化学法还原二氧化碳制乙烯
在强酸性溶液中通入二氧化碳,用惰性电极进行电解可制得乙烯,其原理如图所示:___________ 。
I.以
 和
和 为原料合成尿素
为原料合成尿素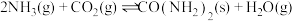
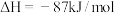 。
。(1)有利于提高
 平衡转化率的措施是___________(填序号)。
平衡转化率的措施是___________(填序号)。| A.高温低压 | B.低温高压 | C.高温高压 | D.低温低压 |
(2)研究发现,合成尿素反应分两步完成,其能量变化如下图所示:
第一步:
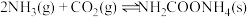

第二步:
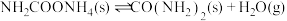


 。
。②决定该反应速率是
Ⅱ.以和催化重整制备合成气:
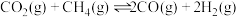 。
。(3)在密闭容器中通入物质的量均为
 的
的 和
和 ,在一定条件下发生反应
,在一定条件下发生反应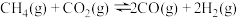 ,
, 的平衡转化率随温度、压强的变化关系如图所示。
的平衡转化率随温度、压强的变化关系如图所示。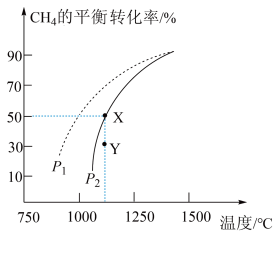
A.容器中混合气体的密度保持不变 B.容器内混合气体的压强保持不变
C.反应速率:
 D.同时断裂
D.同时断裂 键和
键和 键
键②由图可知,压强

 (填“>”“<”或“=”,下同);
(填“>”“<”或“=”,下同); 点速率
点速率
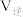 。
。③已知气体分压=气体总压×气体的物质的量分数,用平衡分压代替平衡浓度可以得到平衡常数
 ,则
,则 点对应温度下的
点对应温度下的
 的代数式表示)。
的代数式表示)。Ⅲ.电化学法还原二氧化碳制乙烯
在强酸性溶液中通入二氧化碳,用惰性电极进行电解可制得乙烯,其原理如图所示:
更新时间:2024-04-28 20:32:14
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
【推荐1】水煤气变换反应(CO(g)+H2O(g) CO2(g)+H2(g) )可消除燃料电池原料气流中残留的CO、防止Pt电极中毒,具有重要的工业应用价值。
CO2(g)+H2(g) )可消除燃料电池原料气流中残留的CO、防止Pt电极中毒,具有重要的工业应用价值。
(1)已知:反应 H2(g)+CuO(s)
H2(g)+CuO(s) Cu(s)+H2O(g)
Cu(s)+H2O(g) 
反应 CO(g)+CuO(s)
CO(g)+CuO(s) Cu(s)+CO2(g)
Cu(s)+CO2(g) 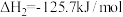
①试计算反应CO(g)+H2O(g) CO2(g)+H2(g)的
CO2(g)+H2(g)的
___________  。
。
②若已知H2O(l)=H2O(g) ΔH = +44 kJ/mol,还可测定___________ 的燃烧热,并通过盖斯定律获得水煤气变换反应的焓变。
(2)水煤气变换反应在金属催化剂上发生的所有主基元反应步骤如下,其中*表示催化剂表面活性位,X*表示金属表面活性位吸附物种。
CO + * CO* (R1) H2O + *
CO* (R1) H2O + *  H2O * (R2) H2O * + *
H2O * (R2) H2O * + * OH* + H* (R3)
OH* + H* (R3)
OH* + * H* + O*(R4) CO* + O *
H* + O*(R4) CO* + O *  CO2* + * (R5) OH* + CO*
CO2* + * (R5) OH* + CO*  COOH* + * (R6)
COOH* + * (R6)
COOH* + * H* + CO2* (R7) H* + CO*
H* + CO2* (R7) H* + CO* CHO* + * (R8) ___________(R9)
CHO* + * (R8) ___________(R9)
HCOO* + * H* + CO2* (R10) 2H*
H* + CO2* (R10) 2H*  H2 * + * (R11)
H2 * + * (R11)
①分析上述基元反应可知水煤气变换反应中CO可通过___________ 种不同的途径氧化成CO2,请写出基元反应 ___________ (R9)。
②下图图a为在纯镍Ni(111)和掺杂P的镍催化剂Ni3P(001)、Ni12P5(001)、NiP2(100)表面上发生H2O * + * OH* + H* 反应的能量分布曲线图。图b为在纯镍Ni(111)和掺杂P的镍催化剂Ni3P(001)、Ni12P5(001)、NiP2(100)表面上发生副基元反应CO * + *
OH* + H* 反应的能量分布曲线图。图b为在纯镍Ni(111)和掺杂P的镍催化剂Ni3P(001)、Ni12P5(001)、NiP2(100)表面上发生副基元反应CO * + * C* + O* 反应的能量分布曲线图。
C* + O* 反应的能量分布曲线图。___________ ,由此可见,最佳催化剂的确定应该是多个研究视角下综合选择的结果。
(3)水煤气变换反应的正逆反应速率可以表示为: ,
,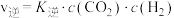 ,
,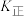 和
和 都是温度的函数。在图中画出
都是温度的函数。在图中画出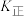 、
、 随温变化的趋势。
随温变化的趋势。___________ ___________ 。
 CO2(g)+H2(g) )可消除燃料电池原料气流中残留的CO、防止Pt电极中毒,具有重要的工业应用价值。
CO2(g)+H2(g) )可消除燃料电池原料气流中残留的CO、防止Pt电极中毒,具有重要的工业应用价值。(1)已知:反应
 H2(g)+CuO(s)
H2(g)+CuO(s) Cu(s)+H2O(g)
Cu(s)+H2O(g) 
反应
 CO(g)+CuO(s)
CO(g)+CuO(s) Cu(s)+CO2(g)
Cu(s)+CO2(g) 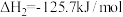
①试计算反应CO(g)+H2O(g)
 CO2(g)+H2(g)的
CO2(g)+H2(g)的
 。
。②若已知H2O(l)=H2O(g) ΔH = +44 kJ/mol,还可测定
(2)水煤气变换反应在金属催化剂上发生的所有主基元反应步骤如下,其中*表示催化剂表面活性位,X*表示金属表面活性位吸附物种。
CO + *
 CO* (R1) H2O + *
CO* (R1) H2O + *  H2O * (R2) H2O * + *
H2O * (R2) H2O * + * OH* + H* (R3)
OH* + H* (R3)OH* + *
 H* + O*(R4) CO* + O *
H* + O*(R4) CO* + O *  CO2* + * (R5) OH* + CO*
CO2* + * (R5) OH* + CO*  COOH* + * (R6)
COOH* + * (R6)COOH* + *
 H* + CO2* (R7) H* + CO*
H* + CO2* (R7) H* + CO* CHO* + * (R8) ___________(R9)
CHO* + * (R8) ___________(R9) HCOO* + *
 H* + CO2* (R10) 2H*
H* + CO2* (R10) 2H*  H2 * + * (R11)
H2 * + * (R11) ①分析上述基元反应可知水煤气变换反应中CO可通过
②下图图a为在纯镍Ni(111)和掺杂P的镍催化剂Ni3P(001)、Ni12P5(001)、NiP2(100)表面上发生H2O * + *
 OH* + H* 反应的能量分布曲线图。图b为在纯镍Ni(111)和掺杂P的镍催化剂Ni3P(001)、Ni12P5(001)、NiP2(100)表面上发生副基元反应CO * + *
OH* + H* 反应的能量分布曲线图。图b为在纯镍Ni(111)和掺杂P的镍催化剂Ni3P(001)、Ni12P5(001)、NiP2(100)表面上发生副基元反应CO * + * C* + O* 反应的能量分布曲线图。
C* + O* 反应的能量分布曲线图。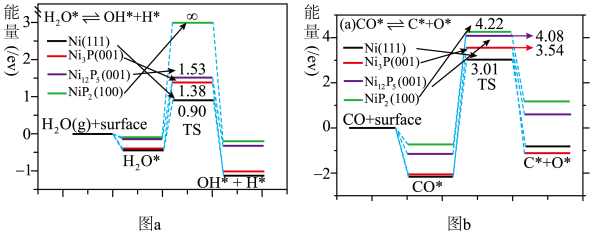
(3)水煤气变换反应的正逆反应速率可以表示为:
 ,
,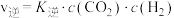 ,
,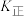 和
和 都是温度的函数。在图中画出
都是温度的函数。在图中画出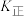 、
、 随温变化的趋势。
随温变化的趋势。
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】氧化亚氮(N2O)是一种强温室气体,且易转换成颗粒污染物。研究氧化亚氮分解对环境保护有重要意义。
(1)污水生物脱氮过程中,在异养微生物催化下,硝酸铵可分解为N2O和另一种产物,该反应的化学方程式为_____ 。
(2)已知反应2N2O(g)=2N2(g)+O2(g)的 ΔH=-163kJ•mol-1,1molN2(g)、1molO2(g)分子中化学键断裂时分别需要吸收945kJ、498kJ的能量,则1molN2O(g)分子中化学键断裂时需要吸收的能量为______ kJ。
(3)在一定温度下的恒容容器中,反应2N2O(g)=2N2(g)+O2(g)的部分实验数据如表:
①在0~20min时段,反应速率v(N2O)为______ mol L-1
L-1 min-1。
min-1。
②若N2O起始浓度c0为0.150mol L-1,则反应至30min时N2O的转化率α=
L-1,则反应至30min时N2O的转化率α=______ 。比较不同起始浓度时N2O的分解速率:v(c0=0.1500mol L-1)
L-1)______ v(c0=0.1000mol L-1)(填“>”、“=”或“<”)。
L-1)(填“>”、“=”或“<”)。
③不同温度(T)下,N2O分解半衰期随起始压强的变化关系如图所示(图中半衰期指任一浓度N2O消耗一半时所需的相应时间),则T1______ T2(填“>”、“=”或“<”)。当温度为T1、起始压强为p0,反应至t1min时,体系压强p=_____ (用p0表示)。

(4)碘蒸气存在能大幅度提高N2O的分解速率,反应历程为:
第一步:I2(g) 2I(g)(快反应)
2I(g)(快反应)
第二步:I(g)+N2O(g) N2(g)+IO(g)(慢反应)
N2(g)+IO(g)(慢反应)
第三步:IO(g)+N2O(g) N2(g)+O2(g)+I(g)(快反应)
N2(g)+O2(g)+I(g)(快反应)
实验表明,含碘时N2O分解速率方程v=k•c(N2O)•[c(I2)]0.5(k为速率常数)。下列表述正确的是_____ (填标号)。
(1)污水生物脱氮过程中,在异养微生物催化下,硝酸铵可分解为N2O和另一种产物,该反应的化学方程式为
(2)已知反应2N2O(g)=2N2(g)+O2(g)的 ΔH=-163kJ•mol-1,1molN2(g)、1molO2(g)分子中化学键断裂时分别需要吸收945kJ、498kJ的能量,则1molN2O(g)分子中化学键断裂时需要吸收的能量为
(3)在一定温度下的恒容容器中,反应2N2O(g)=2N2(g)+O2(g)的部分实验数据如表:
| 反应时间/min | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
| c(N2O)/mol/L | 0.10 | 0.09 | 0.08 | 0.07 | 0.06 | 0.05 | 0.04 | 0.03 | 0.02 | 0.01 | 0.01 |
 L-1
L-1 min-1。
min-1。②若N2O起始浓度c0为0.150mol
 L-1,则反应至30min时N2O的转化率α=
L-1,则反应至30min时N2O的转化率α= L-1)
L-1) L-1)(填“>”、“=”或“<”)。
L-1)(填“>”、“=”或“<”)。③不同温度(T)下,N2O分解半衰期随起始压强的变化关系如图所示(图中半衰期指任一浓度N2O消耗一半时所需的相应时间),则T1

(4)碘蒸气存在能大幅度提高N2O的分解速率,反应历程为:
第一步:I2(g)
 2I(g)(快反应)
2I(g)(快反应)第二步:I(g)+N2O(g)
 N2(g)+IO(g)(慢反应)
N2(g)+IO(g)(慢反应)第三步:IO(g)+N2O(g)
 N2(g)+O2(g)+I(g)(快反应)
N2(g)+O2(g)+I(g)(快反应)实验表明,含碘时N2O分解速率方程v=k•c(N2O)•[c(I2)]0.5(k为速率常数)。下列表述正确的是
| A.N2O分解反应中,k(含碘)>k(无碘) |
| B.第一步对总反应速率起决定作用 |
| C.第二步活化能比第三步大 |
| D.I2浓度与N2O分解速率无关 |
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】氮氧化物治理是环境学家研究的热点之一。回答下列问题:
(1)H2还原法
已知:H2在催化剂Rh表面还原NO的部分反应机理如下表所示。
基元反应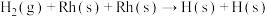 的焓变△H=
的焓变△H=_________ 。
(2)CO还原法
已知: 的速率方程为
的速率方程为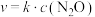 ,k为速率常数,只与温度有关。
,k为速率常数,只与温度有关。
①画出未达平衡时 随时间t的变化关系趋势图
随时间t的变化关系趋势图_________ 。
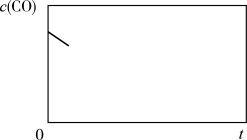
②为提高该反应的化学反应速率,可采取的措施是_________ (填字母序号)。
A.升温 B.恒压时,再充入N2 C.恒容时,再充入CO D.恒压时,再充入N2O
(3)CH4还原法在2L密闭恒容容器中分别加入0.50mol CH4和1.2molNO2,发生反应:
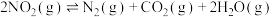 。测得不同温度下
。测得不同温度下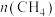 随反应时间t的变化如下表所示。
随反应时间t的变化如下表所示。
①T1温度下,0~20min内,NO2降解速率为_________ 。
②T1_________ T2 (填“>”“<”或“=”),该反应为反应_________ (填“吸热”或“放热”)。
③设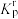 为相对压力平衡常数,其表达式写法:在浓度平衡常数表达式中,用相对分压代替浓度。气体的相对分压等于其分压(单位为kPa)除以
为相对压力平衡常数,其表达式写法:在浓度平衡常数表达式中,用相对分压代替浓度。气体的相对分压等于其分压(单位为kPa)除以 。已知T2温度下,反应达平衡时,CH4的分压为akPa。则T2温度时,该反应的相对压力平衡常数
。已知T2温度下,反应达平衡时,CH4的分压为akPa。则T2温度时,该反应的相对压力平衡常数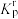 =
=_________ 。
(1)H2还原法
已知:H2在催化剂Rh表面还原NO的部分反应机理如下表所示。
| 序号 | 基元反应 | 活化能Ea/( kJ∙mol-1) |
| ① | 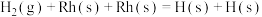 | 12.6 |
| ② | 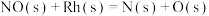 | 97.5 |
| ③ |  | 83.7 |
| ④ |  | 33.5 |
| ⑤ | 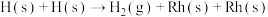 | 77.8 |
基元反应
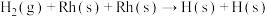 的焓变△H=
的焓变△H=(2)CO还原法
已知:
 的速率方程为
的速率方程为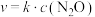 ,k为速率常数,只与温度有关。
,k为速率常数,只与温度有关。①画出未达平衡时
 随时间t的变化关系趋势图
随时间t的变化关系趋势图
②为提高该反应的化学反应速率,可采取的措施是
A.升温 B.恒压时,再充入N2 C.恒容时,再充入CO D.恒压时,再充入N2O
(3)CH4还原法在2L密闭恒容容器中分别加入0.50mol CH4和1.2molNO2,发生反应:

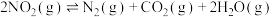 。测得不同温度下
。测得不同温度下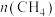 随反应时间t的变化如下表所示。
随反应时间t的变化如下表所示。| 温度K | 时间t/min | 0 | 10 | 20 | 40 | 50 |
| T1 | n(CH4)/mol | 0.50 | 0.30 | 0.18 | 0.15 | 0.15 |
| T2 | n(CH4)/mol | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
①T1温度下,0~20min内,NO2降解速率为
②T1
③设
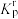 为相对压力平衡常数,其表达式写法:在浓度平衡常数表达式中,用相对分压代替浓度。气体的相对分压等于其分压(单位为kPa)除以
为相对压力平衡常数,其表达式写法:在浓度平衡常数表达式中,用相对分压代替浓度。气体的相对分压等于其分压(单位为kPa)除以 。已知T2温度下,反应达平衡时,CH4的分压为akPa。则T2温度时,该反应的相对压力平衡常数
。已知T2温度下,反应达平衡时,CH4的分压为akPa。则T2温度时,该反应的相对压力平衡常数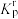 =
=
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】空间站 还原转化系统能把呼出的
还原转化系统能把呼出的 捕集、分离并与空间站电解水系统产生的
捕集、分离并与空间站电解水系统产生的 进行加氢处理,从而实现空间站内物料的循环利用。
进行加氢处理,从而实现空间站内物料的循环利用。
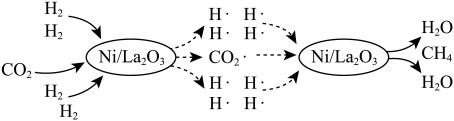
(1)一种借助光将 转化为
转化为 的催化机理如图所示。该转化过程总反应的化学方程式是
的催化机理如图所示。该转化过程总反应的化学方程式是_______ ;图中所示的各物质中,含有极性共价键的非极性分子是_______ (填化学式)。
(2)一定条件下, 和
和 还可发生如下两个平行反应:
还可发生如下两个平行反应:
i.

ii.
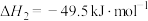
①已知相关键能数据如下表:
则反应i的
_______  。
。
②为了提高 的产率,理论上应采用的措施是
的产率,理论上应采用的措施是_______ (填标号)。
A.低温低压 B.高温低压 C.高温高压 D.低温高压
③保持温度 ,压强
,压强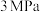 ,按投料比
,按投料比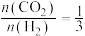 向密闭容器中充入
向密闭容器中充入 和
和 ,反应相同时间测得不同催化剂下
,反应相同时间测得不同催化剂下 转化率和
转化率和 选择性的相关实验数据如下表所示(已知
选择性的相关实验数据如下表所示(已知 选择性:转化的
选择性:转化的 中生成
中生成 的百分比)。
的百分比)。
上述条件下,使用cat.2作催化剂,下列说法能判断反应ii达到平衡状态的是_______ (填标号)。
A.气体压强不再变化 B.气体平均相对分子质量不再变化
C. 和
和 的物质的量之比为
的物质的量之比为 D.
D. 和
和 的物质的量之比不再变化
的物质的量之比不再变化
(3)一定条件下,向 恒容密闭容器中充入
恒容密闭容器中充入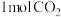 和
和 ,只发生上述反应ii,达平衡时,
,只发生上述反应ii,达平衡时, 的转化率为80%,则该温度下的平衡常数
的转化率为80%,则该温度下的平衡常数
_______ (保留两位小数)。
(4)若恒容密闭容器中只发生上述反应i,在进气比 不同、温度不同时,测得相应的
不同、温度不同时,测得相应的 平衡转化率如图所示。则B和D两点的温度
平衡转化率如图所示。则B和D两点的温度
_______ 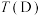 (填“<”,“>”,或“=”),其原因是
(填“<”,“>”,或“=”),其原因是_______ 。

 还原转化系统能把呼出的
还原转化系统能把呼出的 捕集、分离并与空间站电解水系统产生的
捕集、分离并与空间站电解水系统产生的 进行加氢处理,从而实现空间站内物料的循环利用。
进行加氢处理,从而实现空间站内物料的循环利用。(1)一种借助光将
 转化为
转化为 的催化机理如图所示。该转化过程总反应的化学方程式是
的催化机理如图所示。该转化过程总反应的化学方程式是
(2)一定条件下,
 和
和 还可发生如下两个平行反应:
还可发生如下两个平行反应:i.


ii.

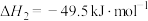
①已知相关键能数据如下表:
| 化学键 |  |  |  |  |
键能/ | 436 | 464 | 803 | 1072 |

 。
。②为了提高
 的产率,理论上应采用的措施是
的产率,理论上应采用的措施是A.低温低压 B.高温低压 C.高温高压 D.低温高压
③保持温度
 ,压强
,压强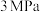 ,按投料比
,按投料比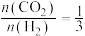 向密闭容器中充入
向密闭容器中充入 和
和 ,反应相同时间测得不同催化剂下
,反应相同时间测得不同催化剂下 转化率和
转化率和 选择性的相关实验数据如下表所示(已知
选择性的相关实验数据如下表所示(已知 选择性:转化的
选择性:转化的 中生成
中生成 的百分比)。
的百分比)。| 催化剂 |  转化率 转化率 |  选择性 选择性 |
| cat.1 | 21.9% | 67.3% |
| cat.2 | 36.1% | 100.0% |
A.气体压强不再变化 B.气体平均相对分子质量不再变化
C.
 和
和 的物质的量之比为
的物质的量之比为 D.
D. 和
和 的物质的量之比不再变化
的物质的量之比不再变化(3)一定条件下,向
 恒容密闭容器中充入
恒容密闭容器中充入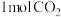 和
和 ,只发生上述反应ii,达平衡时,
,只发生上述反应ii,达平衡时, 的转化率为80%,则该温度下的平衡常数
的转化率为80%,则该温度下的平衡常数
(4)若恒容密闭容器中只发生上述反应i,在进气比
 不同、温度不同时,测得相应的
不同、温度不同时,测得相应的 平衡转化率如图所示。则B和D两点的温度
平衡转化率如图所示。则B和D两点的温度
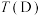 (填“<”,“>”,或“=”),其原因是
(填“<”,“>”,或“=”),其原因是
您最近半年使用:0次
【推荐2】异丁烷(用i-C4H10表示)与CO2耦合脱氢制备异丁烯(用i-C4H8表示),涉及的主要反应有:
反应1 i-C4H10(g) i-C4H8(g) +H2(g) ΔH1
i-C4H8(g) +H2(g) ΔH1
反应2 CO2(g) +H2(g) CO(g) + H2O(g) ΔH2
CO(g) + H2O(g) ΔH2
反应3 i- C4H10(g)+ CO2(g) i-C4H8(g)+CO(g)+ H2O(g) ΔH3
i-C4H8(g)+CO(g)+ H2O(g) ΔH3
反应4 i-C4H10(g)+9CO2(g) 5H2O(g)+13CO(g) ΔH4 ( 副反应)
5H2O(g)+13CO(g) ΔH4 ( 副反应)
回答下列问题:
(1) 已知i-C4H10(g)、i-C4H8(g)、 H2(g)的燃烧热分别为ΔHa、ΔHb、ΔHc, 则 ΔH1=____________ (用ΔHa、ΔHb、ΔHc表示),ΔH3 =___________ (用ΔH1、ΔH2表示)。
(2)一定条件下,若向体积为V L的恒容密闭容器中通入2mol i-C4H10和2 mol CO2,发生上述反应1 ~反应4,t min后测得i- C4H10的物质的量为0.6 mol,则反应体系中0~t min 内异丁烷的平均反应速率v(i – C4H10)=___________ 。
(3)投料比n(CO2) :n(i-C4H10)=1 : 1时,经过化学热力学模拟计算,反应1、反应3、反应4的i- C4H10平衡转化率分别与反应温度的关系如图所示。
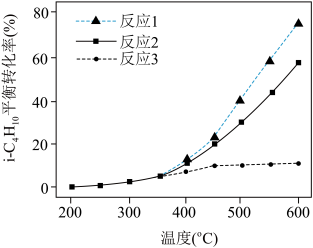
①判断ΔH3___________ 0 (填“>”“<”或“=”);温度越高,越有利于发生___ (填“反应1”“反应3”或“反应4”)。
②反应4(副反应)中,温度高于450 ℃时,i- C4H10的平衡转化率较小且增加幅度放缓,说明温度升高,该副反应也不会过度进行,试分析其原因_______ ;该副反应中i-C4H10平衡转化率的极限最大值为_________ 。
③综合考虑各种因素,提高异丁烯(i- C4H8)平衡产率适宜采取下列措施中的____ (填标号)。
a 适当升高温度 b 适当减小压强
c 尽量增大n(CO2) :n(i-C4H10) d 用更高效的催化剂
反应1 i-C4H10(g)
 i-C4H8(g) +H2(g) ΔH1
i-C4H8(g) +H2(g) ΔH1反应2 CO2(g) +H2(g)
 CO(g) + H2O(g) ΔH2
CO(g) + H2O(g) ΔH2反应3 i- C4H10(g)+ CO2(g)
 i-C4H8(g)+CO(g)+ H2O(g) ΔH3
i-C4H8(g)+CO(g)+ H2O(g) ΔH3反应4 i-C4H10(g)+9CO2(g)
 5H2O(g)+13CO(g) ΔH4 ( 副反应)
5H2O(g)+13CO(g) ΔH4 ( 副反应)回答下列问题:
(1) 已知i-C4H10(g)、i-C4H8(g)、 H2(g)的燃烧热分别为ΔHa、ΔHb、ΔHc, 则 ΔH1=
(2)一定条件下,若向体积为V L的恒容密闭容器中通入2mol i-C4H10和2 mol CO2,发生上述反应1 ~反应4,t min后测得i- C4H10的物质的量为0.6 mol,则反应体系中0~t min 内异丁烷的平均反应速率v(i – C4H10)=
(3)投料比n(CO2) :n(i-C4H10)=1 : 1时,经过化学热力学模拟计算,反应1、反应3、反应4的i- C4H10平衡转化率分别与反应温度的关系如图所示。

①判断ΔH3
②反应4(副反应)中,温度高于450 ℃时,i- C4H10的平衡转化率较小且增加幅度放缓,说明温度升高,该副反应也不会过度进行,试分析其原因
③综合考虑各种因素,提高异丁烯(i- C4H8)平衡产率适宜采取下列措施中的
a 适当升高温度 b 适当减小压强
c 尽量增大n(CO2) :n(i-C4H10) d 用更高效的催化剂
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】甲烷在日常生活及有机合成中用途广泛,某实验小组研究甲烷在高温下气相裂解反应的原理及其应用。
已知:①CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH1=-890.3kJ·mol-1
②C2H4(g)+3O2(g)=2CO2(g)+2H2O(l) ΔH2=-1323.8kJ·mol-1
③2H2(g)+O2(g)=2H2O(l) ΔH3=-571.6kJ·mol-1
(1)裂解反应2CH4(g)⇌C2H4(g)+2H2(g)的ΔH=______ kJ·mol-1。
(2)在某密闭容器中投入1molCH4(g),在不同条件下发生反应:2CH4(g)⇌C2H4(g)+2H2(g)。实验测得平衡时C2H4(g)的物质的量随温度、压强的变化如图1所示。_______ ,温度:T1____ (填“>”、“<”或“=”)T2。
②M、N、Q三点的平衡常数由大到小的顺序为_______________ 。
③M点对应的压强平衡常数Kp=________________ (以分压表示,分压=总压×物质的量分数)。
④若在某密闭容器中充入2molH2、a(a>0)molC2H4和2molCH4,在T1K、p1kPa下进行上述反应。为了使该反应逆向进行,a的范围为_____________________ 。
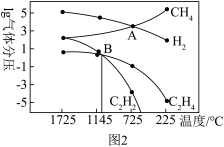
(3)该实验小组在研究过程中得出固体表面催化裂解甲烷时,几种气体平衡时分压(Pa)与温度(°C)的关系如图2所示。______________ 。
已知:①CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH1=-890.3kJ·mol-1
②C2H4(g)+3O2(g)=2CO2(g)+2H2O(l) ΔH2=-1323.8kJ·mol-1
③2H2(g)+O2(g)=2H2O(l) ΔH3=-571.6kJ·mol-1
(1)裂解反应2CH4(g)⇌C2H4(g)+2H2(g)的ΔH=
(2)在某密闭容器中投入1molCH4(g),在不同条件下发生反应:2CH4(g)⇌C2H4(g)+2H2(g)。实验测得平衡时C2H4(g)的物质的量随温度、压强的变化如图1所示。

②M、N、Q三点的平衡常数由大到小的顺序为
③M点对应的压强平衡常数Kp=
④若在某密闭容器中充入2molH2、a(a>0)molC2H4和2molCH4,在T1K、p1kPa下进行上述反应。为了使该反应逆向进行,a的范围为
(3)该实验小组在研究过程中得出固体表面催化裂解甲烷时,几种气体平衡时分压(Pa)与温度(°C)的关系如图2所示。
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】苯乙烯( )是合成树脂、离子交换树脂及合成橡胶等的重要单体。目前生产苯乙烯的主要方法是乙苯催化脱氢法,其反应原理为:
)是合成树脂、离子交换树脂及合成橡胶等的重要单体。目前生产苯乙烯的主要方法是乙苯催化脱氢法,其反应原理为:
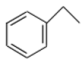 (g)
(g)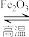
 (g)+H2(g)∆H2=+120kJ∙mol-1
(g)+H2(g)∆H2=+120kJ∙mol-1
(1)其他条件不变时,升高反应温度,乙苯的转化率___________ ,反应速率___________ 。(填“增大”“减小”或“不变”)。
(2)通入水蒸气可延缓催化剂 被还原而失活,其原因是
被还原而失活,其原因是______ (用化学平衡原理解释)。
(3)一定条件下,在体积不变的密闭容器中上述反应达到平衡,在t1时刻加入 ,t2时刻反应再次达到平衡,反应过程中各物质浓度随时间变化的关系如图所示。
,t2时刻反应再次达到平衡,反应过程中各物质浓度随时间变化的关系如图所示。
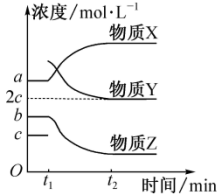
①物质X为___________ (填名称),判断理由是___________ 。
②t2时刻,苯乙烯的浓度为___________ 。
③ 时间内,乙苯的反应速率为
时间内,乙苯的反应速率为___________ 。
 )是合成树脂、离子交换树脂及合成橡胶等的重要单体。目前生产苯乙烯的主要方法是乙苯催化脱氢法,其反应原理为:
)是合成树脂、离子交换树脂及合成橡胶等的重要单体。目前生产苯乙烯的主要方法是乙苯催化脱氢法,其反应原理为: (g)
(g)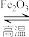
 (g)+H2(g)∆H2=+120kJ∙mol-1
(g)+H2(g)∆H2=+120kJ∙mol-1(1)其他条件不变时,升高反应温度,乙苯的转化率
(2)通入水蒸气可延缓催化剂
 被还原而失活,其原因是
被还原而失活,其原因是(3)一定条件下,在体积不变的密闭容器中上述反应达到平衡,在t1时刻加入
 ,t2时刻反应再次达到平衡,反应过程中各物质浓度随时间变化的关系如图所示。
,t2时刻反应再次达到平衡,反应过程中各物质浓度随时间变化的关系如图所示。
①物质X为
②t2时刻,苯乙烯的浓度为
③
 时间内,乙苯的反应速率为
时间内,乙苯的反应速率为
您最近半年使用:0次
【推荐2】已知某密闭容器中存在可逆反应2CO(g)+4H2(g) =CH3CH2OH(g)+H2O(g) ΔH。测得其他条件相同时,CO的平衡转化率随着温度(T)、压强(p)的变化如图1中曲线所示, 平衡常数K与温度关系如图2所示。
回答下列问题:
图1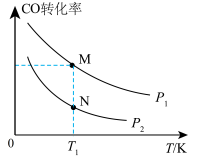 图2
图2 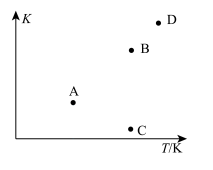
(1)该反应的ΔH___ 0(填“>”或“<”,后同),pl____ p2,M、N相比,混合气体平均相对分子质量较大的是____ 。
(2) A、B, C、D四点中能正确表示该反应的平衡常数与温度T的关系的点为_____ 。
(3)下列各项数据能表明一定温度下,恒容密闭容器中反应2CO(g)+4H2(g) =CH3CH2OH(g)+H2O(g)达到平衡状态的是___ 。
a.气体密度保持不变 b.反应过程中 c(CO):c(H2)=1:2
c.生成速率:v(CO)=2v(H2O) d. ΔH—定
(4)若在恒容条件下,最初向容器中通入1 mol CO、2 mol H2,在适当催化剂、温度下使其发生反应2CO(g)+4H2(g) =CH3CH2OH(g)+H2O(g)。测得开始时容器总压为 3xl05Pa,反应经2 min达到平衡且平衡时体系压强降低了 ,则v(CO)=
,则v(CO)= ____ Pa/min,该温度下的平衡常数为Kp的值为____ 。
回答下列问题:
图1
 图2
图2 
(1)该反应的ΔH
(2) A、B, C、D四点中能正确表示该反应的平衡常数与温度T的关系的点为
(3)下列各项数据能表明一定温度下,恒容密闭容器中反应2CO(g)+4H2(g) =CH3CH2OH(g)+H2O(g)达到平衡状态的是
a.气体密度保持不变 b.反应过程中 c(CO):c(H2)=1:2
c.生成速率:v(CO)=2v(H2O) d. ΔH—定
(4)若在恒容条件下,最初向容器中通入1 mol CO、2 mol H2,在适当催化剂、温度下使其发生反应2CO(g)+4H2(g) =CH3CH2OH(g)+H2O(g)。测得开始时容器总压为 3xl05Pa,反应经2 min达到平衡且平衡时体系压强降低了
 ,则v(CO)=
,则v(CO)=
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】氢气是一种高能燃料,也广泛应用在工业合成中。
(1)标准摩尔生成焓是指在25℃和101kPa,最稳定的单质生成1mol化合物的焓变。已知25℃和101kPa
时下列反应:
①2C2H6(g)+7O2(g)=4CO2(g) +6H2O(l) △H=-3116 kJ·mol-1
②C(石墨,s)+O2(g) =CO2(g) △H=-393.5 kJ·mol-1
③2H2(g)+O2(g) =2H2O(l) △H=-571.6 kJ·mol-1
写出乙烷标准生成焓的热化学方程式:___________________________________________ 。
(2)已知合成氨的反应为:N2+3H2 2NH3 △H<0。某温度下,若将1mol N2和2.8mol H2分别投入到初始体积为2L的恒温恒容、恒温恒压和恒容绝热的三个密闭容器中,测得反应过程中三个容器(用a、b、c表示)内N2的转化率随时间的变化如图所示,请回答下列问题:
2NH3 △H<0。某温度下,若将1mol N2和2.8mol H2分别投入到初始体积为2L的恒温恒容、恒温恒压和恒容绝热的三个密闭容器中,测得反应过程中三个容器(用a、b、c表示)内N2的转化率随时间的变化如图所示,请回答下列问题:

①图中代表反应在恒容绝热容器中进行的曲线是______ (用a、b、c表示)
②曲线a条件下该反应的平衡常数K=_________ 。
③b容器中M点,v(正)____ v(逆)(填“大于”、“小于”或“等于”)
(3)利用氨气可以设计成高能环保燃料电池,用该电池电解含有NO2-的碱性工业废水,在阴极产生N2。阴极电极反应式为______ ;标准状况下,当阴极收集到11.2 LN2时,理论上消耗NH3的体积为_____ 。
(4)氨水是制备铜氨溶液的常用试剂,通过以下反应及数据来探究配制铜氨溶液的最佳途径。
已知:Cu(OH)2(s) ⇌Cu2++2OH- Ksp=2.2×10-20
Cu2++4NH3·H2O ⇌[Cu (NH3) 4]2+(深蓝色)+4H2O Kβ=7.24×1012
①请用数据说明利用该反应:Cu(OH)2(s) +4NH3·H2O ⇌[Cu (NH3) 4]2++4H2O+2OH-配制铜氨溶液是否可行:_________________________________________ 。
②已知反应Cu(OH)2(S) +2NH3·H2O+2NH 4+⇌[Cu (NH3) 4]2++4H2O K=5.16×102。向盛有少量Cu(OH)2固体的试管中加入14 mol·L-1的氨水,得到悬浊液;此时若加入适量的硫酸铵固体,出现的现象为_______________ ;解释出现该现象的原因是_____________________ 。
(1)标准摩尔生成焓是指在25℃和101kPa,最稳定的单质生成1mol化合物的焓变。已知25℃和101kPa
时下列反应:
①2C2H6(g)+7O2(g)=4CO2(g) +6H2O(l) △H=-3116 kJ·mol-1
②C(石墨,s)+O2(g) =CO2(g) △H=-393.5 kJ·mol-1
③2H2(g)+O2(g) =2H2O(l) △H=-571.6 kJ·mol-1
写出乙烷标准生成焓的热化学方程式:
(2)已知合成氨的反应为:N2+3H2
 2NH3 △H<0。某温度下,若将1mol N2和2.8mol H2分别投入到初始体积为2L的恒温恒容、恒温恒压和恒容绝热的三个密闭容器中,测得反应过程中三个容器(用a、b、c表示)内N2的转化率随时间的变化如图所示,请回答下列问题:
2NH3 △H<0。某温度下,若将1mol N2和2.8mol H2分别投入到初始体积为2L的恒温恒容、恒温恒压和恒容绝热的三个密闭容器中,测得反应过程中三个容器(用a、b、c表示)内N2的转化率随时间的变化如图所示,请回答下列问题:
①图中代表反应在恒容绝热容器中进行的曲线是
②曲线a条件下该反应的平衡常数K=
③b容器中M点,v(正)
(3)利用氨气可以设计成高能环保燃料电池,用该电池电解含有NO2-的碱性工业废水,在阴极产生N2。阴极电极反应式为
(4)氨水是制备铜氨溶液的常用试剂,通过以下反应及数据来探究配制铜氨溶液的最佳途径。
已知:Cu(OH)2(s) ⇌Cu2++2OH- Ksp=2.2×10-20
Cu2++4NH3·H2O ⇌[Cu (NH3) 4]2+(深蓝色)+4H2O Kβ=7.24×1012
①请用数据说明利用该反应:Cu(OH)2(s) +4NH3·H2O ⇌[Cu (NH3) 4]2++4H2O+2OH-配制铜氨溶液是否可行:
②已知反应Cu(OH)2(S) +2NH3·H2O+2NH 4+⇌[Cu (NH3) 4]2++4H2O K=5.16×102。向盛有少量Cu(OH)2固体的试管中加入14 mol·L-1的氨水,得到悬浊液;此时若加入适量的硫酸铵固体,出现的现象为
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
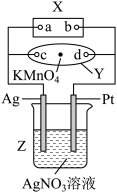
【推荐1】(1)2004年美国圣路易斯大学研制了一种新型乙醇电池,该电池采用磺酸类质子溶剂,在200 ℃左右时供电,电池示意图如图所示:

写出该电池负极的电极反应式:____ 。
(2)图中X为电源,Y为浸透滴有酚酞试液的饱和食盐水的滤纸,滤纸中央滴有一滴KMnO4溶液,通电后Y中央的紫红色斑向d端扩散。电解一段时间后,Z产生280 mL的气体(标准状况下),此时Z中溶液的体积为500 mL,假设溶液中还有AgNO3存在,则溶液中氢离子的物质的量是____ ,需加入____ g的____ (填化学式)可使溶液复原。
(3)氧化还原反应与生产、生活、科技密切相关。请回答下列问题:
①银制器皿久置表面变黑是因为表面生成了Ag2S,该现象属于____ 腐蚀。
②在如图所示的原电池装置中,负极的电极反应为____ ,电池总反应为____ ,当电路中通过0.1 mol e-时,交换膜左侧溶液中离子减少的物质的量为____ 。
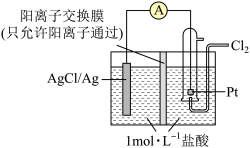
③电解NO制备NH4NO3原理如图所示,接电源负极的电极为____ (填X或Y),Y电极反应式为____ ,为使电解产物完全转化为NH4NO3,需要补充的物质A的化学式为____ 。
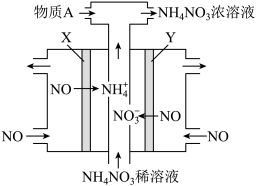

写出该电池负极的电极反应式:
(2)图中X为电源,Y为浸透滴有酚酞试液的饱和食盐水的滤纸,滤纸中央滴有一滴KMnO4溶液,通电后Y中央的紫红色斑向d端扩散。电解一段时间后,Z产生280 mL的气体(标准状况下),此时Z中溶液的体积为500 mL,假设溶液中还有AgNO3存在,则溶液中氢离子的物质的量是

(3)氧化还原反应与生产、生活、科技密切相关。请回答下列问题:
①银制器皿久置表面变黑是因为表面生成了Ag2S,该现象属于
②在如图所示的原电池装置中,负极的电极反应为

③电解NO制备NH4NO3原理如图所示,接电源负极的电极为

您最近半年使用:0次
【推荐2】赤泥硫酸铵焙烧浸出液水解制备偏钛酸[TiO(OH)2]可回收钛。
已知:
i.⼀定条件下,Ti4+水解⽅程式:
ii.⼀定温度下: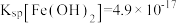 ;
;
I.赤泥与硫酸铵混合制取浸出液。
(1)用化学用语表示(NH4)2SO4溶液呈酸性的原因___________ 。
II.水解制备偏钛酸:浸出液中含Fe3+、Ti4+等,先向其中加入还原铁粉,然后控制水解条件实现Ti4+水解制备偏钛酸。
(2)浸出液(pH=2)中含有大量Ti4+,若杂质离子沉淀会降低钛水解率。从定量⻆度解释加入还原铁粉的目的___________ 。
(3)⼀定条件下,还原铁粉添加比对钛水解率的影响如图所示。当还原铁粉添加比大于1时,钛水解率急剧下降,解释其原因___________ 。 ;n铁粉为还原铁粉添加量,n理论为浸出液中Fe3+全部还原为Fe2+所需的还原铁粉理论量。
;n铁粉为还原铁粉添加量,n理论为浸出液中Fe3+全部还原为Fe2+所需的还原铁粉理论量。
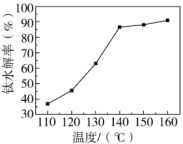
(4)⼀定条件下,温度对钛水解率的影响如图所示。结合化学平衡移动原理解释钛水解率随温度升高而增大的原因___________ 。___________ (填“正”或“负”)极。
(6)写出电极Y上发生的电极反应式___________ 。
已知:
i.⼀定条件下,Ti4+水解⽅程式:

ii.⼀定温度下:
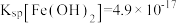 ;
;
I.赤泥与硫酸铵混合制取浸出液。
(1)用化学用语表示(NH4)2SO4溶液呈酸性的原因
II.水解制备偏钛酸:浸出液中含Fe3+、Ti4+等,先向其中加入还原铁粉,然后控制水解条件实现Ti4+水解制备偏钛酸。
(2)浸出液(pH=2)中含有大量Ti4+,若杂质离子沉淀会降低钛水解率。从定量⻆度解释加入还原铁粉的目的
(3)⼀定条件下,还原铁粉添加比对钛水解率的影响如图所示。当还原铁粉添加比大于1时,钛水解率急剧下降,解释其原因
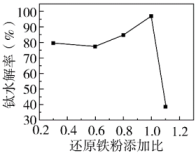
 ;n铁粉为还原铁粉添加量,n理论为浸出液中Fe3+全部还原为Fe2+所需的还原铁粉理论量。
;n铁粉为还原铁粉添加量,n理论为浸出液中Fe3+全部还原为Fe2+所需的还原铁粉理论量。(4)⼀定条件下,温度对钛水解率的影响如图所示。结合化学平衡移动原理解释钛水解率随温度升高而增大的原因
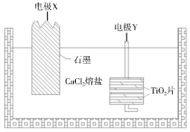
(6)写出电极Y上发生的电极反应式
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】I.硫酸工业中废渣称为硫酸渣,其成分为SiO2、Fe2O3、Al2O3、MaO。某学习小组的同学设计以下方案,进行硫酸渣中金属元素的提取实验。

已知:溶液pH=3.7时,Fe3+已经沉淀完全;一水合氨其饱和溶液中c(OH-)约为1×10-3mol·L-1。
(1)写出A与氢氧化钠溶液反应的离子方程式:______________________________ 。
(2)上述流程中两次使用试剂①,推测试剂①应该是____________ (填字母)
A.氢氧化钠 B.氧化铝 C.氨水 D.水
(3)H中溶质是______________ 。(填化学式)
(4)溶液D到固体E过程中需要控制溶液pH=13,如果pH过小,可能导致的后果是______________ 。
(4)计算溶液F中c(Mg2+)=______________ (25℃时,氢氧化镁的Ksp=5.6×10-12)
II.某化学兴趣小组用下图所示装置进行电化学原理的实验探究。

(1)A装置为乙醇燃料电池,若X、Y均是铜,电解质溶液为NaOH溶液,电池工作一段时间,X极附近生成砖红色沉淀,查阅资料得知是Cu2O,试写出该电极发生的电极反应式为________________________ 。
(2)若B电池的电解质溶液为500mL1.0mol/L的NaCl溶液,X、Y皆为惰性电极,当电池工作一段时间断开电源K,Y电极有560mL(标准状况)无色气体生成(假设电极产生气体完全溢出,溶液体积不变)此时B电池溶液的pH=____________ ,要是该溶液恢复到原来的状态,需加入____________ (填物质并注明物质的量)。

已知:溶液pH=3.7时,Fe3+已经沉淀完全;一水合氨其饱和溶液中c(OH-)约为1×10-3mol·L-1。
(1)写出A与氢氧化钠溶液反应的离子方程式:
(2)上述流程中两次使用试剂①,推测试剂①应该是
A.氢氧化钠 B.氧化铝 C.氨水 D.水
(3)H中溶质是
(4)溶液D到固体E过程中需要控制溶液pH=13,如果pH过小,可能导致的后果是
(4)计算溶液F中c(Mg2+)=
II.某化学兴趣小组用下图所示装置进行电化学原理的实验探究。

(1)A装置为乙醇燃料电池,若X、Y均是铜,电解质溶液为NaOH溶液,电池工作一段时间,X极附近生成砖红色沉淀,查阅资料得知是Cu2O,试写出该电极发生的电极反应式为
(2)若B电池的电解质溶液为500mL1.0mol/L的NaCl溶液,X、Y皆为惰性电极,当电池工作一段时间断开电源K,Y电极有560mL(标准状况)无色气体生成(假设电极产生气体完全溢出,溶液体积不变)此时B电池溶液的pH=
您最近半年使用:0次



