名校
1 . 我国科学家实现了在铜催化剂条件下将DMF[(CH3)2NCHO]转化为三甲胺[N(CH3)3]。计算机模拟单个DMF分子在铜催化剂表面的反应历程如图所示,下列说法正确的是
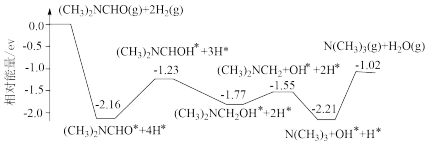

| A.该历程中最小能垒的化学方程式为 (CH3)2NCH2OH*=(CH3)2NCH2+OH* |
| B.该历程中最大能垒(活化能)为2.16eV |
| C.该反应热化学方程式为(CH3)2NCHO(g)+2H2(g)=N(CH3)3(g)+H2O(g) ΔH=-1.02ev•mol-1 |
| D.增大压强或升高温度均能加快反应速率,并增大DMF平衡转化率 |
您最近一年使用:0次
2022-08-24更新
|
780次组卷
|
29卷引用:山东省威海市2020届高三年级高考模拟考(二模)化学试题
山东省威海市2020届高三年级高考模拟考(二模)化学试题(已下线)专题07 化学反应中的能量变化-2020年高考真题和模拟题化学分项汇编浙江省杭州第二中学2021届高三上学期期中考试化学试题山西省运城市教育发展联盟2021-2022学年高二上学期11月期中检测化学试题河北省张家口市宣化一中2020-2021学年高二下学期期初考试化学试题(已下线)解密08 化学反应与能量(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)解密08 化学反应与能量(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)浙江省绍兴市第一中学2020-2021学年高三1月高考适应性考试化学试题(已下线)押全国卷理综第13题 反应机理图分析、能垒图分析等创新题型及阿伏伽德罗常数-备战2021年高考化学临考题号押题(课标全国卷)(已下线)考点20 化学能与热能-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点20 化学能与热能-备战2022年高考化学一轮复习考点帮(浙江专用)湖南省长沙市雅礼中学2021-2022学年高三上学期月考卷(三)化学试题辽宁省大连市第一中学 2021-2022学年高三上学期期中联考化学试题河南省顶尖名校联盟2021-2022学年高二下学期联赛考试化学试题(已下线)卷04 小题素养卷-【小题小卷】冲刺2022年高考化学小题限时集训(新高考专用)(已下线)2022年湖南卷高考真题变式题(11-14)(已下线)考点17 化学反应的热效应-备战2023年高考化学一轮复习考点帮(全国通用)辽宁省大连市普兰店区第一中学2022届高三上学期期中联考化学试题湖南省邵阳市第二中学2022届高三下学期全真模拟考试化学试题湖南省株洲市第二中学2022-2023学年高二上学期期中考试化学试题湖南省株洲南方中学2022-2023学年高二上学期期中考试化学试题(已下线)第七章 化学反应速率与化学平衡 热点强化12 化学反应历程、机理的分析应用北京市第二十中学2022-2023学年高三下学期开学检测化学试题(已下线)查补易混易错04 化学反应原理部分-【查漏补缺】2023年高考化学三轮冲刺过关(新高考专用)山东省青岛第二中学2021-2022学年高二上学期期中考试化学试题福建省南安市华侨中学2023-2024学年高二上学期10月月考化学试题福建省德化一中、永安一中、漳平一中三校协作2023-2024学年高二上学期12月联考化学试题(已下线)广西“贵百河”2023-2024学年高二上学期12月份联考化学试题山东省德州市实验中学2023-2024学年高二上学期期中考试 化学试题
名校
解题方法
2 . 反应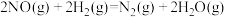 中,每生成
中,每生成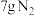 放出
放出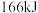 的热量,该反应的速率表达式为
的热量,该反应的速率表达式为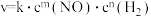 (k、m、n待测),其反应包含下列两步:
(k、m、n待测),其反应包含下列两步:
①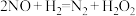 (慢)
(慢)
②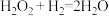 (快)
(快)
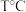 时测得有关实验数据如下:
时测得有关实验数据如下:
下列说法正确的是
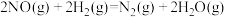 中,每生成
中,每生成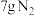 放出
放出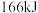 的热量,该反应的速率表达式为
的热量,该反应的速率表达式为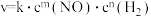 (k、m、n待测),其反应包含下列两步:
(k、m、n待测),其反应包含下列两步:①
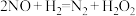 (慢)
(慢)②
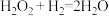 (快)
(快)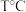 时测得有关实验数据如下:
时测得有关实验数据如下:| 序号 | 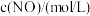 | 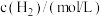 | 速率/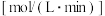 |
| Ⅰ | 0.0060 | 0.0010 |  |
| Ⅱ | 0.0060 | 0.0020 |  |
| Ⅲ | 0.0010 | 0.0060 |  |
| Ⅳ | 0.0020 | 0.0060 | 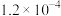 |
| A.正反应的活化能一定是①<② |
| B.整个反应速度由第②步反应决定 |
C.该反应速率表达式: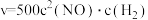 |
D.该反应的热化学方程式为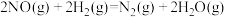  |
您最近一年使用:0次
2021-09-20更新
|
761次组卷
|
19卷引用:山西省忻州市第一中学2019-2020学年高二下学期期中考试化学试题
山西省忻州市第一中学2019-2020学年高二下学期期中考试化学试题2016-2017学年河北正定中学高二上开学考试化学卷2016-2017学年湖南省衡阳八中高二上月考四化学卷甘肃省兰州第一中学2017-2018学年高二上学期第一次月考(9月)化学试题【全国校级联考】内蒙古赤峰市重点高中(赤峰二中,平煤高级中学等)2017-2018学年高二下学期期末联考(A)化学试题2020届高三化学二轮冲刺新题专练——影响化学反应速率的因素(提升练)夯基提能2020届高三化学选择题对题专练——选修4化学反应原理—— 影响化学反应速率的因素(强化练习)安徽省太和第一中学2019-2020学年高一下学期期末考试化学试题(已下线)第02章 化学反应速率与化学平衡(B卷能力提高篇)-2020-2021学年高二化学选择性必修1同步单元AB卷(新教材人教版)(已下线)第七章 能力提升检测卷-2021年高考化学一轮复习讲练测湖南省湘阴县知源学校2020-2021学年高二上学期9月月考化学试题内蒙古包头市回民中学2020-2021学年高二上学期期中考试化学试题山东省东营市胜利第二中学2020-2021学年高二10月月考化学试题(已下线)专题七 能力提升检测卷 (测) — 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)第20讲 化学平衡常数及转化率的计算(讲) — 2022年高考化学一轮复习讲练测(新教材新高考)江苏省泰州中学2022届高三上学期期初检测化学试题(已下线)专题21 化学反应速率(热点讲义)-2022年高三毕业班化学常考点归纳与变式演练安徽省合肥市第六中学2021-2022学年高二上学期月考化学试题安徽省舒城中学2022-2023学年高二上学期第二次月考化学试题
3 . 氮的氧化物是造成大气污染的主要物质,研究氮氧化物间的相互转化及脱除具有重要意义。
I.氮氧化物间的相互转化
(1)已知2NO(g)+O2(g) 2NO2(g)的反应历程分两步:
2NO2(g)的反应历程分两步:
第一步2NO(g) N2O2(g)(快速平衡)
N2O2(g)(快速平衡)
第二步N2O2(g)+O2(g) 2NO2(g)(慢反应)
2NO2(g)(慢反应)
①用O2表示的速率方程为v(O2)=k1·c2(NO)·c(O2);NO2表示的速率方程为v(NO2)=k2·c2(NO)·c(O2),k1与k2分别表示速率常数,则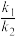 =
=___________ 。
②下列关于反应2NO(g)+O2(g)=2NO2(g)的说法正确的是___________ (填序号)。
A.增大压强,反应速率常数一定增大
B.第一步反应的活化能小于第二步反应的活化能
C.反应的总活化能等于第一步和第二步反应的活化能之和
(2)2NO2(g) N2O4(g) (△H<0),用分压(某组分的分压等于总压与其物质的量分数的积)表示的平衡常数KP与
N2O4(g) (△H<0),用分压(某组分的分压等于总压与其物质的量分数的积)表示的平衡常数KP与 (T为温度)的关系如图。
(T为温度)的关系如图。
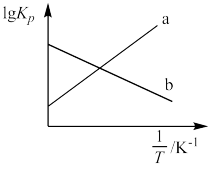
①能正确表示lgKP与 关系的曲线是
关系的曲线是___________ (填“a”或“b”)。
②298K时,在体积固定的密闭容器中充入一定量的NO2,平衡时NO2的分压为100kPa。已知KP=2.7×10-3kPa-1,则NO2的转化率为___________ 。
II.烟气中氮氧化物的脱除
(3)以NH3为还原剂在脱硝装置中消除烟气中的氮氧化物。
主反应:4NH3(g)+4NO(g)+O2(g)=4N2(g)+6H2O(g) △H1
副反应:4NH3(g)+3O2(g)=2N2(g)+6H2O(g) △H2=-1267.1kJ/mol
4NH3(g)+5O2(g)=4NO(g)+6H2O(g) △H3=-907.3kJ/mol
△H1=___________ 。
(4)以连二亚硫酸盐(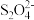 )为还原剂脱除烟气中的NO,并通过电解再生,装置如下图。
)为还原剂脱除烟气中的NO,并通过电解再生,装置如下图。
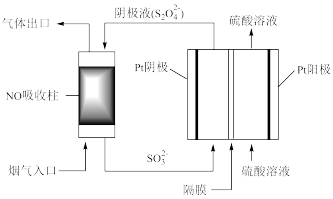
阴极的电极反应式为___________ ,电解槽中的隔膜为___________ (填“阳”或“阴”)离子交换膜。
I.氮氧化物间的相互转化
(1)已知2NO(g)+O2(g)
 2NO2(g)的反应历程分两步:
2NO2(g)的反应历程分两步:第一步2NO(g)
 N2O2(g)(快速平衡)
N2O2(g)(快速平衡)第二步N2O2(g)+O2(g)
 2NO2(g)(慢反应)
2NO2(g)(慢反应)①用O2表示的速率方程为v(O2)=k1·c2(NO)·c(O2);NO2表示的速率方程为v(NO2)=k2·c2(NO)·c(O2),k1与k2分别表示速率常数,则
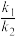 =
=②下列关于反应2NO(g)+O2(g)=2NO2(g)的说法正确的是
A.增大压强,反应速率常数一定增大
B.第一步反应的活化能小于第二步反应的活化能
C.反应的总活化能等于第一步和第二步反应的活化能之和
(2)2NO2(g)
 N2O4(g) (△H<0),用分压(某组分的分压等于总压与其物质的量分数的积)表示的平衡常数KP与
N2O4(g) (△H<0),用分压(某组分的分压等于总压与其物质的量分数的积)表示的平衡常数KP与 (T为温度)的关系如图。
(T为温度)的关系如图。
①能正确表示lgKP与
 关系的曲线是
关系的曲线是②298K时,在体积固定的密闭容器中充入一定量的NO2,平衡时NO2的分压为100kPa。已知KP=2.7×10-3kPa-1,则NO2的转化率为
II.烟气中氮氧化物的脱除
(3)以NH3为还原剂在脱硝装置中消除烟气中的氮氧化物。
主反应:4NH3(g)+4NO(g)+O2(g)=4N2(g)+6H2O(g) △H1
副反应:4NH3(g)+3O2(g)=2N2(g)+6H2O(g) △H2=-1267.1kJ/mol
4NH3(g)+5O2(g)=4NO(g)+6H2O(g) △H3=-907.3kJ/mol
△H1=
(4)以连二亚硫酸盐(
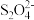 )为还原剂脱除烟气中的NO,并通过电解再生,装置如下图。
)为还原剂脱除烟气中的NO,并通过电解再生,装置如下图。
阴极的电极反应式为
您最近一年使用:0次
2020-12-14更新
|
285次组卷
|
3卷引用:河南省实验中学2021届高三上学期期中考试化学试题
名校
4 . 关于有效碰撞理论,下列说法不正确 的是
| A.化学反应的实质是活化分子有合适取向时的有效碰撞 |
| B.增大反应物浓度能够增大活化分子百分数,化学反应速率一定增大 |
| C.升高温度,活化分子百分数增加,化学反应速率一定增大 |
| D.催化剂能改变反应历程和活化能,影响化学反应速率 |
您最近一年使用:0次
2020-12-08更新
|
218次组卷
|
6卷引用:福建省三明市泰宁县福建省泰宁第一中学2019-2020学年高二上学期第二次阶段考试化学试题
福建省三明市泰宁县福建省泰宁第一中学2019-2020学年高二上学期第二次阶段考试化学试题福建省泉州第十六中学2020-2021学年高二上学期期中考试化学(选考班)试题山西省太原市第五中学校2023-2024学年高二上学期10月月考化学试题海南省北京师范大学万宁附中2020-2021学年高一下学期期中考试化学试题(已下线)2.1.3 活化能(素养提优B练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)福建省福州铜盘中学2021-2022学年高二上学期12月月考化学试题
名校
5 . 已知反应:2NO(g)+Br2(g)=2NOBr(g) △H=-akJ·mol-1(a>0),其反应机理如下:
①NO(g)+Br2(g)=NOBr2(g) △H1快反应;
②NO(g)+NOBr2(g)=2NOBr(g) △H2慢反应。
下列说法不正确的是( )
①NO(g)+Br2(g)=NOBr2(g) △H1快反应;
②NO(g)+NOBr2(g)=2NOBr(g) △H2慢反应。
下列说法不正确的是( )
| A.△H=△H1+△H2 |
| B.该反应的速率主要取决于反应① |
| C.NOBr2是该反应的中间产物,不是催化剂 |
| D.恒容时,增大Br2(g)的浓度能增加单位体积活化分子总数,加快反应速率 |
您最近一年使用:0次
2020-11-24更新
|
535次组卷
|
7卷引用:山西省太原市2020-2021学年高二上学期期中质量监测化学(理)试题
山西省太原市2020-2021学年高二上学期期中质量监测化学(理)试题选择性必修1 专题2 第一单元综合训练(已下线)选择性必修1 期中检测(基础过关卷)-【高效检测】2021-2022学年高二化学章末测试卷(人教版2019选择性必修1)湖北省孝感市2021-2022学年高二上学期期中联考化学试题浙江省温州市平阳县万全综合高级中学2021-2022学年高二上学期期中考试化学试题 天津市静海区第一中学2023-2024学年高二上学期12月月考化学试题广东省惠州市龙门县高级中学2023-2024学年高二上学期12月月考化学试题
名校
6 . 在恒容条件下,能使NO2(g)+CO(g) CO2(g)+NO(g)正反应速率增大且活化分子的百分数也增大的措施是:
CO2(g)+NO(g)正反应速率增大且活化分子的百分数也增大的措施是:
 CO2(g)+NO(g)正反应速率增大且活化分子的百分数也增大的措施是:
CO2(g)+NO(g)正反应速率增大且活化分子的百分数也增大的措施是:| A.增大NO2或CO的浓度 |
| B.减小CO2或NO的浓度 |
| C.通入Ne使气体的压强增大 |
| D.升高反应的温度 |
您最近一年使用:0次
2020-11-02更新
|
626次组卷
|
22卷引用:2016-2017学年山西省怀仁一中高二上开学考化学试卷
2016-2017学年山西省怀仁一中高二上开学考化学试卷【全国百强校】山西省平遥中学2018-2019学年高二上学期期中考试化学试题2015-2016学年安徽省舒城晓天中学高二上学期期中测试化学试卷2016-2017学年湖北沙市中学高二上第一次双周练化学卷2016-2017学年江苏省泰州中学高二上月考一化学试卷安徽师范大学附属中学2017-2018学年高二上学期期中考查化学试题山东省师范大学附属中学2017-2018学年高二上学期第五次学分认定(期中)考试(理)化学试题山东师范大学附属中学2017-2018学年高二上学期第五次学分认定考试化学(理)试题【校级联考】天津市静海区2019届高三上学期12月四校联考化学试题福建省漳州市长泰县第一中学2019-2020学年高二10月月考化学试题重庆市第一中学2020-2021学年高二10月月考化学试题(已下线)第10单元 化学反应速率与化学平衡(A卷 基础过关检测)-2021年高考化学一轮复习单元滚动双测卷河南省安阳县第三高级中学2020-2021学年高二上学期第一次阶段考试化学试题吉林省辽源市田家炳高级中学校2020-2021学年高二上学期期中考试化学试题浙江省浙北G2(嘉兴一中、湖州中学)2020-2021学年高二上学期期中联考化学试题重庆市清华中学2020-2021学年高二11月月考化学试题宁夏大学附属中学2020-2021学年高二下学期第一次月考化学试题河南省新乡县龙泉高级中学2021-2022学年高二上学期9月月考化学试题广东省广州市协和中学等3校2022-2023学年高二上学期(12月)期末考试化学试题上海市上海中学2022-2023学年高一下学期期末考试化学试题四川省南充高级中学2021-2022学年高一下学期第二次月考化学试题广东省汕头市潮阳黄图盛中学2023-2024学年高二上学期期中考试化学试题
7 . 下列说法不正确的是
| A.活化分子的碰撞不一定是有效碰撞 |
| B.发生有效碰撞的分子一定是活化分子 |
| C.升高温度和增大压强都可以提高反应体系内活化分子百分数 |
| D.催化剂可以改变反应的活化能,可以提高活化分子百分数,但是不能改变反应热 |
您最近一年使用:0次
2020-10-29更新
|
197次组卷
|
2卷引用:山西省太原市第五中学2020-2021学年高二上学期10月月考试题
8 . 下列说法正确的是( )
| A.增大压强(缩小容器体积),活化分子百分数增大,反应速率一定增大 |
| B.增大反应物浓度,活化分子百分数增大,反应速率一定增大 |
| C.降低温度,活化分子百分数增大,反应速率一定增大 |
| D.使用催化剂,活化分子百分数增大,反应速率一定增大 |
您最近一年使用:0次
2020-10-11更新
|
142次组卷
|
3卷引用:【全国校级联考】山西省汾阳市第二高级中学、文水县第二高级中学2016-2017学年高二上学期第一次联考化学试题
名校
解题方法
9 . 在气体反应中,使反应物中活化分子数增多,且活化分子百分数增大的方法是( )
①增大反应物浓度②升高温度③增大压强④移去生成物⑤加入合适的催化剂
①增大反应物浓度②升高温度③增大压强④移去生成物⑤加入合适的催化剂
| A.①③⑤ | B.②⑤ | C.②③⑤ | D.①③④ |
您最近一年使用:0次
2020-09-02更新
|
279次组卷
|
23卷引用:山西省长治二中2018-2019学年高二上学期第一次月考化学试题
山西省长治二中2018-2019学年高二上学期第一次月考化学试题2015-2016学年重庆市杨家坪中学高二上学期第一次月考化学试卷2015-2016学年宁夏育才中学高二上期末考试化学试卷2015-2016学年吉林省长春外国语学校高二上学期期末化学试卷2015-2016学年湖北省武汉二中高一下期末化学试卷湖北省宜昌市协作体2016-2017学年高一下学期期末考试化学试题安徽省铜陵市第一中学2017-2018学年高二10月月考化学试题浙江省宁波市北仑中学2018-2019学年高二上学期期初返校考试化学试题【全国百强校】安徽省铜陵市第一中学2018-2019学年高二上学期10月月考化学试题四川省宜宾市第三中学2018-2019学年高二上学期11月月考化学试题浙江省诸暨中学2018-2019学年高二(平行班)下学期期中考试化学试题河北省沧州市泊头市第一中学2019-2020学年高二月考检测化学试题河北省泊头市第一中学2019-2020学年高二上学期期末模拟考试化学试卷江西省上饶市横峰中学2019-2020学年高一(自招班)下学期入学考试化学试题(已下线)2.1.2 影响化学反应速率的因素(重点练)——2020-2021学年高二化学上学期十分钟同步课堂专练(苏教版选修4)河南省兰考县第三高级中学卫星试验部2020-2021学年高二上学期第一次月考化学试题黑龙江省哈尔滨市第一中学校2019-2020学年高一下学期期末考试化学试题贵州省遵义市航天高级中学2020-2021学年高二上学期第一次月考化学(理)试题陕西省宝鸡市金台区2020-2021学年高二上学期期中考试化学(理)试题江苏省海安市2020-2021学年高二上学期期中考试化学试题江西省南昌市外国语学校2020~2021学年高二上学期期中考试理科化学试题云南省红河县一中2021-2022学年高二上学期期中考试化学试题广西南宁市宾阳县宾阳中学2021-2022学年高二上学期期中考试化学(理科)试题
解题方法
10 . 常温常压下,H2和O2在Ag9(图中物质1)团簇上生成H2O2的吉布斯自由能( )的部分变化曲线如图。下列说法错误的是
)的部分变化曲线如图。下列说法错误的是

 )的部分变化曲线如图。下列说法错误的是
)的部分变化曲线如图。下列说法错误的是
| A.物质2中的O2是处于被吸附活化状态 |
B.物质3→物质4的过程中活化吉布斯自由能能垒为 |
C.物质4可能为 |
D.反应 具有自发性 具有自发性 |
您最近一年使用:0次
2020-07-15更新
|
85次组卷
|
2卷引用:山西省2019-2020学年高二6月联合考试化学试题



