解题方法
1 . 2SO2(g)+O2(g) 2SO3(g)反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能)。下列有关叙述正确的是
2SO3(g)反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能)。下列有关叙述正确的是

 2SO3(g)反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能)。下列有关叙述正确的是
2SO3(g)反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能)。下列有关叙述正确的是
| A.曲线①表示使用了催化剂时的反应过程 |
| B.升高温度,活化分子百分数增加,υ正加快 |
| C.使用催化剂会使该反应的反应热发生改变 |
| D.△H=+(E2−E1) kJ∙mol−1 |
您最近一年使用:0次
2 . 下列关于有效碰撞理论与影响速率因素之间关系正确的是
| A.增大反应物浓度,可以提高活化分子百分数,从而提高反应速率 |
| B.对于气体反应来说,通过压缩体积增大压强,可以提高单位体积内活化分子数,从而提高反应速率 |
| C.温度升高,分子动能增加,反应所需活化能减少,反应速率增大 |
| D.选用适当的催化剂,分子运动加快,增加了碰撞频率,故反应速率增大 |
您最近一年使用:0次
2021-12-24更新
|
462次组卷
|
4卷引用:北京师范大学附属中学2020-2021学年高二上学期期中考试化学试题
名校
3 . Ni可活化C2H6放出CH4,其反应历程如下图所示:
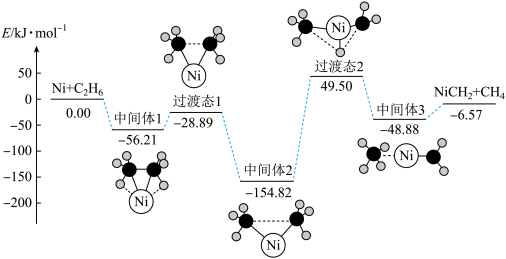
下列关于活化历程的说法正确的是

下列关于活化历程的说法正确的是
| A.决速步骤:中间体1→中间体2 | B.总反应为Ni+C2H6→NiCH2+CH4 |
| C.Ni−H键的形成对氢原子的迁移是不利的 | D.涉及非极性键的断裂和生成 |
您最近一年使用:0次
2021-10-09更新
|
511次组卷
|
6卷引用:重庆市西南大学附属中学2022届高三上学期第二次月考化学试题
2020·全国·模拟预测
名校
解题方法
4 . 如图是CH4与Cl2生成CH3Cl的部分反应过程中各物质物质的能量变化关系图(Ea表示活化能),下列说法正确的是
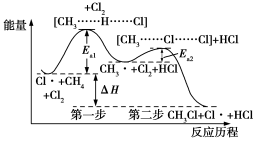

| A.增大Cl2的浓度,可提高反应速率,但不影响ΔH的大小 |
| B.升高温度,Ea1、Ea2均减小,反应速率加快 |
| C.Cl·可由Cl2在高温条件下生成,是CH4与Cl2反应的催化剂 |
| D.第一步反应的速率大于第二步反应 |
您最近一年使用:0次
2021-04-13更新
|
293次组卷
|
4卷引用:学科网2020年高三11月大联考考后强化卷(新课标Ⅰ卷)
(已下线)学科网2020年高三11月大联考考后强化卷(新课标Ⅰ卷)(已下线)学科网2020年高三11月大联考考后强化卷(新课标Ⅱ卷)重庆市西南大学附属中学校2023-2024学年高二下学期3月联合考试化学试题 吉林省吉林实验中学2021-2022学年高三上学期第二次诊断测试化学试题
名校
5 . 下列措施能降低化学反应的活化能,提高反应速率的是
| A.增大反应物浓度 | B.加催化剂 |
| C.加压 | D.升温 |
您最近一年使用:0次
2021-01-28更新
|
233次组卷
|
8卷引用:黑龙江省嫩江市高级中学2020-2021学年高二上学期9月月考化学试题
名校
6 . 下列利用相关数据作出的推理或判断一定正确的是
| A.利用焓变数据判断反应能否自发进行 |
| B.利用反应热数据判断反应速率的大小 |
| C.利用平衡常数判断反应进行的程度大小 |
| D.利用反应的活化能数据判断反应热的大小 |
您最近一年使用:0次
2020-12-29更新
|
385次组卷
|
4卷引用:广东省广州市执信中学(广雅,执信,二中联考)2019-2020学年高二上学期期末考试化学试题
名校
7 . 下列条件中,不改变活化分子百分率但仍可以加快反应速率的是
| A.加热 | B.减压 | C.加催化剂 | D.加大反应物浓度 |
您最近一年使用:0次
名校
8 . 关于有效碰撞理论,下列说法正确的是
| A.活化分子间的碰撞一定是有效碰撞 |
| B.升高温度会加快反应速率,原因是增加了活化分子的有效碰撞次数 |
| C.使用催化剂能提高反应速率,原因是提高了分子的能量,使有效碰撞频率增大 |
| D.反应物分子之间的碰撞一定会引起化学键的断裂 |
您最近一年使用:0次
2020-11-24更新
|
237次组卷
|
4卷引用:浙江省杭州市富阳区第二中学2020-2021学年高二上学期期中考试化学试题
名校
9 . 在恒容条件下,能使NO2(g)+CO(g) CO2(g)+NO(g)正反应速率增大且活化分子的百分数也增大的措施是:
CO2(g)+NO(g)正反应速率增大且活化分子的百分数也增大的措施是:
 CO2(g)+NO(g)正反应速率增大且活化分子的百分数也增大的措施是:
CO2(g)+NO(g)正反应速率增大且活化分子的百分数也增大的措施是:| A.增大NO2或CO的浓度 |
| B.减小CO2或NO的浓度 |
| C.通入Ne使气体的压强增大 |
| D.升高反应的温度 |
您最近一年使用:0次
2020-11-02更新
|
627次组卷
|
22卷引用:重庆市第一中学2020-2021学年高二10月月考化学试题
重庆市第一中学2020-2021学年高二10月月考化学试题重庆市清华中学2020-2021学年高二11月月考化学试题2015-2016学年安徽省舒城晓天中学高二上学期期中测试化学试卷2016-2017学年山西省怀仁一中高二上开学考化学试卷2016-2017学年湖北沙市中学高二上第一次双周练化学卷2016-2017学年江苏省泰州中学高二上月考一化学试卷安徽师范大学附属中学2017-2018学年高二上学期期中考查化学试题山东省师范大学附属中学2017-2018学年高二上学期第五次学分认定(期中)考试(理)化学试题山东师范大学附属中学2017-2018学年高二上学期第五次学分认定考试化学(理)试题【全国百强校】山西省平遥中学2018-2019学年高二上学期期中考试化学试题【校级联考】天津市静海区2019届高三上学期12月四校联考化学试题福建省漳州市长泰县第一中学2019-2020学年高二10月月考化学试题(已下线)第10单元 化学反应速率与化学平衡(A卷 基础过关检测)-2021年高考化学一轮复习单元滚动双测卷河南省安阳县第三高级中学2020-2021学年高二上学期第一次阶段考试化学试题吉林省辽源市田家炳高级中学校2020-2021学年高二上学期期中考试化学试题浙江省浙北G2(嘉兴一中、湖州中学)2020-2021学年高二上学期期中联考化学试题宁夏大学附属中学2020-2021学年高二下学期第一次月考化学试题河南省新乡县龙泉高级中学2021-2022学年高二上学期9月月考化学试题广东省广州市协和中学等3校2022-2023学年高二上学期(12月)期末考试化学试题上海市上海中学2022-2023学年高一下学期期末考试化学试题四川省南充高级中学2021-2022学年高一下学期第二次月考化学试题广东省汕头市潮阳黄图盛中学2023-2024学年高二上学期期中考试化学试题
名校
10 . 以下说法不正确的是 ( )
| A.升高温度可以提高活化分子百分率,加快反应速率 |
| B.使用催化剂可以降低反应活化能,加快反应速率 |
| C.一个反应活化能越大,反应放出或吸收的热量就越多 |
| D.对于有气体参与的反应,温度不变时压强的变化可以看作改变浓度 |
您最近一年使用:0次
2020-10-08更新
|
142次组卷
|
2卷引用:安徽省舒城中学2020-2021学年高二上学期第二次月考化学试题



