解题方法
1 . 甲醇( )作为重要的清洁燃料和合成化学的关键前驱体,在化工行业需求旺盛。以
)作为重要的清洁燃料和合成化学的关键前驱体,在化工行业需求旺盛。以 为催化剂在水溶液中电催化二氧化碳还原为
为催化剂在水溶液中电催化二氧化碳还原为 和
和 的能量变化如图所示:
的能量变化如图所示:
 )作为重要的清洁燃料和合成化学的关键前驱体,在化工行业需求旺盛。以
)作为重要的清洁燃料和合成化学的关键前驱体,在化工行业需求旺盛。以 为催化剂在水溶液中电催化二氧化碳还原为
为催化剂在水溶液中电催化二氧化碳还原为 和
和 的能量变化如图所示:
的能量变化如图所示: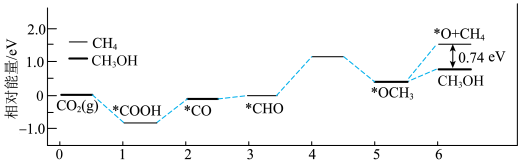
A.生成甲醇反应的决速步为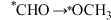 |
| B.两反应只涉及极性键的断裂和生成 |
| C.通过上图分析:甲烷比甲醇稳定 |
D.用 作催化剂可提高甲醇的选择性 作催化剂可提高甲醇的选择性 |
您最近一年使用:0次
名校
解题方法
2 . 已知反应: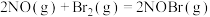
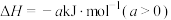 ,其反应机理如下:
,其反应机理如下:
①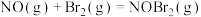
 快反应;
快反应;
②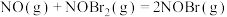
 慢反应。
慢反应。
下列说法不正确的是
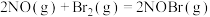
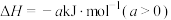 ,其反应机理如下:
,其反应机理如下:①
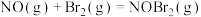
 快反应;
快反应;②
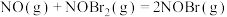
 慢反应。
慢反应。下列说法不正确的是
A.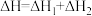 |
| B.该反应的反应速率主要取决于反应② |
| C.NOBr2是该反应的中间产物,不是催化剂 |
| D.恒容时,增大Br2(g)的浓度能增加单位体积内活化分子百分数,加快反应速率 |
您最近一年使用:0次
名校
解题方法
3 .  催化还原 NO是重要的烟气脱硝技术,其反应过程与能量关系如图1所示。研究发现,在催化剂上可能发生的反应过程如图2所示。下列说法正确的是
催化还原 NO是重要的烟气脱硝技术,其反应过程与能量关系如图1所示。研究发现,在催化剂上可能发生的反应过程如图2所示。下列说法正确的是
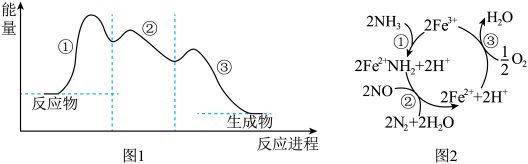
| A.图1三步反应中,第①步反应的活化能最大,为慢反应 |
B.图2中 催化剂 催化剂 |
| C.图2充入过量的O2有利于NO转化为 N2 |
D.图2脱硝的总反应为  |
您最近一年使用:0次
2024-01-22更新
|
69次组卷
|
2卷引用:四川省达州市2023-2024学年高二上学期期末监测化学试题
名校
4 .  与
与 在镍基催化剂催化作用下能发生如图所示的可逆反应,下列说法
在镍基催化剂催化作用下能发生如图所示的可逆反应,下列说法错误 的是

 与
与 在镍基催化剂催化作用下能发生如图所示的可逆反应,下列说法
在镍基催化剂催化作用下能发生如图所示的可逆反应,下列说法
| A.催化剂能降低反应的活化能,增大单位体积内的活化分子百分数 |
B.更换更高效的催化剂,能提高 的平衡转化率 的平衡转化率 |
C.图示反应过程中有 键的断裂与形成 键的断裂与形成 |
D.该过程的总反应为 |
您最近一年使用:0次
名校
5 . 甲酸常被用于橡胶、医药等工业。在一定条件下可分解生成 和
和 。在有、无催化剂条件下的能量与反应历程的关系如图所示。下列说法错误的是
。在有、无催化剂条件下的能量与反应历程的关系如图所示。下列说法错误的是

 和
和 。在有、无催化剂条件下的能量与反应历程的关系如图所示。下列说法错误的是
。在有、无催化剂条件下的能量与反应历程的关系如图所示。下列说法错误的是
| A.途径一与途径二甲酸平衡转化率相同 |
B.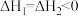 |
C.途径二 参与反应,通过改变反应途径,降低反应的活化能,加快反应速率 参与反应,通过改变反应途径,降低反应的活化能,加快反应速率 |
D.途径二反应的快慢由生成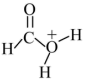 的速率决定 的速率决定 |
您最近一年使用:0次
名校
6 . “绿水青山就是金山银山”,运用化学反应原理研究碳、氮、硫的单质及其化合物的反应对缓解环境污染、能源危机具有重要意义。
(1)CO 还原 NO 的反应为 2CO(g)+ 2NO(g) 2CO2 (g)+ N2 (g) ∆H= -746kJ•mol-1,部分化学键的键能数据如下表(CO 以 C≡O 键构成):
2CO2 (g)+ N2 (g) ∆H= -746kJ•mol-1,部分化学键的键能数据如下表(CO 以 C≡O 键构成):
①由以上数据可求得 NO 的键能为___________ kJ·mol-1。
②写出两条有利于提高 NO 平衡转化率的措施___________ 。
(2)研究 之间的转化具有重要意义,下图能表示
之间的转化具有重要意义,下图能表示 之间转化历程。
之间转化历程。
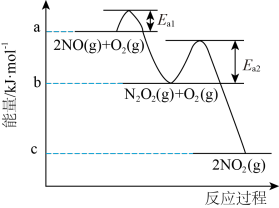
①写出图中所表示的总反应的热化学方程式___________ 。(用含a、b或c的代数式表示反应热 )
)
②上述总反应的决速步骤的活化能是________ (填写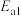 或
或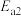 )。
)。
(3) 与
与 在高温下发生反应:
在高温下发生反应: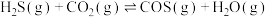
 。在610K时,将0.1mol
。在610K时,将0.1mol  与0.3mol
与0.3mol  充入2.5L的空钢瓶中(体积不变),经过10min,反应达到平衡,反应平衡时水蒸气的物质的量分数为0.125。
充入2.5L的空钢瓶中(体积不变),经过10min,反应达到平衡,反应平衡时水蒸气的物质的量分数为0.125。
①能判断该反应达到化学平衡状态的依据是___________ 。
A.容器中压强不变 B.容器中 的物质的量分数不变
的物质的量分数不变
C. D.容器中混合气体的密度不变
D.容器中混合气体的密度不变
②反应平衡常数K的值为___________ , 的平衡转化率α=
的平衡转化率α=_______ 。
③要增大该反应的平衡常数K,可采取的措施是___________ 。
(1)CO 还原 NO 的反应为 2CO(g)+ 2NO(g)
 2CO2 (g)+ N2 (g) ∆H= -746kJ•mol-1,部分化学键的键能数据如下表(CO 以 C≡O 键构成):
2CO2 (g)+ N2 (g) ∆H= -746kJ•mol-1,部分化学键的键能数据如下表(CO 以 C≡O 键构成):| 化学键 | C≡O | N≡N | C=O |
| E/(kJ·mol-1) | 1076 | 945 | 745 |
②写出两条有利于提高 NO 平衡转化率的措施
(2)研究
 之间的转化具有重要意义,下图能表示
之间的转化具有重要意义,下图能表示 之间转化历程。
之间转化历程。
①写出图中所表示的总反应的热化学方程式
 )
)②上述总反应的决速步骤的活化能是
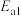 或
或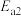 )。
)。(3)
 与
与 在高温下发生反应:
在高温下发生反应: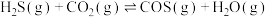
 。在610K时,将0.1mol
。在610K时,将0.1mol  与0.3mol
与0.3mol  充入2.5L的空钢瓶中(体积不变),经过10min,反应达到平衡,反应平衡时水蒸气的物质的量分数为0.125。
充入2.5L的空钢瓶中(体积不变),经过10min,反应达到平衡,反应平衡时水蒸气的物质的量分数为0.125。①能判断该反应达到化学平衡状态的依据是
A.容器中压强不变 B.容器中
 的物质的量分数不变
的物质的量分数不变C.
 D.容器中混合气体的密度不变
D.容器中混合气体的密度不变②反应平衡常数K的值为
 的平衡转化率α=
的平衡转化率α=③要增大该反应的平衡常数K,可采取的措施是
您最近一年使用:0次
名校
解题方法
7 . 已知反应S2O (aq)+2I-(aq)
(aq)+2I-(aq) 2SO
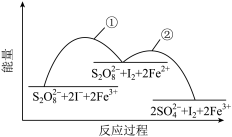
2SO (aq)+I2(aq),若向该溶液中加入含Fe3+的某溶液,反应机理如图所示。下列有关说法正确的是
(aq)+I2(aq),若向该溶液中加入含Fe3+的某溶液,反应机理如图所示。下列有关说法正确的是
 (aq)+2I-(aq)
(aq)+2I-(aq) 2SO
2SO (aq)+I2(aq),若向该溶液中加入含Fe3+的某溶液,反应机理如图所示。下列有关说法正确的是
(aq)+I2(aq),若向该溶液中加入含Fe3+的某溶液,反应机理如图所示。下列有关说法正确的是
| A.反应①②均为放热反应 |
| B.Fe2+是该反应的催化剂 |
| C.增大Fe3+浓度,能够加快反应速率 |
| D.若不加Fe3+,正反应的活化能比逆反应的活化能大 |
您最近一年使用:0次
名校
8 . 下列说法中正确的是
①熵增加且放热的反应一定是自发反应
②凡是放热反应都是自发的,吸热反应都是非自发的
③增大反应物浓度,可增大单位体积内活化分子数,从而使有效碰撞次数增多
④有气体参加的化学反应,若增大压强(即缩小反应容器的体积),可增大活化分子的百分数,从而使反应速率增大
⑤也能用固体或纯液体的变化量来表示反应快慢
⑥催化剂能增大活化分子百分数,从而增大化学反应速率
①熵增加且放热的反应一定是自发反应
②凡是放热反应都是自发的,吸热反应都是非自发的
③增大反应物浓度,可增大单位体积内活化分子数,从而使有效碰撞次数增多
④有气体参加的化学反应,若增大压强(即缩小反应容器的体积),可增大活化分子的百分数,从而使反应速率增大
⑤也能用固体或纯液体的变化量来表示反应快慢
⑥催化剂能增大活化分子百分数,从而增大化学反应速率
| A.①②③ | B.①③⑥ | C.①④⑤ | D.③⑤⑥ |
您最近一年使用:0次
名校
解题方法
9 . 已知反应: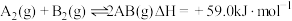 该反应的能量变化曲线如图所示。下列叙述正确的是
该反应的能量变化曲线如图所示。下列叙述正确的是

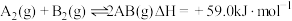 该反应的能量变化曲线如图所示。下列叙述正确的是
该反应的能量变化曲线如图所示。下列叙述正确的是
| A.使用催化剂只提高了单位体积的活化分子数,未提高活化分子的百分数 |
B.曲线Ⅰ未使用催化剂,每生成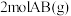 ,吸收 ,吸收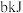 热量 热量 |
C.曲线Ⅱ使用了催化剂,使该反应的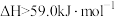 |
D.曲线Ⅰ未使用催化剂,该反应正反应的活化能为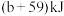 |
您最近一年使用:0次
名校
10 . 某密闭容器中发生反应X2(g)+3Y(g) Z(g)+W(g) ΔH,其反应进程和能量的变化如图所示:
Z(g)+W(g) ΔH,其反应进程和能量的变化如图所示:
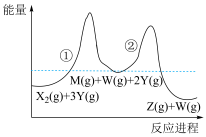
下列有关说法正确的是
 Z(g)+W(g) ΔH,其反应进程和能量的变化如图所示:
Z(g)+W(g) ΔH,其反应进程和能量的变化如图所示:
下列有关说法正确的是
| A.总反应快慢主要由反应②决定 |
| B.总反应的ΔH<0 |
| C.平衡后缩小容器容积,正反应速率增大,逆反应速率减小 |
| D.其他条件不变,加入X2(g),平衡向右移动,X2的平衡转化率增大 |
您最近一年使用:0次
2023-12-19更新
|
125次组卷
|
3卷引用:四川省绵阳南山实验中学2023-2024学年高二上学期期中考试化学试题



