解题方法
1 . 工业制硫酸的关键反应为
 ,在
,在 存在时,该反应的机理为:i.
存在时,该反应的机理为:i. (快);ii.
(快);ii.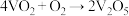 (慢)。下列说法正确的是
(慢)。下列说法正确的是

 ,在
,在 存在时,该反应的机理为:i.
存在时,该反应的机理为:i. (快);ii.
(快);ii.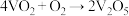 (慢)。下列说法正确的是
(慢)。下列说法正确的是| A.反应i的活化能比反应ii的活化能小 | B.反应i是决速步骤 |
| C.工业生产中应选择低温条件 | D. 是该反应的催化剂 是该反应的催化剂 |
您最近一年使用:0次
解题方法
2 . 已知:CO2氧化C2H6制C2H4的主反应热化学方程式为:C2H6(g)+CO2(g)=C2H4(g)+CO(g)+H2O(g) △H=+177kJ/mol。该反应的历程分为如下两步:
反应①:C2H6(g)=C2H4(g)+H2(g)(快反应) △H1
反应②:H2(g)+CO2(g)=CO(g)+H2O(g)(慢反应) △H2=+42kJ/mol
下列说法不正确的是
反应①:C2H6(g)=C2H4(g)+H2(g)(快反应) △H1
反应②:H2(g)+CO2(g)=CO(g)+H2O(g)(慢反应) △H2=+42kJ/mol
下列说法不正确的是
| A.反应①在高温条件下可以自发进行 |
B.相比于提高 ,提高c(C2H6)对主反应速率影响更大 ,提高c(C2H6)对主反应速率影响更大 |
C.将 液化分离,有利提高C2H6的转化率 液化分离,有利提高C2H6的转化率 |
D.反应①的活化能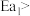 反应②的活化能 反应②的活化能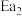 |
您最近一年使用:0次
解题方法
3 . 已知W→Z的能量变化与反应进程的关系如图所示:
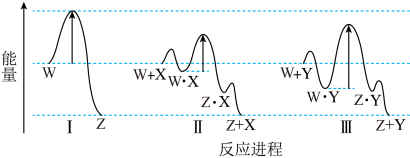
| A.生成Z的速率:Ⅲ>Ⅱ | B.平衡时W的转化率:Ⅰ=Ⅱ=Ⅲ |
| C.△H(Ⅰ)=△H(Ⅱ)=△H(Ⅲ) | D.X、Y分别参与了进程Ⅱ、Ⅲ的反应 |
您最近一年使用:0次
4 . CH4与CO2混合气体在催化剂表面会发生积碳反应和消碳反应。反应中催化剂活性会因积碳反应而降低,同时存在的消碳反应则使积碳量减少。在其余条件不变的情况下,该催化剂表面积碳量随温度升高呈现先增大后减小的变化。
下列关于升温过程中积碳、消碳反应的平衡常数(K),反应速率(v)以及催化剂的说法正确的是
| 积碳反应 | 消碳反应 | ||
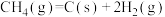 |  | ||
|  | 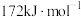 | |
| 活化能 | 催化剂M |  |  |
| 催化剂N | 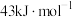 |  | |
| A.K积增加、K消减小 |
| B.v消增加倍数比v积增加倍数大 |
| C.K积减小倍数比K消减小倍数大 |
| D.催化剂M优于催化剂N |
您最近一年使用:0次
解题方法
5 . 下列说法不正确 的是
| A.增大反应物浓度,可增大单位体积内活化分子数目,从而使反应速率增大 |
| B.有气体参加的化学反应,若增大压强(即缩小反应容器的体积),不能增加活化分子的百分数 |
| C.活化分子间所发生的碰撞为有效碰撞 |
| D.升高温度能使化学反应速率增大的主要原因是增加了反应物中活化分子的百分数 |
您最近一年使用:0次
解题方法
6 . 多相催化反应是在催化剂表面通过吸附、解吸过程进行的。如图,我国学者发现T℃时,甲醇( )在铜基催化剂上的反应机理如下(该反应为可逆反应):
)在铜基催化剂上的反应机理如下(该反应为可逆反应):
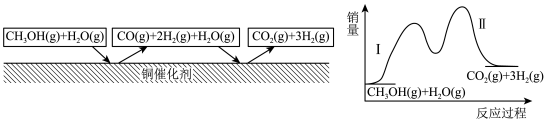
下列有关说法正确的是
 )在铜基催化剂上的反应机理如下(该反应为可逆反应):
)在铜基催化剂上的反应机理如下(该反应为可逆反应):
下列有关说法正确的是
| A.相同条件下,反应Ⅰ和反应Ⅱ相比,反应I的反应速率更快发生 |
B.反应Ⅰ为  |
| C.通过控制催化剂的用量可以控制反应的速率和反应进行的程度 |
D. 与 与 在高温条件下更容易反应 在高温条件下更容易反应 |
您最近一年使用:0次
名校
解题方法
7 .  可活化
可活化 放出
放出 ,其反应历程如图所示:
,其反应历程如图所示:

下列关于活化历程的说法正确的是
 可活化
可活化 放出
放出 ,其反应历程如图所示:
,其反应历程如图所示:
下列关于活化历程的说法正确的是
A.该转化过程 >0 >0 |
B.该反应过程中,最大能垒(活化能)为204.32 |
C.在此反应过程中 的成键数目未发生变化 的成键数目未发生变化 |
| D.整个过程中,Ni是该反应的催化剂 |
您最近一年使用:0次
名校
解题方法
8 .  催化剂光助一芬顿反应用于漂白有机染料的一种机理如图所示,其中包括①②光激发产生光电子与光生空穴(
催化剂光助一芬顿反应用于漂白有机染料的一种机理如图所示,其中包括①②光激发产生光电子与光生空穴( ,具有很强的得电子能力)、③④空穴氧化、⑥超氧自由基氧化、⑦光生电子还原铁离子等。下列说法正确的是
,具有很强的得电子能力)、③④空穴氧化、⑥超氧自由基氧化、⑦光生电子还原铁离子等。下列说法正确的是

 催化剂光助一芬顿反应用于漂白有机染料的一种机理如图所示,其中包括①②光激发产生光电子与光生空穴(
催化剂光助一芬顿反应用于漂白有机染料的一种机理如图所示,其中包括①②光激发产生光电子与光生空穴( ,具有很强的得电子能力)、③④空穴氧化、⑥超氧自由基氧化、⑦光生电子还原铁离子等。下列说法正确的是
,具有很强的得电子能力)、③④空穴氧化、⑥超氧自由基氧化、⑦光生电子还原铁离子等。下列说法正确的是
A.反应⑤每消耗1mol  ,共转移4mol ,共转移4mol  |
| B.反应⑨中双氧水将颜料直接氧化成无色物质 |
C.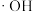 、 、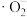 和 和 在漂白颜料时体现了强还原性 在漂白颜料时体现了强还原性 |
| D.催化剂可以降低反应活化能,提高单位体积内活化分子百分数 |
您最近一年使用:0次
2024-02-26更新
|
209次组卷
|
2卷引用:江西省五市九校协作体2023-2024学年高三上学期第一次联考化学试题
名校
解题方法
9 . 金属Ni可活化C2H6放出CH4,其反应历程如图所示:

下列说法正确的是

下列说法正确的是
| A.中间体1→中间体2的过程决定整个历程的反应速率 |
| B.加入催化剂可降低反应的活化能,加快反应速率 |
| C.整个历程中有碳碳键的断裂与形成 |
| D.中间体2→中间体3的过程是放热过程 |
您最近一年使用:0次
10 . 科学家通过密度泛函理论研究甲醇与水蒸气重整制氢反应机理时,得到甲醇在Pd(Ⅲ)表面发生解离时路径与相对能量关系如图所示,其中附在Pd(Ⅲ)表面的物种用*标注。下列说法错误的是

| A.②中包含C—H键的断裂过程 |
| B.该历程中反应活化能最小的是③ |
| C.该历程中制约反应速率的方程式为CO*+4H*→CO*+2H2 |
D.CH3OH(g) CO(g)+2H2(g)的反应热等于5个路径逆反应活化能之和与正反应活化能之和的差值 CO(g)+2H2(g)的反应热等于5个路径逆反应活化能之和与正反应活化能之和的差值 |
您最近一年使用:0次
2024-02-24更新
|
120次组卷
|
3卷引用:江苏省连云港市赣榆智贤中学2023-2024学年高二上学期第一次学情检测化学试题




