名校
1 . 工业制硫酸中的一步重要反应是SO2在400-500℃下的催化氧化:2SO2+O2 2SO3,该反应正向为放热反应。若反应在密闭容器中进行,下列有关说法正确的是
2SO3,该反应正向为放热反应。若反应在密闭容器中进行,下列有关说法正确的是
 2SO3,该反应正向为放热反应。若反应在密闭容器中进行,下列有关说法正确的是
2SO3,该反应正向为放热反应。若反应在密闭容器中进行,下列有关说法正确的是| A.使用催化剂是为了增大反应速率 |
| B.在上述条件下,SO2不可能100%转化为SO3 |
| C.达到平衡时,SO2的浓度与SO3的浓度一定相等 |
| D.将SO2通入BaCl2溶液中可生成BaSO3沉淀 |
您最近一年使用:0次
名校
2 . 下列四种溶液中,分别加入少量的固体二氧化锰,能产生气体的是
| A.3%的H2O2溶液 | B.1mol/L NaOH溶液 | C.1mol/L KClO3溶液 | D.0.1mol/L盐酸 |
您最近一年使用:0次
名校
3 . 某恒温恒容密闭容器中发生反应: 。下列叙述正确的是
。下列叙述正确的是
 。下列叙述正确的是
。下列叙述正确的是| A.充入氩气,反应速率减小 | B.增大 的质量,平衡常数增大 的质量,平衡常数增大 |
C.充入 ,反应速率不变 ,反应速率不变 | D.加入催化剂,平衡不移动 |
您最近一年使用:0次
2023-12-01更新
|
78次组卷
|
2卷引用:海南省海南华侨中学 海南省农垦中学2023-2024学年高二上学期11月学业水平测试期中联考化学试题
名校
解题方法
4 . 在合成氨工业中,为增加NH3的日产量,下列措施与平衡移动无关的是
| A.不断将氨分离出来 |
| B.使用催化剂 |
| C.采用450℃左右的高温而不是650℃的高温 |
| D.采用10Mpa—30Mpa的压强 |
您最近一年使用:0次
2022-11-09更新
|
29次组卷
|
2卷引用:海南省海口市第四中学2023-2024学年高二上学期11月期中考试化学试题
5 . 研究CO2、H2的开发利用意义重大。一定条件下发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g),反应过程中的能量变化情况如图所示。请按要求回答下列问题:
CH3OH(g)+H2O(g),反应过程中的能量变化情况如图所示。请按要求回答下列问题:
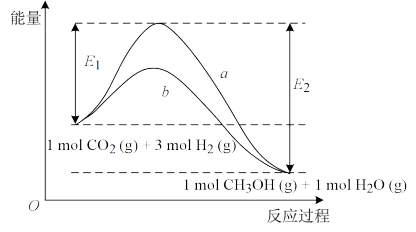
(1)曲线a和曲线b分别表示不使用催化剂和使用催化剂的两种情况。该反应是___ (填“吸热”或“放热”)反应。计算当反应生成2molCH3OH(g)时能量变化是___ (用E1、E2表示)。
(2)选择适宜的催化剂是___ (填“能”或“不能”)改变该反应的能量变化。
(3)下列说法一定正确的是___ (填选项字母)。
A.a与b相比,a表示的反应速度较大
B.反应物断裂化学键吸收的总能量小于生成物形成化学键释放的总能量
C.CO2(g)和H2(g)所具有的总能量一定高于CH3OH(g)和H2O(g)所具有的总能量
(4)推测反应CH3OH(g)+H2O(g) CO2(g)+3H2(g)是
CO2(g)+3H2(g)是___ (填“吸热”或“放热”)反应。
 CH3OH(g)+H2O(g),反应过程中的能量变化情况如图所示。请按要求回答下列问题:
CH3OH(g)+H2O(g),反应过程中的能量变化情况如图所示。请按要求回答下列问题: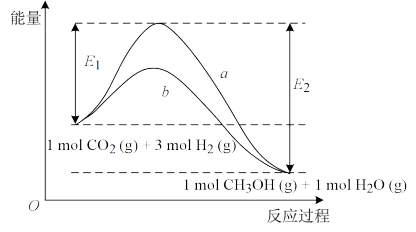
(1)曲线a和曲线b分别表示不使用催化剂和使用催化剂的两种情况。该反应是
(2)选择适宜的催化剂是
(3)下列说法一定正确的是
A.a与b相比,a表示的反应速度较大
B.反应物断裂化学键吸收的总能量小于生成物形成化学键释放的总能量
C.CO2(g)和H2(g)所具有的总能量一定高于CH3OH(g)和H2O(g)所具有的总能量
(4)推测反应CH3OH(g)+H2O(g)
 CO2(g)+3H2(g)是
CO2(g)+3H2(g)是
您最近一年使用:0次
6 . 控制变量法是化学实验的常用方法之一,下图所示实验探究影响反应速率的因素是


| A.催化剂 | B.温度 |
| C.压强 | D.浓度 |
您最近一年使用:0次
2019-11-05更新
|
208次组卷
|
4卷引用:海南省东方市八所中学2018-2019学年高一下学期期中联考化学试题



