2021·浙江·模拟预测
解题方法
1 . 下列实验方案设计、现象与结论都正确的是
| 实验目的 | 方案设计 | 现象和结论 | |
| A | 探究Fe2+、Cu2+对H2O2溶液分解的催化效果强弱 | 在两支试管a、b中各加2 mL5%H2O2溶液,分别滴入0.1 mol•L-1FeCl3溶液和0.1 mol•L-1CuSO4溶液各0.5 mL | 若a中产生气泡快于b中,则说明Fe3+的催化效果强于Cu2+ |
| B | 探究Fe与水蒸气高温反应后固体产物中铁元素的化合价 | 取少量固体产物于试管中,加足量的稀硫酸溶解,分成两份:一份滴加几滴KSCN溶液,另一份少量滴加KMnO4溶液 | 若前者溶液变血红色,后者溶液紫色褪去,则固体产物中铁元素有+2、+3两种价态 |
| C | 探究油脂在碱性条件下的水解 | 在小烧杯中加入约5 g动物脂肪、6 mL95%的乙醇,再加入6 mL 40%的氢氧化钠溶液,微热一段时间后取少量溶液,加入新制氢氧化铜 | 若出现绛蓝色,则油脂已发生水解 |
| D | 探究Cu与硫酸的 反应 | 铜粉加入稀硫酸中,加热,再加入少量KNO3固体 | 未加KNO3固体前,无明显现象;加入KNO3固体后,产生大量气泡,则说明KNO3起催化作用 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
2 . 合成氨在国民经济中占有十分重要的地位。
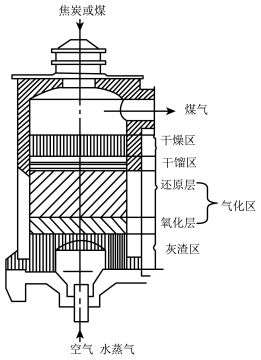
(1)制备原料气阶段:以煤、焦炭、水蒸气、空气为原料在如图反应器中合成氢气。
氧化层中进行的反应:
Ⅰ、 ,
,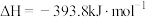
Ⅱ、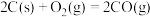 ,
,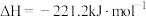
还原层中进行的反应:
Ⅲ、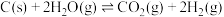 ,
,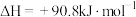
Ⅳ、 ,
,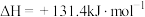
①在还原层中 在产物中的体积分数为
在产物中的体积分数为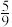 ,写出反应的热化学方程式:
,写出反应的热化学方程式:___________ 。
②下列说法正确的是___________
A.氧化层能维持炉中的反应温度
B.升温可提高还原区 的平衡选择性,减少CO的排放
的平衡选择性,减少CO的排放
C.氧化区中的反应 、
、 。
。
D.若通入的 ,后续必须要补充
,后续必须要补充 才可作为制氨的原料气
才可作为制氨的原料气
(2)氨的合成阶段:气固相合成催化
①氨合成阶段 在低温时主要由速率控制
在低温时主要由速率控制 的产率,已知在接近平衡时:
的产率,已知在接近平衡时: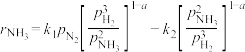 (
(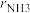 —氨合成反应的净速率;
—氨合成反应的净速率; ,
, —正、逆反应速率常数;
—正、逆反应速率常数;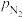 ,
,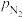 ,
, —
— ,
, ,
, 的分压;
的分压; 为常数,与催化剂有关,经实验测定以铁为主的氨合成催化剂
为常数,与催化剂有关,经实验测定以铁为主的氨合成催化剂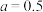 ,试用
,试用 ,
, 表示氨合成反应的平衡常数
表示氨合成反应的平衡常数
___________ )。
②已知,320℃恒温1L的容器中通入一定量的 和
和 ,
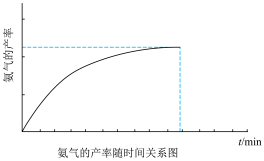
, 的产率随时间变化关系如图所示。起始温度为320℃绝热1L的容器中通入与恒温时相同量的
的产率随时间变化关系如图所示。起始温度为320℃绝热1L的容器中通入与恒温时相同量的 和
和 在
在 时刻达到平衡后,调整装置保持320℃,在
时刻达到平衡后,调整装置保持320℃,在 时刻重新达到平衡。画出投料后到
时刻重新达到平衡。画出投料后到 时刻容器内的
时刻容器内的 的产率随时间变化关系曲线
的产率随时间变化关系曲线___________ 。
(3)氨水催化吸收 是小型合成氨厂广泛采用的脱硫方法。原料气中
是小型合成氨厂广泛采用的脱硫方法。原料气中 在脱硫塔中被氨吸收得到
在脱硫塔中被氨吸收得到 。补充完成在吸收液中添加对苯二酚(作为载氧体和催化剂),回收单质硫的化学方程式。
。补充完成在吸收液中添加对苯二酚(作为载氧体和催化剂),回收单质硫的化学方程式。
Ⅰ: Ⅱ:
Ⅱ:___________
(1)制备原料气阶段:以煤、焦炭、水蒸气、空气为原料在如图反应器中合成氢气。
氧化层中进行的反应:

Ⅰ、
 ,
,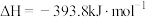
Ⅱ、
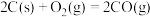 ,
,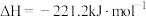
还原层中进行的反应:
Ⅲ、
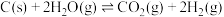 ,
,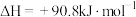
Ⅳ、
 ,
,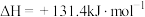
①在还原层中
 在产物中的体积分数为
在产物中的体积分数为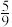 ,写出反应的热化学方程式:
,写出反应的热化学方程式:②下列说法正确的是
A.氧化层能维持炉中的反应温度
B.升温可提高还原区
 的平衡选择性,减少CO的排放
的平衡选择性,减少CO的排放C.氧化区中的反应
 、
、 。
。D.若通入的
 ,后续必须要补充
,后续必须要补充 才可作为制氨的原料气
才可作为制氨的原料气(2)氨的合成阶段:气固相合成催化
①氨合成阶段
 在低温时主要由速率控制
在低温时主要由速率控制 的产率,已知在接近平衡时:
的产率,已知在接近平衡时: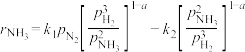 (
(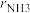 —氨合成反应的净速率;
—氨合成反应的净速率; ,
, —正、逆反应速率常数;
—正、逆反应速率常数;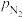 ,
,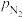 ,
, —
— ,
, ,
, 的分压;
的分压; 为常数,与催化剂有关,经实验测定以铁为主的氨合成催化剂
为常数,与催化剂有关,经实验测定以铁为主的氨合成催化剂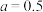 ,试用
,试用 ,
, 表示氨合成反应的平衡常数
表示氨合成反应的平衡常数
②已知,320℃恒温1L的容器中通入一定量的
 和
和 ,
, 的产率随时间变化关系如图所示。起始温度为320℃绝热1L的容器中通入与恒温时相同量的
的产率随时间变化关系如图所示。起始温度为320℃绝热1L的容器中通入与恒温时相同量的 和
和 在
在 时刻达到平衡后,调整装置保持320℃,在
时刻达到平衡后,调整装置保持320℃,在 时刻重新达到平衡。画出投料后到
时刻重新达到平衡。画出投料后到 时刻容器内的
时刻容器内的 的产率随时间变化关系曲线
的产率随时间变化关系曲线
(3)氨水催化吸收
 是小型合成氨厂广泛采用的脱硫方法。原料气中
是小型合成氨厂广泛采用的脱硫方法。原料气中 在脱硫塔中被氨吸收得到
在脱硫塔中被氨吸收得到 。补充完成在吸收液中添加对苯二酚(作为载氧体和催化剂),回收单质硫的化学方程式。
。补充完成在吸收液中添加对苯二酚(作为载氧体和催化剂),回收单质硫的化学方程式。Ⅰ:
 Ⅱ:
Ⅱ:
您最近一年使用:0次



