1 . 下列实验目的或结论及操作、现象均正确的是
选项 | 实验操作及现象 | 目的或结论 |
A | 称取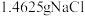 ,置于 ,置于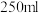 容量瓶中,加水至刻度线 容量瓶中,加水至刻度线 | 配制 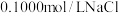 溶液 溶液 |
B | 向某溶液中加入浓 溶液并加热,能产生使湿润的红色石蕊试纸变蓝的气体 溶液并加热,能产生使湿润的红色石蕊试纸变蓝的气体 | 溶液中含有 |
C | 向 溶液中同时通入 溶液中同时通入 和 和 ,产生白色沉淀 ,产生白色沉淀 |  将 将 氧化成了 氧化成了 |
D | 向体积和浓度均相同的 中分别加入等体积的 中分别加入等体积的 的 的 和 和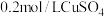 溶液 溶液 | 验证 、 、 对 对 催化分解速率的影响 |
| A. | B.B | C.C | D.D |
您最近一年使用:0次
名校
2 . 根据实验目的,下列实验现象、结论都正确的是
| 选项 | 实验目的 | 实验过程 | 现象及结论 |
| A | 测定中和反应的反应热 | 测定浓度均为1.0  和 和 溶液初始温度 溶液初始温度 。快速将体积均为100 。快速将体积均为100 的 的 和 和 溶液倒入量热计中,盖好杯盖,轻轻搅拌,记录体系的最高温度 溶液倒入量热计中,盖好杯盖,轻轻搅拌,记录体系的最高温度 。 。 |  和 和 溶液密度近似为1 溶液密度近似为1 ,溶液的比热容4.18 ,溶液的比热容4.18 。中和反应的反应热: 。中和反应的反应热: 。 。 |
| B | 探究铁钉镀铜 | 直流电源正极、负极分别与铁钉、铜片连接,将铁钉和铜片插入 溶液中,接通电源。 溶液中,接通电源。 | 铜片逐渐溶解,铁钉表面有红色物质析出。 |
| C | 探究浓度对化学平衡的影响 | 向 溶液中缓慢滴加硫酸,溶液由黄色变为橙色。 溶液中缓慢滴加硫酸,溶液由黄色变为橙色。 | 增大 浓度,化学平衡向生成 浓度,化学平衡向生成 的方向移动。 的方向移动。 |
| D | 探究不同催化剂的催化效果 | 向两支试管中各加入2 10% 10% 溶液,再分别加入2滴1 溶液,再分别加入2滴1  溶液、2滴1 溶液、2滴1  溶液。 溶液。 | 滴加 溶液的试管产生气泡的速率快,说明 溶液的试管产生气泡的速率快,说明 的催化效果好。 的催化效果好。 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-11-12更新
|
129次组卷
|
2卷引用:河南省郑州市十校联考2023-2024学年高二上学期期中考试化学试题
解题方法
3 . 下列操作中,实验现象与得出的结论不一致的是
| 选项 | 实验目的 | 操作及现象 | 结论 |
| A | 验证Mn2+在KMnO4溶液与 H2C2O4溶液反应中的催化作用 | 取两支洁净的试管各加入5 mL硫酸酸化的0.1mol·L-1KMnO4溶液,在两支试管中分别再加入:①10 mL0.1 mol· L-1 H2C2O4溶液与2 mL MnSO4 溶液;②10 mL 0.1 mol·L-1 H2C2O4溶液与2 mL蒸馏水。加入①的试管紫色先消失 | 证明Mn2+能降低该反应的活化能 |
| B | 判断Ksp(AgCl)与Ksp(AgI)的大小 | 向AgCl悬浊液中加入NaI溶液时白色沉淀转化为黄色沉淀 | Ksp(AgCl)> Ksp(AgI) |
| C | 判断CH3COO-与 水解常数的大小 水解常数的大小 | 相同温度下,分别测定浓度均为0.1 mol·L-1的CH3COONa溶液和Na2CO3溶液的pH,后者大于前者 | 水解常数: Kh(CH3COO- ) <Kh( ) ) |
| D | 判断某FeCl3溶液样品中是否含有Fe2+ | 向某FeCl3溶液样品中加入硫酸酸化的KMnO4溶液,紫色褪去 | 该样品中一定含有Fe2+ |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-08-08更新
|
743次组卷
|
2卷引用:四川省眉山市仁寿县铧强中学2021-2022学年高二下学期期中考试化学试题
解题方法
4 . 下列实验操作和现象与预期实验目的或所得结论不一致的是
| 选项 | 实验操作和现象 | 预期实验目的或所得结论 |
| A | 将酸性KMnO4溶液滴入丙烯醛中,溶液的紫红色褪去 | 不能说明丙烯醛中含有碳碳双键 |
| B | 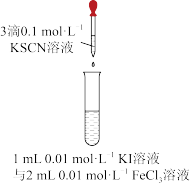 现象为溶液变红 | 证明化学反应存在一定的限度 |
| C | 相同条件下,在两支试管中各加入3mL6%的H2O2溶液,再向H2O2溶液中分别滴入1mLH2O和1mLFeCl3溶液,观察并比较H2O2的分解速率 | 探究催化剂对H2O2分解速率的影响 |
| D | 向2mL甲苯中加入3滴酸性KMnO4溶液,振荡,紫色褪去;向2mL苯中加入3滴酸性KMnO4溶液,振荡,紫色没有褪去 | 证明与苯环相连的甲基易被氧化 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
5 . 下列装置能达到对应实验目的的是


| A.可根据最终气球的大小判断反应速率的大小 |
B.探究温度对[Cu(H2O)4]2++4Cl- [CuCl4]2-+4H2O平衡的影响 [CuCl4]2-+4H2O平衡的影响 |
| C.探究KMnO4浓度对化学反应速率的影响 |
D.探究浓度对Fe3++3SCN- Fe(SCN)3平衡的影响 Fe(SCN)3平衡的影响 |
您最近一年使用:0次
2023-11-03更新
|
274次组卷
|
2卷引用:四川省成都市彭州市2023-2024学年高二上学期期中考试化学试题
解题方法
6 . 下列操作规范且能达到实验目的的是


| A.若装置I中反应速率①>②,可以验证Fe3+的催化效果比Cu2+好 |
B.由装置II中颜色的变化可以判断反应N2O4(g) 2NO2(g) △H>0 2NO2(g) △H>0 |
| C.可通过装置III测定反应速率的大小 |
| D.可用装置IV来测定醋酸的浓度 |
您最近一年使用:0次
2022-11-13更新
|
158次组卷
|
2卷引用:山东省日照市2022-2023学年高二上学期期中校际联考化学试题
名校
解题方法
7 .  是一种绿色氧化还原试剂,在化学研究中应用广泛。
是一种绿色氧化还原试剂,在化学研究中应用广泛。
(一)A实验小组拟在同浓度 的催化下,探究
的催化下,探究 浓度对
浓度对 分解反应速率的影响。
分解反应速率的影响。
(1)写出本实验 分解反应方程式并标明电子转移的方向和数目:
分解反应方程式并标明电子转移的方向和数目:___________ 。
(2)设计实验方案:在不同 浓度下,测定
浓度下,测定___________ (要求所测得的数据能直接体现反应速率大小)。
(二)B实验小组在验证 氧化
氧化 时发现异常现象,并进行了深入探究。
时发现异常现象,并进行了深入探究。
实验Ⅰ:
(3)实验Ⅰ中溶液变红的原因是___________ 。(请用离子方程式表示其原理)
(4)探究实验Ⅰ中红色褪去的原因:取反应后溶液,___________ (填实验操作和现象),证明溶液中有 ,而几乎无
,而几乎无 。
。
(5)查阅资料发现,酸性溶液中 能氧化
能氧化 ,但反应很慢且无明显现象,
,但反应很慢且无明显现象, 对该反应没影响。实验Ⅰ中褪色相对较快,由此推测
对该反应没影响。实验Ⅰ中褪色相对较快,由此推测 在酸性溶液中能加快
在酸性溶液中能加快 与
与 的反应。通过实验Ⅱ和Ⅲ得到了证实。参照实验Ⅱ的图例,补全实验Ⅲ加入的试剂和现象。
的反应。通过实验Ⅱ和Ⅲ得到了证实。参照实验Ⅱ的图例,补全实验Ⅲ加入的试剂和现象。
实验Ⅱ:

实验Ⅲ:
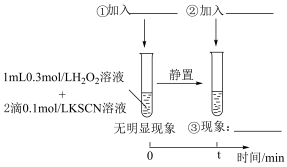
①___________ ;②___________ ;③___________ 。
(三)C实验小组猜测, 会否也能加快
会否也能加快 与
与 的反应。通过实验Ⅱ和Ⅳ得到了证实。
的反应。通过实验Ⅱ和Ⅳ得到了证实。
(6)实验Ⅳ:
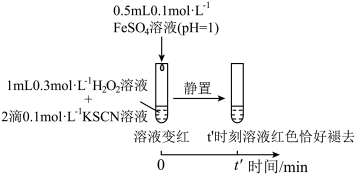
实验得知,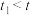 ,对比实验Ⅱ和Ⅳ得到结论:在本实验条件下,
,对比实验Ⅱ和Ⅳ得到结论:在本实验条件下,___________ 。
 是一种绿色氧化还原试剂,在化学研究中应用广泛。
是一种绿色氧化还原试剂,在化学研究中应用广泛。(一)A实验小组拟在同浓度
 的催化下,探究
的催化下,探究 浓度对
浓度对 分解反应速率的影响。
分解反应速率的影响。(1)写出本实验
 分解反应方程式并标明电子转移的方向和数目:
分解反应方程式并标明电子转移的方向和数目:(2)设计实验方案:在不同
 浓度下,测定
浓度下,测定(二)B实验小组在验证
 氧化
氧化 时发现异常现象,并进行了深入探究。
时发现异常现象,并进行了深入探究。实验Ⅰ:
| 装置与操作 | 现象 |
 | 溶液立即变红,继续滴加 溶液,红色变浅并逐渐褪去 溶液,红色变浅并逐渐褪去 |
(4)探究实验Ⅰ中红色褪去的原因:取反应后溶液,
 ,而几乎无
,而几乎无 。
。(5)查阅资料发现,酸性溶液中
 能氧化
能氧化 ,但反应很慢且无明显现象,
,但反应很慢且无明显现象, 对该反应没影响。实验Ⅰ中褪色相对较快,由此推测
对该反应没影响。实验Ⅰ中褪色相对较快,由此推测 在酸性溶液中能加快
在酸性溶液中能加快 与
与 的反应。通过实验Ⅱ和Ⅲ得到了证实。参照实验Ⅱ的图例,补全实验Ⅲ加入的试剂和现象。
的反应。通过实验Ⅱ和Ⅲ得到了证实。参照实验Ⅱ的图例,补全实验Ⅲ加入的试剂和现象。实验Ⅱ:

实验Ⅲ:

①
(三)C实验小组猜测,
 会否也能加快
会否也能加快 与
与 的反应。通过实验Ⅱ和Ⅳ得到了证实。
的反应。通过实验Ⅱ和Ⅳ得到了证实。(6)实验Ⅳ:

实验得知,
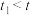 ,对比实验Ⅱ和Ⅳ得到结论:在本实验条件下,
,对比实验Ⅱ和Ⅳ得到结论:在本实验条件下,
您最近一年使用:0次
2023-10-19更新
|
162次组卷
|
2卷引用:广东省广州市执信中学2023-2024学年高二上学期11月期中考试化学试题
8 . 化学实验是研究化学反应原理的途径之一、回答下列问题:
(1)实验一:中和反应热的测定
用50mL 盐酸与50mL
盐酸与50mL NaOH溶液在如图所示的装置中进行反应。通过测定反应过程中所放出的热量可计算中和反应的反应热。
NaOH溶液在如图所示的装置中进行反应。通过测定反应过程中所放出的热量可计算中和反应的反应热。

①指出装置存在的一处错误___________ 。
②已知中和后生成的溶液的比热容c为 ,溶液的密度约为
,溶液的密度约为 ,某学习小组三次实验测得温度平均升高了3.5℃。可计算出生成1mol
,某学习小组三次实验测得温度平均升高了3.5℃。可计算出生成1mol 时的反应热
时的反应热
___________ kJ/mol。(结果保留一位小数)
③经计算,得到生成1mol 时放出的热量大于57.3kJ,产生偏差的原因可能是
时放出的热量大于57.3kJ,产生偏差的原因可能是___________ (填标号)。
a.实验装置保温、隔热效果差
b.量取盐酸的体积时仰视读数
c.分多次把NaOH溶液倒入盛有盐酸的内筒中
d.用温度计测定盐酸起始温度后直接测定NaOH溶液的温度
(2)实验二:探究影响化学反应速率的因素
为比较不同催化剂对 分解的催化效果,某实验小组设计了如图所示的实验。
分解的催化效果,某实验小组设计了如图所示的实验。

 对
对 的催化机理分两步进行,请写出第一步反应的离子方程式:
的催化机理分两步进行,请写出第一步反应的离子方程式:
①___________ 。
② 。
。
实验发现左边试管中产生气泡的速率更快,所得实验结论是___________ 。
(3)实验三:探究影响化学平衡移动的因素
①往2mL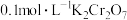 溶液中加入5~10滴
溶液中加入5~10滴 NaOH溶液,实验现象为
NaOH溶液,实验现象为___________ ,原因是 溶液中存在平衡体系:
溶液中存在平衡体系:___________ 。(用离子方程式表示),NaOH消耗量了 ,使平衡正向移动。
,使平衡正向移动。
②取少量 溶液于一支试管中加热,溶液由蓝色变为黄色,这表明升高温度使:
溶液于一支试管中加热,溶液由蓝色变为黄色,这表明升高温度使:___________ (用离子方程式表示)的平衡正向移动。
(1)实验一:中和反应热的测定
用50mL
 盐酸与50mL
盐酸与50mL NaOH溶液在如图所示的装置中进行反应。通过测定反应过程中所放出的热量可计算中和反应的反应热。
NaOH溶液在如图所示的装置中进行反应。通过测定反应过程中所放出的热量可计算中和反应的反应热。
①指出装置存在的一处错误
②已知中和后生成的溶液的比热容c为
 ,溶液的密度约为
,溶液的密度约为 ,某学习小组三次实验测得温度平均升高了3.5℃。可计算出生成1mol
,某学习小组三次实验测得温度平均升高了3.5℃。可计算出生成1mol 时的反应热
时的反应热
③经计算,得到生成1mol
 时放出的热量大于57.3kJ,产生偏差的原因可能是
时放出的热量大于57.3kJ,产生偏差的原因可能是a.实验装置保温、隔热效果差
b.量取盐酸的体积时仰视读数
c.分多次把NaOH溶液倒入盛有盐酸的内筒中
d.用温度计测定盐酸起始温度后直接测定NaOH溶液的温度
(2)实验二:探究影响化学反应速率的因素
为比较不同催化剂对
 分解的催化效果,某实验小组设计了如图所示的实验。
分解的催化效果,某实验小组设计了如图所示的实验。
 对
对 的催化机理分两步进行,请写出第一步反应的离子方程式:
的催化机理分两步进行,请写出第一步反应的离子方程式:①
②
 。
。实验发现左边试管中产生气泡的速率更快,所得实验结论是
(3)实验三:探究影响化学平衡移动的因素
①往2mL
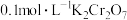 溶液中加入5~10滴
溶液中加入5~10滴 NaOH溶液,实验现象为
NaOH溶液,实验现象为 溶液中存在平衡体系:
溶液中存在平衡体系: ,使平衡正向移动。
,使平衡正向移动。②取少量
 溶液于一支试管中加热,溶液由蓝色变为黄色,这表明升高温度使:
溶液于一支试管中加热,溶液由蓝色变为黄色,这表明升高温度使:
您最近一年使用:0次
名校
解题方法
9 . 过氧化氢(H2O2)是常用的绿色氧化剂。某化学兴趣小组查阅了H2O2的相关信息,并针对它的某些性质进行了探究,具体如下:H2O2可以通过H2和O2在某催化剂表面直接反应合成,具体原理如下图所示:

(1)采用同位素示踪法研究催化剂中H+的作用:将H2用D2(2H2)代替再进行实验。催化剂中氢离子参与反应的证据是生成的产物中有H2O2或_______ 粒子(填化学式)。
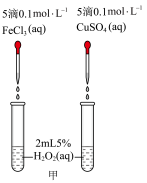
II.H2O2不稳定,在Fe3+、Cu2+等粒子的催化下会很快分解并放出热量。为了比较Fe3+和Cu2+对H2O2分解的催化效果,设计了如下实验。
(2)定性分析:通过观察甲装置两支试管中_______ 的现象,得出关于FeCl3和CuSO4催化效果的结论。某同学认为此方案还需要进一步控制变量,提出可将试剂CuSO4更换为_______ (填化学式)。
(3)定量测定:用乙装置进行定量实验。实验时组装好装置乙,关闭分液漏斗的活塞,将注射器活塞向外拉出一段距离后松开,观察活塞是否回到原来的位置。该操作的实验目的是_______ 。若反应30s后注射器中收集到气体的体积为VmL(标准状况),则锥形瓶A中实际产生气体的体积_______ VmL(填“>”、“<”或“=”)。
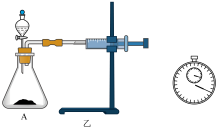
III.H2O2既有氧化性,又有还原性。
(4)H2O2可以氧化废水中的CN—,Cu2+可催化该反应。已知H2O2与CN—反应会生成参与大气循环的无毒气体。氰化氢(HCN)是一种易挥发的弱酸,有剧毒,对环境危害很大。
①H2O2与CN-的反应不能在酸性溶液中进行,原因是_______ ,反应生成气体的化学式为_______ 。
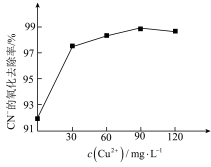
②一定条件下,测得CN-的氧化去除率随溶液中c(Cu2+)的变化如下图所示。c(Cu2+)过多时,CN-的氧化去除率有所下降,原因是_______ 。
(5)取少量84消毒液(有效成分为NaClO)于试管中,滴加H2O2溶液,产生大量无色气体。写出发生反应的化学方程式_______ 。

(1)采用同位素示踪法研究催化剂中H+的作用:将H2用D2(2H2)代替再进行实验。催化剂中氢离子参与反应的证据是生成的产物中有H2O2或
II.H2O2不稳定,在Fe3+、Cu2+等粒子的催化下会很快分解并放出热量。为了比较Fe3+和Cu2+对H2O2分解的催化效果,设计了如下实验。
(2)定性分析:通过观察甲装置两支试管中

(3)定量测定:用乙装置进行定量实验。实验时组装好装置乙,关闭分液漏斗的活塞,将注射器活塞向外拉出一段距离后松开,观察活塞是否回到原来的位置。该操作的实验目的是

III.H2O2既有氧化性,又有还原性。
(4)H2O2可以氧化废水中的CN—,Cu2+可催化该反应。已知H2O2与CN—反应会生成参与大气循环的无毒气体。氰化氢(HCN)是一种易挥发的弱酸,有剧毒,对环境危害很大。
①H2O2与CN-的反应不能在酸性溶液中进行,原因是
②一定条件下,测得CN-的氧化去除率随溶液中c(Cu2+)的变化如下图所示。c(Cu2+)过多时,CN-的氧化去除率有所下降,原因是

(5)取少量84消毒液(有效成分为NaClO)于试管中,滴加H2O2溶液,产生大量无色气体。写出发生反应的化学方程式
您最近一年使用:0次
10 . 用如图装置进行铜与稀硝酸反应的实验。开始反应阶段几乎不产生气泡,约2分钟后,铜表面产生无色气泡,5分钟后产生气体逐渐变快,溶液变为蓝色,液面上方气体变为浅红棕色。

A.铜与稀硝酸反应生成的气体为 和 和 |
| B.根据实验现象推测,铜与稀硝酸反应时可能吸收热量 |
C.根据实验现象推测, 或 或 可能为铜与稀硝酸反应的催化剂 可能为铜与稀硝酸反应的催化剂 |
| D.当试管中的反应停止后,向试管中加入稀硫酸,铜丝表面一定无现象 |
您最近一年使用:0次
2021-07-12更新
|
292次组卷
|
2卷引用:北京市第二十七中学2021-2022学年高一下学期期中考试化学试题



