1 . 为了深入探究某个化学问题,往往需要我们会依据一定的原理作出假设,并设计一定的化学实验方案。某化学兴趣小组的同学,对实验室制备氧气的若干问题进行如下探究:
[探究一]为探究影响双氧水分解速率的某种因素,A小组记录了如下实验数据:
(1)写出本实验中反应的化学方程式为___________ ;测量 体积的装置是
体积的装置是___________ (选填下图1中的装置编号)。
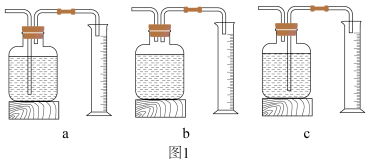
(2)由实验I、Ⅱ、Ⅲ可知:影响双氧水分解速率的因素是:___________
[探究二]B小组查阅资料:在过氧化氢溶液的分解反应中,氧化铜也能作催化剂。于是他们用天平称量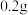 氧化铜,取5%过氧化氢溶液
氧化铜,取5%过氧化氢溶液 于试管中,进行如图2实验:
于试管中,进行如图2实验:
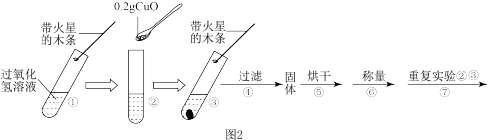
(3)填表:
(4)步骤①的目的是___________ 。
(5)步骤④需用到的玻璃仪器有铁架台(带铁圈)、烧杯、___________ 、___________ 。
(6)步骤⑦中应选用___________ 的过氧化氢溶液。
(7)过氧化氢能将二氧化硫氧化,请写出离子方程式为___________ 。
[探究一]为探究影响双氧水分解速率的某种因素,A小组记录了如下实验数据:
| 双氧水的质量 | 双氧水的浓度 |  的质量 的质量 | 相同时间内产生 的体积 的体积 | |
| I | 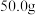 | 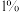 |  |  |
| Ⅱ | 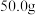 |  |  | 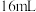 |
| Ⅲ | 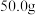 | 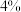 |  | 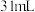 |
(1)写出本实验中反应的化学方程式为
 体积的装置是
体积的装置是
(2)由实验I、Ⅱ、Ⅲ可知:影响双氧水分解速率的因素是:
[探究二]B小组查阅资料:在过氧化氢溶液的分解反应中,氧化铜也能作催化剂。于是他们用天平称量
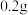 氧化铜,取5%过氧化氢溶液
氧化铜,取5%过氧化氢溶液 于试管中,进行如图2实验:
于试管中,进行如图2实验:
(3)填表:
| 步骤③现象 | 步骤⑥结果 | 步骤⑦现象 | 结论 |
| 称得氧化铜的质量为 | 将固体加入盛有过氧化氢溶液的试管中,并把带火星的木条伸入试管,观察现象。 | 在过氧化氢溶液的分解实验中,氧化铜也能作催化剂。 |
(4)步骤①的目的是
(5)步骤④需用到的玻璃仪器有铁架台(带铁圈)、烧杯、
(6)步骤⑦中应选用
(7)过氧化氢能将二氧化硫氧化,请写出离子方程式为
您最近一年使用:0次
2 . 通过以下实验装置,不能达到实验目的的是
|
|
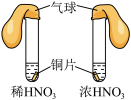
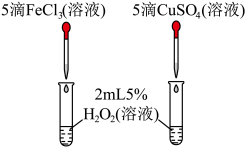
| A.通过气球膨胀速率比较浓硝酸和稀硝酸的氧化性强弱 | B.通过试管中气泡产生速率比较 和 和 的催化效率高低 的催化效率高低 |
|
|
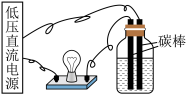
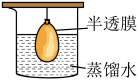
| C.通过小灯泡亮度判断不同浓度NaCl溶液的导电性强弱 | D.通过以上装置分离NaCl溶液和 胶体 胶体 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
3 . 下列操作规范且能达到实验目的的是


| A.若装置I中反应速率①>②,可以验证Fe3+的催化效果比Cu2+好 |
B.由装置II中颜色的变化可以判断反应N2O4(g) 2NO2(g) △H>0 2NO2(g) △H>0 |
| C.可通过装置III测定反应速率的大小 |
| D.可用装置IV来测定醋酸的浓度 |
您最近一年使用:0次
2022-11-13更新
|
158次组卷
|
2卷引用:山东省临沂市平邑县第一中学西校区2023-2024学年高二上学期第一次月考化学试题
名校
解题方法
4 . 下列实验操作能达到实验目的的是
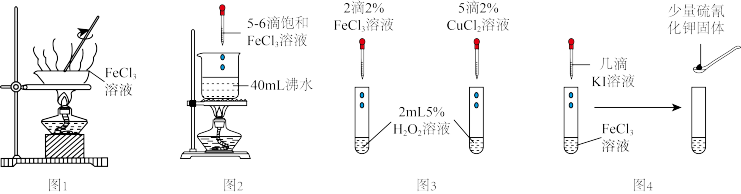

| A.图1:加热蒸干FeCl3溶液制备FeCl3固体 |
| B.图2:制备Fe(OH)3胶体 |
| C.图3:比较Fe3+、Cu2+对H2O2分解的催化效果 |
| D.图4:验证FeCl3与KI的反应是可逆反应 |
您最近一年使用:0次
2022-12-07更新
|
240次组卷
|
3卷引用:河南省2022-2023学年高三上学期12月联考化学试题
名校
5 . 下列实验操作规范且能达到实验目的的是
| 目的 | 操作 | |
| A | 测定醋酸钠溶液的pH | 用玻璃棒蘸 取溶液,点在湿润的pH试纸上 |
| B | 排除碱式滴定管尖嘴部分的气泡 | 将胶管弯曲使玻璃尖嘴斜向上,用两指捏住胶管,轻轻挤压玻璃珠,使溶液从尖嘴流出 |
| C | 由TiCl4制备TiO2∙xH2O | 在干燥的HCl气流中加热 |
| D | 研究催化剂对H2O2分解速率的影响 | 分别向两支试管中加入相同体积不同浓度的H2O2溶液,再向其中一支中加入少量MnO2 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-01-20更新
|
559次组卷
|
7卷引用:四川省仁寿第一中学校南校区2022—2023学年高二下学期3月月考化学试题
名校
解题方法
6 .  是一种绿色氧化还原试剂,在化学研究中应用广泛。
是一种绿色氧化还原试剂,在化学研究中应用广泛。
(一)A实验小组拟在同浓度 的催化下,探究
的催化下,探究 浓度对
浓度对 分解反应速率的影响。
分解反应速率的影响。
(1)写出本实验 分解反应方程式并标明电子转移的方向和数目:
分解反应方程式并标明电子转移的方向和数目:___________ 。
(2)设计实验方案:在不同 浓度下,测定
浓度下,测定___________ (要求所测得的数据能直接体现反应速率大小)。
(二)B实验小组在验证 氧化
氧化 时发现异常现象,并进行了深入探究。
时发现异常现象,并进行了深入探究。
实验Ⅰ:
(3)实验Ⅰ中溶液变红的原因是___________ 。(请用离子方程式表示其原理)
(4)探究实验Ⅰ中红色褪去的原因:取反应后溶液,___________ (填实验操作和现象),证明溶液中有 ,而几乎无
,而几乎无 。
。
(5)查阅资料发现,酸性溶液中 能氧化
能氧化 ,但反应很慢且无明显现象,
,但反应很慢且无明显现象, 对该反应没影响。实验Ⅰ中褪色相对较快,由此推测
对该反应没影响。实验Ⅰ中褪色相对较快,由此推测 在酸性溶液中能加快
在酸性溶液中能加快 与
与 的反应。通过实验Ⅱ和Ⅲ得到了证实。参照实验Ⅱ的图例,补全实验Ⅲ加入的试剂和现象。
的反应。通过实验Ⅱ和Ⅲ得到了证实。参照实验Ⅱ的图例,补全实验Ⅲ加入的试剂和现象。
实验Ⅱ:

实验Ⅲ:
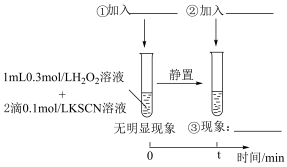
①___________ ;②___________ ;③___________ 。
(三)C实验小组猜测, 会否也能加快
会否也能加快 与
与 的反应。通过实验Ⅱ和Ⅳ得到了证实。
的反应。通过实验Ⅱ和Ⅳ得到了证实。
(6)实验Ⅳ:
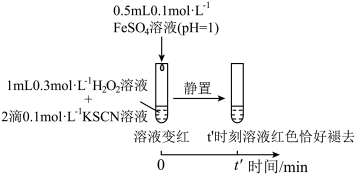
实验得知,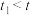 ,对比实验Ⅱ和Ⅳ得到结论:在本实验条件下,
,对比实验Ⅱ和Ⅳ得到结论:在本实验条件下,___________ 。
 是一种绿色氧化还原试剂,在化学研究中应用广泛。
是一种绿色氧化还原试剂,在化学研究中应用广泛。(一)A实验小组拟在同浓度
 的催化下,探究
的催化下,探究 浓度对
浓度对 分解反应速率的影响。
分解反应速率的影响。(1)写出本实验
 分解反应方程式并标明电子转移的方向和数目:
分解反应方程式并标明电子转移的方向和数目:(2)设计实验方案:在不同
 浓度下,测定
浓度下,测定(二)B实验小组在验证
 氧化
氧化 时发现异常现象,并进行了深入探究。
时发现异常现象,并进行了深入探究。实验Ⅰ:
| 装置与操作 | 现象 |
 | 溶液立即变红,继续滴加 溶液,红色变浅并逐渐褪去 溶液,红色变浅并逐渐褪去 |
(4)探究实验Ⅰ中红色褪去的原因:取反应后溶液,
 ,而几乎无
,而几乎无 。
。(5)查阅资料发现,酸性溶液中
 能氧化
能氧化 ,但反应很慢且无明显现象,
,但反应很慢且无明显现象, 对该反应没影响。实验Ⅰ中褪色相对较快,由此推测
对该反应没影响。实验Ⅰ中褪色相对较快,由此推测 在酸性溶液中能加快
在酸性溶液中能加快 与
与 的反应。通过实验Ⅱ和Ⅲ得到了证实。参照实验Ⅱ的图例,补全实验Ⅲ加入的试剂和现象。
的反应。通过实验Ⅱ和Ⅲ得到了证实。参照实验Ⅱ的图例,补全实验Ⅲ加入的试剂和现象。实验Ⅱ:

实验Ⅲ:

①
(三)C实验小组猜测,
 会否也能加快
会否也能加快 与
与 的反应。通过实验Ⅱ和Ⅳ得到了证实。
的反应。通过实验Ⅱ和Ⅳ得到了证实。(6)实验Ⅳ:

实验得知,
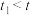 ,对比实验Ⅱ和Ⅳ得到结论:在本实验条件下,
,对比实验Ⅱ和Ⅳ得到结论:在本实验条件下,
您最近一年使用:0次
2023-10-19更新
|
162次组卷
|
2卷引用:广东省广州市执信中学2023-2024学年高二上学期10月选考化学试题
名校
解题方法
7 . 某校化学小组探究 与
与 溶液的反应,进行了如下实验(以下实验过程中溶液体积变化忽略不计):
溶液的反应,进行了如下实验(以下实验过程中溶液体积变化忽略不计):
(1)对比实验i、ii、iii,说明反应速率与___________ 有关。
(2)为了探究淡黄色固体的成分,甲同学进行实验:取实验iv试管壁上的淡黄色固体,发现其微溶于乙醇,易溶于 ,淡黄色固体是
,淡黄色固体是___________ 。
(3)根据上述实验现象,甲同学猜测一定有单质碘生成,猜测的理论依据是___________ ,但实验中溶液始终没有变蓝。
(4)利用如图装置继续实验,证实了单质碘可以生成。实验现象是___________ 。
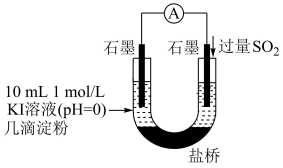
(5)对于实验i、ii、iii未能检测到单质碘,甲同学继续实验
根据(2)(4)(5)的实验现象,结合化学反应原理解释实验iv中始终未检测到单质碘的原因是___________ 。
(6)根据上述一系列实验,乙同学大胆猜测,整个反应中 起到了催化剂作用,为了证明乙同学的猜想正确,还需要的实验证据是
起到了催化剂作用,为了证明乙同学的猜想正确,还需要的实验证据是___________ 。
实验结果证实了猜想,则总反应的化学方程式是___________ 。
 与
与 溶液的反应,进行了如下实验(以下实验过程中溶液体积变化忽略不计):
溶液的反应,进行了如下实验(以下实验过程中溶液体积变化忽略不计):| 实验 | 实验操作 | 实验现象 |
| i | 取 淀粉 淀粉 溶液 溶液 ,通入 ,通入 至量 至量 | 溶液慢慢变为浅黄色 |
| ii | 取 淀粉 淀粉 溶液 溶液 ,通入 ,通入 至过量 至过量 | 溶液迅速变为黄色,略有浑浊 |
| iii | 取 淀粉 淀粉 溶液 溶液 (用盐酸酸化至 (用盐酸酸化至 ),通入 ),通入 至过量 至过量 | 溶液迅速变为黄色,有浑浊 |
| iv | 将实验iii中的黄色浊液进行离心分离 | 试管壁上附着淡黄色固体,溶液为黄色 |
(1)对比实验i、ii、iii,说明反应速率与
(2)为了探究淡黄色固体的成分,甲同学进行实验:取实验iv试管壁上的淡黄色固体,发现其微溶于乙醇,易溶于
 ,淡黄色固体是
,淡黄色固体是(3)根据上述实验现象,甲同学猜测一定有单质碘生成,猜测的理论依据是
(4)利用如图装置继续实验,证实了单质碘可以生成。实验现象是

(5)对于实验i、ii、iii未能检测到单质碘,甲同学继续实验
| 实验 | 实验操作 | 实验现象 |
| v | 将 通入蓝色的碘淀粉混合溶液中 通入蓝色的碘淀粉混合溶液中 | 溶液蓝色迅速褪去 |
| vi | 取实验iv离心后的黄色溶液少量,加入盐酸酸化的 溶液 溶液 | 生成白色沉淀 |
(6)根据上述一系列实验,乙同学大胆猜测,整个反应中
 起到了催化剂作用,为了证明乙同学的猜想正确,还需要的实验证据是
起到了催化剂作用,为了证明乙同学的猜想正确,还需要的实验证据是实验结果证实了猜想,则总反应的化学方程式是
您最近一年使用:0次
解题方法
8 . 铜和稀硝酸在无氧环境下会生成弱酸 。某实验小组为探究铜和稀硝酸的反应,设计实验装置如图。
。某实验小组为探究铜和稀硝酸的反应,设计实验装置如图。

实验过程现象记录如下表。
(1)仪器a的名称为_______ 。
(2)滴入硝酸前,为营造无氧环境,应进行的操作是_______ 。
(3)反应过程中产生的 会进一步与Cu反应生成NO,其离子方程式为
会进一步与Cu反应生成NO,其离子方程式为_______ 。
(4)溶液呈绿色是 和体系中某种微粒相互作用的结果,为探究该微粒进行下列实验:
和体系中某种微粒相互作用的结果,为探究该微粒进行下列实验:
根据以上实验现象可知, 和
和_______ (填化学式)相互作用达到平衡呈绿色。
(5)取适量150 min时反应液于试管中,加入_______ ,溶液由蓝色变为绿色,,说明150 min时反应液中含有 。
。
(6)结合平衡移动原理解释150~300 min反应液颜色变化的原因_______ 。
(7)基于上述装置,选择合适试剂,设计实验证明 对Cu与
对Cu与 硝酸的反应具有催化作用
硝酸的反应具有催化作用_______ (简述实验方案及观测指标)。
 。某实验小组为探究铜和稀硝酸的反应,设计实验装置如图。
。某实验小组为探究铜和稀硝酸的反应,设计实验装置如图。
实验过程现象记录如下表。
| 时间/min | 0~75 | 75~150 | 150~225 | 225~300 | 300~375 |
| 溶液颜色 | 接近无色 | 无色→浅蓝色 | 浅蓝色→绿色 | 绿色→深蓝色 | 浅蓝色 |
| 生成NO体积/mL | 0 | 1.0 | 42.0 | 137.5 | 0.5 |
| 反应体系温度/℃ | 26.6 | 26.8 | 26.8~27.2 | 27.2~28.8 | 28.8~28.6 |
(2)滴入硝酸前,为营造无氧环境,应进行的操作是
(3)反应过程中产生的
 会进一步与Cu反应生成NO,其离子方程式为
会进一步与Cu反应生成NO,其离子方程式为(4)溶液呈绿色是
 和体系中某种微粒相互作用的结果,为探究该微粒进行下列实验:
和体系中某种微粒相互作用的结果,为探究该微粒进行下列实验:| 序号 | 实验操作 | 现象 |
| a | 往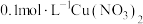 溶液中通入NO 溶液中通入NO | 溶液始终为蓝色 |
| b | 往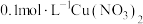 溶液中加入 溶液中加入 | 溶液变为绿色 |
| c | 往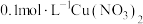 溶液中加入 溶液中加入 后逐滴加入 后逐滴加入 硝酸 硝酸 | 溶液先变为绿色后逐渐变为蓝色 |
 和
和(5)取适量150 min时反应液于试管中,加入
 。
。(6)结合平衡移动原理解释150~300 min反应液颜色变化的原因
(7)基于上述装置,选择合适试剂,设计实验证明
 对Cu与
对Cu与 硝酸的反应具有催化作用
硝酸的反应具有催化作用
您最近一年使用:0次
名校
解题方法
9 . 二氧化氯常用作氧化剂、脱臭剂、保鲜剂、漂白剂等。因其具有对人体及动物无害以及对环境不造成二次污染等特点备受人们青睐。某实验室设计如图装置制取并收集 且探究其性质。
且探究其性质。
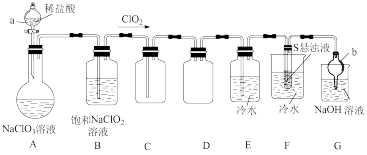
已知:
① 是一种易溶于水的黄绿色气体,与冷水几乎不反应,与热水能反应,其熔点
是一种易溶于水的黄绿色气体,与冷水几乎不反应,与热水能反应,其熔点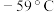 ,沸点
,沸点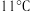 ,受热易分解;
,受热易分解;
②稀盐酸与 反应或
反应或 与
与 溶液反应均可制取
溶液反应均可制取 。
。
回答下列问题:
(1)仪器b的名称是___________ 。
(2)装置A中发生反应: +
+___________ 
 ,滴加稀盐酸时,应缓慢滴加,其主要原因是
,滴加稀盐酸时,应缓慢滴加,其主要原因是___________ 。
(3)根据(2)试分析装置B的作用:___________ (用化学方程式说明)。
(4)装置F中可得到两种强酸的混合溶液,该装置中的现象为___________ ,反应的化学方程式为___________ 。
(5)已知在酸性条件下 可发生反应生成
可发生反应生成 并释放出
并释放出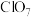 ,向
,向 溶液中滴加盐酸,反应剧烈,若将盐酸换成等
溶液中滴加盐酸,反应剧烈,若将盐酸换成等 的硫酸,开始反应缓慢,稍后一段时间产生气体速率迅速加快,产生气体速率迅速加快的原因是
的硫酸,开始反应缓慢,稍后一段时间产生气体速率迅速加快,产生气体速率迅速加快的原因是___________ 。
 且探究其性质。
且探究其性质。
已知:
①
 是一种易溶于水的黄绿色气体,与冷水几乎不反应,与热水能反应,其熔点
是一种易溶于水的黄绿色气体,与冷水几乎不反应,与热水能反应,其熔点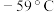 ,沸点
,沸点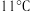 ,受热易分解;
,受热易分解;②稀盐酸与
 反应或
反应或 与
与 溶液反应均可制取
溶液反应均可制取 。
。回答下列问题:
(1)仪器b的名称是
(2)装置A中发生反应:
 +
+
 ,滴加稀盐酸时,应缓慢滴加,其主要原因是
,滴加稀盐酸时,应缓慢滴加,其主要原因是(3)根据(2)试分析装置B的作用:
(4)装置F中可得到两种强酸的混合溶液,该装置中的现象为
(5)已知在酸性条件下
 可发生反应生成
可发生反应生成 并释放出
并释放出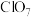 ,向
,向 溶液中滴加盐酸,反应剧烈,若将盐酸换成等
溶液中滴加盐酸,反应剧烈,若将盐酸换成等 的硫酸,开始反应缓慢,稍后一段时间产生气体速率迅速加快,产生气体速率迅速加快的原因是
的硫酸,开始反应缓慢,稍后一段时间产生气体速率迅速加快,产生气体速率迅速加快的原因是
您最近一年使用:0次
2022-09-12更新
|
171次组卷
|
2卷引用:河南省洛阳市第一高级中学2022~2023学年高三上学期9月月考化学试题
10 . 尿素[CO(NH2)2]的合成与利用,体现了化学科学与技术的不断进步。
(1) 与
与 在一定条件下制得尿素,实现了由无机物到有机物的合成,该反应的化学方程式为
在一定条件下制得尿素,实现了由无机物到有机物的合成,该反应的化学方程式为___________ 。
(2)电催化法合成尿素
2021年,科学家设计出一种在 催化剂表面合成尿素的方法,其可能的反应机理如图-1所示。反应部分历程及能量关系如图-2所示。
催化剂表面合成尿素的方法,其可能的反应机理如图-1所示。反应部分历程及能量关系如图-2所示。


①甲醛和羟胺( )缩合生成甲胺(
)缩合生成甲胺( )的实现,为科学家利用碳源和氮源小分子合成尿素提供了基础。这是由于该缩合反应形成了
)的实现,为科学家利用碳源和氮源小分子合成尿素提供了基础。这是由于该缩合反应形成了___________ 化学键。
②已知在制备和反应过程中,催化剂表面的电子能自发从 端转移到Bi端,
端转移到Bi端, 能成功吸附在Bi端的原因可能是
能成功吸附在Bi端的原因可能是___________ 。
③实际生产时可忽略步骤Ⅲ可能出现的副产物 和
和 ,原因是
,原因是___________ 。
(3)尿素能应用于脱除烟气中的污染物。控制其他条件相同,将混有 、
、 、
、 、
、 和
和 的模拟烟气匀速通过装有尿素溶液的装置,在装置出口处检测
的模拟烟气匀速通过装有尿素溶液的装置,在装置出口处检测 、
、 的脱除率
的脱除率 [
[ ]。
]。
①实验测得,烟气中少量 有利于
有利于 的脱除,这是利用了
的脱除,这是利用了 的
的___________ 性。
②当无 存在,且烟气中
存在,且烟气中 与
与 的物质的量浓度相等时,
的物质的量浓度相等时, 达到最大值。该条件下尿素脱除
达到最大值。该条件下尿素脱除 的化学反应方程式为
的化学反应方程式为___________ 。
③当无 存在,且烟气中
存在,且烟气中 超过一定数值时,测得
超过一定数值时,测得 变为负值,其原因是
变为负值,其原因是___________ 。
(1)
 与
与 在一定条件下制得尿素,实现了由无机物到有机物的合成,该反应的化学方程式为
在一定条件下制得尿素,实现了由无机物到有机物的合成,该反应的化学方程式为(2)电催化法合成尿素
2021年,科学家设计出一种在
 催化剂表面合成尿素的方法,其可能的反应机理如图-1所示。反应部分历程及能量关系如图-2所示。
催化剂表面合成尿素的方法,其可能的反应机理如图-1所示。反应部分历程及能量关系如图-2所示。

①甲醛和羟胺(
 )缩合生成甲胺(
)缩合生成甲胺( )的实现,为科学家利用碳源和氮源小分子合成尿素提供了基础。这是由于该缩合反应形成了
)的实现,为科学家利用碳源和氮源小分子合成尿素提供了基础。这是由于该缩合反应形成了②已知在制备和反应过程中,催化剂表面的电子能自发从
 端转移到Bi端,
端转移到Bi端, 能成功吸附在Bi端的原因可能是
能成功吸附在Bi端的原因可能是③实际生产时可忽略步骤Ⅲ可能出现的副产物
 和
和 ,原因是
,原因是(3)尿素能应用于脱除烟气中的污染物。控制其他条件相同,将混有
 、
、 、
、 、
、 和
和 的模拟烟气匀速通过装有尿素溶液的装置,在装置出口处检测
的模拟烟气匀速通过装有尿素溶液的装置,在装置出口处检测 、
、 的脱除率
的脱除率 [
[ ]。
]。①实验测得,烟气中少量
 有利于
有利于 的脱除,这是利用了
的脱除,这是利用了 的
的②当无
 存在,且烟气中
存在,且烟气中 与
与 的物质的量浓度相等时,
的物质的量浓度相等时, 达到最大值。该条件下尿素脱除
达到最大值。该条件下尿素脱除 的化学反应方程式为
的化学反应方程式为③当无
 存在,且烟气中
存在,且烟气中 超过一定数值时,测得
超过一定数值时,测得 变为负值,其原因是
变为负值,其原因是
您最近一年使用:0次
2023-10-17更新
|
259次组卷
|
2卷引用:江苏省决胜新高考部分学校2023-2024学年高三上学期10月大联考化学试题