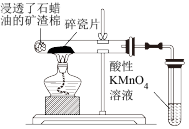
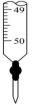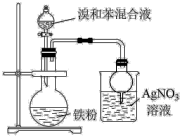下列操作规范且能达到实验目的的是


| A.若装置I中反应速率①>②,可以验证Fe3+的催化效果比Cu2+好 |
B.由装置II中颜色的变化可以判断反应N2O4(g) 2NO2(g) △H>0 2NO2(g) △H>0 |
| C.可通过装置III测定反应速率的大小 |
| D.可用装置IV来测定醋酸的浓度 |
更新时间:2022-11-13 10:42:16
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】已知反应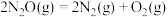 ,速率方程为
,速率方程为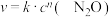 。
。 在金(Au)表面分解的实验数据如表所示。
在金(Au)表面分解的实验数据如表所示。
已知:①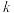 为速率常数,只与温度、催化剂有关,与浓度无关;
为速率常数,只与温度、催化剂有关,与浓度无关;
②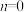 时,该反应为0级反应,
时,该反应为0级反应,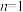 时,该反应为1级反应,以此类推,
时,该反应为1级反应,以此类推,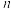 可以为整数,也可以为分数;③浓度消耗一半所用的时间叫半衰期(
可以为整数,也可以为分数;③浓度消耗一半所用的时间叫半衰期( )。
)。
下列说法正确的是
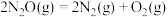 ,速率方程为
,速率方程为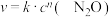 。
。 在金(Au)表面分解的实验数据如表所示。
在金(Au)表面分解的实验数据如表所示。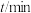 | 0 | 20 | 40 | 60 | 80 | 100 |
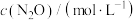 | 0.100 | 0.080 | 0.060 |  | 0.020 | 0 |
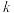 为速率常数,只与温度、催化剂有关,与浓度无关;
为速率常数,只与温度、催化剂有关,与浓度无关;②
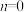 时,该反应为0级反应,
时,该反应为0级反应,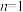 时,该反应为1级反应,以此类推,
时,该反应为1级反应,以此类推,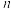 可以为整数,也可以为分数;③浓度消耗一半所用的时间叫半衰期(
可以为整数,也可以为分数;③浓度消耗一半所用的时间叫半衰期( )。
)。下列说法正确的是
A.表格中 |
| B.该反应为2级反应 |
C.保持其他条件不变,若起始浓度为 ,则半衰期为100min ,则半衰期为100min |
D.该反应的速率常数 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】用下列实验装置进行的实验,不能达到相应的实验目的的是


A.利用图1装置进行 的尾气处理 的尾气处理 |
B.利用图2装置和秒表测定反应产生的 的体积及反应时间,计算反应速率 的体积及反应时间,计算反应速率 |
| C.利用图3装置通过观察红棕色气体证明硝酸具有不稳定性 |
| D.利用图4装置加热氯化铵和氢氧化钙的混合物制取氨气 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】绿氢由于生产过程中100%绿色的特点备受青睐,发展前景最为广阔,光催化制氢机理研究取得新进展。如图是通过光催化循环在较低温度下由水分解制备氢气的反应原理。下列有关说法错误的是
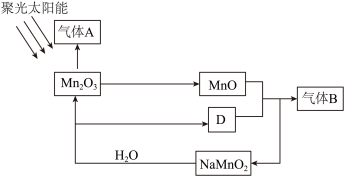
| A.该制氢过程中,消耗了水和太阳能,含锰化合物均为中间产物 |
| B.该制氢过程解决了气体A、B难分离的问题 |
| C.制氢过程中涉及Mn元素转化的反应不都是氧化还原反应 |
D.生成气体B的反应方程式为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】某种含铜的催化剂 可用于汽车尾气脱氮,催化机理如图所示。下列说法错误的是
可用于汽车尾气脱氮,催化机理如图所示。下列说法错误的是

 可用于汽车尾气脱氮,催化机理如图所示。下列说法错误的是
可用于汽车尾气脱氮,催化机理如图所示。下列说法错误的是
| A.该催化循环中Cu的化合价没有发生变化 |
| B.反应①→②不是氧化还原反应 |
C.总反应的化学方程式为 |
D.实验室模拟此过程时,可用浓氨水与碱石灰反应提供 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】三氯氢硅( )在催化剂作用下可发生反应:
)在催化剂作用下可发生反应: ,
, 和
和 时
时 的转化率随时间变化的结果如图所示。下列叙述正确的是
的转化率随时间变化的结果如图所示。下列叙述正确的是

 )在催化剂作用下可发生反应:
)在催化剂作用下可发生反应: ,
, 和
和 时
时 的转化率随时间变化的结果如图所示。下列叙述正确的是
的转化率随时间变化的结果如图所示。下列叙述正确的是
| A.该反应为放热反应 | B.a点时, |
C.反应速率: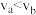 | D.增大压强,可提高 的平衡转化率 的平衡转化率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】已知反应mX(g)+nY(g) qZ(g)的△H<0,m+n﹥q,在恒容密闭容器中反应达到平衡时,下列说法正确的是( )
qZ(g)的△H<0,m+n﹥q,在恒容密闭容器中反应达到平衡时,下列说法正确的是( )
 qZ(g)的△H<0,m+n﹥q,在恒容密闭容器中反应达到平衡时,下列说法正确的是( )
qZ(g)的△H<0,m+n﹥q,在恒容密闭容器中反应达到平衡时,下列说法正确的是( )| A.通入稀有气体,体系压强增大,平衡向正反应方向移动 |
| B.降低温度,混合气体的平均相对分子质量减小 |
| C.增加X的物质的量,X的转化率增大 |
| D.增加X的物质的量,Y的转化率增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列操作规范且能达到实验目的的是
| A | B | C | D |
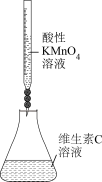 |  | 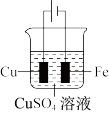 | 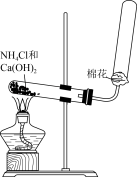 |
| 测定维生素C浓度 | 除去H2S气体中的HCl杂质 | 在铁上镀铜 | 实验室制备并收集氨气 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】用如图装置进行实验,装置正确且能达到相应实验目的的是
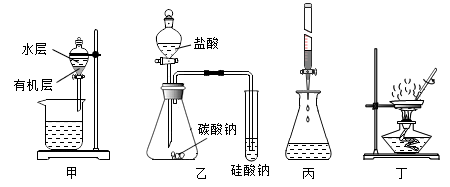

| A.用装置甲加入CCl4 分离碘水中的碘 | B.用装置乙比较碳酸与硅酸酸性强弱 |
| C.用装置丙酸性KMnO4滴定草酸溶液 | D.用装置丁蒸干FeCl3溶液制无水FeCl3 |
您最近一年使用:0次

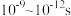 ,主要可用于化学平衡问题的研究
,主要可用于化学平衡问题的研究 和无水硫酸铜均可以检验某气体是否潮湿
和无水硫酸铜均可以检验某气体是否潮湿 装置如下:
装置如下: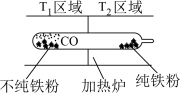
 .对于该过程理解不正确的是
.对于该过程理解不正确的是 是以
是以 为中心原子,
为中心原子, 为配体的配合物
为配体的配合物 区域和
区域和 区域发生反应的平衡常数互为倒数关系
区域发生反应的平衡常数互为倒数关系 增大
增大