1 . H2O2是一种重要的化学品,其合成方法不断发展。
(1)早期制备方法:Ba(NO3)2 BaO
BaO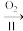 BaO2
BaO2
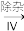 滤液
滤液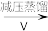 H2O2
H2O2
①I为分解反应,产物除BaO、O2外,还有一种红棕色气体。该反应的化学方程式是____ 。
②II为可逆反应,促进该反应正向进行的措施是____ 。
③III中生成H2O2,反应的化学方程式是____ 。
④减压能够降低蒸馏温度,从H2O2的化学性质角度说明V中采用减压蒸馏的原因:____ 。
(2)电化学制备方法:已知反应2H2O2=2H2O+O2↑能自发进行,反向不能自发进行,通过电解可以实现由H2O和O2为原料制备H2O2,如图为制备装置示意图。

①a极的电极反应式是____ 。
②下列说法正确的是____ 。
A.该装置可以实现电能转化为化学能
B.电极b连接电源负极
C.该方法相较于早期制备方法具有原料廉价,对环境友好等优点
(1)早期制备方法:Ba(NO3)2
 BaO
BaO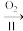 BaO2
BaO2
 滤液
滤液 H2O2
H2O2①I为分解反应,产物除BaO、O2外,还有一种红棕色气体。该反应的化学方程式是
②II为可逆反应,促进该反应正向进行的措施是
③III中生成H2O2,反应的化学方程式是
④减压能够降低蒸馏温度,从H2O2的化学性质角度说明V中采用减压蒸馏的原因:
(2)电化学制备方法:已知反应2H2O2=2H2O+O2↑能自发进行,反向不能自发进行,通过电解可以实现由H2O和O2为原料制备H2O2,如图为制备装置示意图。

①a极的电极反应式是
②下列说法正确的是
A.该装置可以实现电能转化为化学能
B.电极b连接电源负极
C.该方法相较于早期制备方法具有原料廉价,对环境友好等优点
您最近一年使用:0次
2020-08-19更新
|
5447次组卷
|
9卷引用:2020年北京市高考化学试卷
真题
解题方法
2 . 煤炭燃烧过程中会释放出大量的SO2,严重破坏生态环境。采用一定的脱硫技术可以把硫元素以CaSO4的形式固定,从而降低SO2的排放。但是煤炭燃烧过程中产生的CO又会与CaSO4发生化学反应,降低脱硫效率。相关反应的热化学方程式如下:
CaSO4(s)+CO(g)⇌ CaO(s) + SO2(g) + CO2(g) ΔH1=218.4kJ·mol-1(反应Ⅰ)
CaSO4(s)+4CO(g)⇌ CaS(s) + 4CO2(g) ΔH2= -175.6kJ·mol-1(反应Ⅱ)
请回答下列问题:
(1)反应Ⅰ能自发进行的条件是_______ 。
(2)对于气体参与的反应,表示平衡常数Kp时用气体组分(B)的平衡压强p(B)代替该气体物质的量浓度c(B),则反应Ⅱ的Kp=_______ (用表达式表示)。
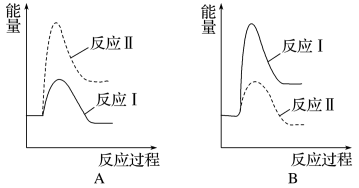
(3)假设某温度下,反应Ⅰ的速率(v1)大于反应Ⅱ的速率(v2),则下列反应过程能量变化示意图正确的是_______ 。

(4)通过监测反应体系中气体浓度的变化判断反应Ⅰ和Ⅱ是否同时发生,理由是_______ 。
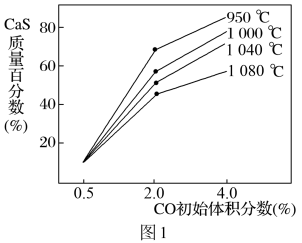
(5)图1为实验测得不同温度下反应体系中CO初始体积百分数与平衡时固体产物中CaS质量百分数的关系曲线。则降低该反应体系中SO2生成量的措施有_______ 。
A.向该反应体系中投入石灰石
B.在合适的温度区间内控制较低的反应温度
C.提高CO的初始体积百分数
D.提高反应体系的温度
(6)恒温恒容条件下,假设反应Ⅰ和Ⅱ同时发生,且v1>v2,请在图2中画出反应体系中c(SO2)随时间t变化的总趋势图______ 。
CaSO4(s)+CO(g)⇌ CaO(s) + SO2(g) + CO2(g) ΔH1=218.4kJ·mol-1(反应Ⅰ)
CaSO4(s)+4CO(g)⇌ CaS(s) + 4CO2(g) ΔH2= -175.6kJ·mol-1(反应Ⅱ)
请回答下列问题:
(1)反应Ⅰ能自发进行的条件是
(2)对于气体参与的反应,表示平衡常数Kp时用气体组分(B)的平衡压强p(B)代替该气体物质的量浓度c(B),则反应Ⅱ的Kp=
(3)假设某温度下,反应Ⅰ的速率(v1)大于反应Ⅱ的速率(v2),则下列反应过程能量变化示意图正确的是


(4)通过监测反应体系中气体浓度的变化判断反应Ⅰ和Ⅱ是否同时发生,理由是
(5)图1为实验测得不同温度下反应体系中CO初始体积百分数与平衡时固体产物中CaS质量百分数的关系曲线。则降低该反应体系中SO2生成量的措施有

A.向该反应体系中投入石灰石
B.在合适的温度区间内控制较低的反应温度
C.提高CO的初始体积百分数
D.提高反应体系的温度
(6)恒温恒容条件下,假设反应Ⅰ和Ⅱ同时发生,且v1>v2,请在图2中画出反应体系中c(SO2)随时间t变化的总趋势图

您最近一年使用:0次
2016-12-09更新
|
3044次组卷
|
5卷引用:2014年全国普通高等学校招生统一考试理科综合能力测试化学(浙江卷)
2014年全国普通高等学校招生统一考试理科综合能力测试化学(浙江卷)2017届宁夏银川二中高三上学期统练二化学试卷(已下线)2019高考备考二轮复习精品资料-专题8 化学反应中与能量变化(教学案)(已下线)2019高考备考二轮复习精品资料-专题9 化学反应速率与化学平衡(教学案)(已下线)专题20.化学反应原理综合应用-十年(2012-2021)高考化学真题分项汇编(浙江专用)
真题
3 . 某温度时,在2L密闭容器中气态物质X和Y反应生成气态物质Z,它们的物质的量随时间的变化如表所示。
(1)根据表中数据,在图1中画出X、Y、Z的物质的量(n)随时间(t)变化的曲线:
________________

(2) 体系中发生反应的化学方程式是___________________________ ;
(3) 列式计算该反应在0-3min时间内产物Z的平均反应速率:_______________ ;
(4) 该反应达到平衡时反应物X的转化率 等于
等于___________________________ ;
(5) 如果该反应是放热反应。改变实验条件(温度、压强、催化剂)得到Z随时间变化的曲线①、②、③(如图2所示)则曲线①、②、③所对应的实验条件改变分别是:
①_________________ ②________________ ③__________________
(1)根据表中数据,在图1中画出X、Y、Z的物质的量(n)随时间(t)变化的曲线:
| t/min | X/mol | Y/mol | Z/mol |
| 0 | 1.00 | 1.00 | 0.00 |
| 1 | 0.90 | 0.80 | 0.20 |
| 3 | 0.75 | 0.50 | 0.50 |
| 5 | 0.65 | 0.30 | 0.70 |
| 9 | 0.55 | 0.10 | 0.90 |
| 10 | 0.55 | 0.10 | 0.90 |
| 14 | 0.55 | 0.10 | 0.90 |

(2) 体系中发生反应的化学方程式是
(3) 列式计算该反应在0-3min时间内产物Z的平均反应速率:
(4) 该反应达到平衡时反应物X的转化率
 等于
等于(5) 如果该反应是放热反应。改变实验条件(温度、压强、催化剂)得到Z随时间变化的曲线①、②、③(如图2所示)则曲线①、②、③所对应的实验条件改变分别是:
①
您最近一年使用:0次
2016-12-09更新
|
48次组卷
|
7卷引用:2009年普通高等学校招生统一考试理综试题化学部分(全国卷Ⅱ)



