1 . 下列有关合成氨工业的叙述,可用勒夏特列原理来解释的是
A.使用铁触媒,使 和 和 混合气体有利于合成氨 混合气体有利于合成氨 |
| B.高压比常压条件更有利于合成氨的反应 |
| C.700K左右比室温更有利于合成氨的反应 |
| D.合成氨时采用循环操作,可提高原料的利用率 |
您最近半年使用:0次
2020-09-13更新
|
396次组卷
|
10卷引用:上海市浦东区浦东中学2019届高三上学期期中考试化学试题
上海市浦东区浦东中学2019届高三上学期期中考试化学试题(已下线)2.4.2 工业合成氨的生产流程-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修第一册)(已下线)2012年人教版高中化学选修2 1.2人工固氮技术—合成氨练习卷鲁科版(2019)选择性必修1第2章 化学反应的方向、限度与速率 第4节 化学反应条件的优化——工业合成氨高中必刷题高二选择性必修1第二章 化学反应速率与化学平衡 第四节 化学反应的调控安徽省淮北市树人高级中学2020-2021学年高二上学期第一次联考化学试题(已下线)第六章 化学反应与能量(培优提升卷)-2020-2021学年高一化学章末集训必刷卷(人教版2019必修第二册)(已下线)第29练 化学反应的调控-2023年高考化学一轮复习小题多维练(全国通用)新疆哈密市第八中学2022-2023学年高二上学期期末考试化学试题(已下线)专题06 化学反应的方向及调控【考题猜想】(6大题型)-2023-2024学年高二化学期中考点大串讲(人教版2019选择性必修1)
10-11高三上·上海普陀·期末
解题方法
2 . 各可逆反应达平衡后,改变反应条件,其变化趋势正确的是
A.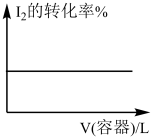 I2(g)+H2(g) I2(g)+H2(g) 2HI(g) (恒温) 2HI(g) (恒温) |
B.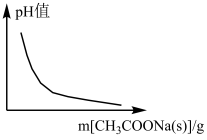 CH3COOH CH3COOH H++CH3COO-(忽略溶液体积变化) H++CH3COO-(忽略溶液体积变化) |
C. FeCl3+3KSCN FeCl3+3KSCN Fe(SCN)3+3KCl(忽略溶液体积变化) Fe(SCN)3+3KCl(忽略溶液体积变化) |
D.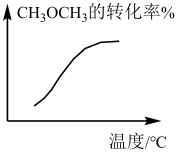 CH3OCH(g)+3H2O(g) CH3OCH(g)+3H2O(g) 6H2(g)+2CO(g)-Q(恒压) 6H2(g)+2CO(g)-Q(恒压) |
您最近半年使用:0次
14-15高三上·上海宝山·阶段练习
名校
解题方法
3 . 各可逆反应达平衡后,改变反应条件,其变化趋势正确的是
A.I2(g)+H2(g)  2HI(g)(恒温) 2HI(g)(恒温) 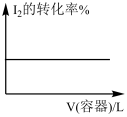 |
B.CH3COOH H++CH3COO- H++CH3COO-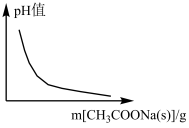 |
C.FeCl3+3KSCN Fe(SCN)3+3KCl Fe(SCN)3+3KCl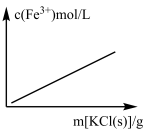 |
D.CH3OCH3(g)+3H2O(g)  6H2(g)+2CO(g)-Q 6H2(g)+2CO(g)-Q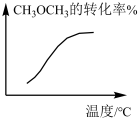 |
您最近半年使用:0次
4 . 对于反应N2 + 3H2 2NH3 ,下列判断正确的是( )
2NH3 ,下列判断正确的是( )
 2NH3 ,下列判断正确的是( )
2NH3 ,下列判断正确的是( )| A.3体积H2和足量N2反应,必定生成2体积NH3 |
| B.工业上采用氮氢循环操作的主要目的是提高H2和N2的利用率 |
| C.500℃左右比室温更有利于向合成氨的方向进行 |
| D.其他条件不变,增大压强,平衡必定向右移动 |
您最近半年使用:0次
名校
5 . 一定温度下,在3个体积均为1.0L的恒容密闭容器中发生反应2SO2(g)+O2(g) 2SO3(g) ΔH<0。达到平衡时,下列说法正确的是
2SO3(g) ΔH<0。达到平衡时,下列说法正确的是
 2SO3(g) ΔH<0。达到平衡时,下列说法正确的是
2SO3(g) ΔH<0。达到平衡时,下列说法正确的是容器 | 温度/℃ | 物质的起始浓度/mol·L-1 | 物质的平衡浓度/mol·L-1 | ||
c(SO2) | c(O2) | c(SO3) | c(SO3) | ||
Ⅰ | 758 | 0.2 | 0.1 | 0 | 0.044 |
Ⅱ | 758 | 0.1 | 0.05 | 0 | |
Ⅲ | 858 | 0.2 | 0.1 | 0 | |
| A.从开始至平衡时,容器Ⅰ中SO3的反应速率为0.044 mol·L-1·s-1 |
| B.平衡时,容器Ⅱ中SO3的浓度小于0.022mol·L-1 |
| C.平衡时,容器Ⅲ中SO3的浓度大于0.044mol·L-1 |
| D.若起始时,向容器Ⅰ中充入0.02mol SO2、0.01mol O2和0.02mol SO3,则反应向逆反应方向进行 |
您最近半年使用:0次
2019-04-18更新
|
136次组卷
|
2卷引用:2019-2020学年上海市黄浦区大同中学高三(上)10月月考化学试卷



