解题方法
1 . 下列实验操作和现象与所得实验结论一致的是
| 选项 | 实验操作和现象 | 结论 |
| A | 向 溶液中滴入几滴浓 溶液中滴入几滴浓 ,溶液橙色加深 ,溶液橙色加深 |  转化为 转化为 |
| B | 向含有少量 的 的 溶液中加入足量MgO粉末,搅拌一段时间后过滤 溶液中加入足量MgO粉末,搅拌一段时间后过滤 | 可除去 溶液中少量 溶液中少量 |
| C | 分别测定浓度均为 的 的 和 和 溶液的pH,后者大于前者 溶液的pH,后者大于前者 | 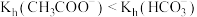 |
| D | 向2mL浓度均为 的NaCl、NaI的混合溶液中滴入2mL 的NaCl、NaI的混合溶液中滴入2mL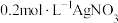 溶液,有黄色沉淀生成 溶液,有黄色沉淀生成 |  |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
2 . t℃时,向容积为2L的刚性容器中充入 和一定量的
和一定量的 发生反应:
发生反应: ,HCHO的平衡分压与起始
,HCHO的平衡分压与起始 的关系如图所示。已知:初始加入
的关系如图所示。已知:初始加入 时,容器内混合气体的总压强为1.2pkPa。
时,容器内混合气体的总压强为1.2pkPa。
已知:分压=总压×物质的量分数, 为以分压表示的平衡常数。
为以分压表示的平衡常数。

下列叙述正确的是
 和一定量的
和一定量的 发生反应:
发生反应: ,HCHO的平衡分压与起始
,HCHO的平衡分压与起始 的关系如图所示。已知:初始加入
的关系如图所示。已知:初始加入 时,容器内混合气体的总压强为1.2pkPa。
时,容器内混合气体的总压强为1.2pkPa。已知:分压=总压×物质的量分数,
 为以分压表示的平衡常数。
为以分压表示的平衡常数。
下列叙述正确的是
A.随 增大,HCHO的平衡体积分数不断增大 增大,HCHO的平衡体积分数不断增大 |
B.e点: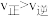 |
C.a点时再投入物质的量均为1mol的 、 、 ,重新平衡时, ,重新平衡时, 的平衡转化率减小 的平衡转化率减小 |
D.c点时反应的压强平衡常数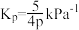 |
您最近一年使用:0次
名校
3 . 下列叙述正确的是
A.已知 的电离方程式为 的电离方程式为 ,则 ,则 是一元弱酸 是一元弱酸 |
B.pH=2的盐酸和硫酸溶液,硫酸溶液中 是盐酸中 是盐酸中 的2倍 的2倍 |
C.将CO中毒的人转至高压氧仓促使反应 逆向移动 逆向移动 |
D.向 的 的 溶液中加氨水至中性,此时溶液含 溶液中加氨水至中性,此时溶液含 数目小于 数目小于 |
您最近一年使用:0次
4 . 对于平衡体系mA(g)+nB(g) pC(g)+qD(g) △H<0。下列结论正确的是
pC(g)+qD(g) △H<0。下列结论正确的是
 pC(g)+qD(g) △H<0。下列结论正确的是
pC(g)+qD(g) △H<0。下列结论正确的是| A.若温度不变,将容器的体积缩小到原来的一半,达到新平衡时A的浓度为原来的2.2倍,则m+n>p+q |
| B.若m+n=p+q,则向含有amol气体的平衡体系中再加入amol的B,达到新平衡时气体的总物质的量等于2amol |
| C.若平衡时,A.B的转化率相等,说明反应开始时,A、B的物质的量之比为m:n |
| D.温度升高时,K值增大 |
您最近一年使用:0次
名校
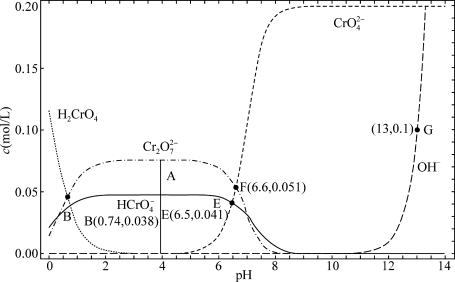
5 . 某温度下,改变0.1mol/L  溶液的pH时,各种含铬元素微粒及
溶液的pH时,各种含铬元素微粒及 浓度变化如图所示(已知
浓度变化如图所示(已知 是二元酸),下列有关说法中,正确的是
是二元酸),下列有关说法中,正确的是
 溶液的pH时,各种含铬元素微粒及
溶液的pH时,各种含铬元素微粒及 浓度变化如图所示(已知
浓度变化如图所示(已知 是二元酸),下列有关说法中,正确的是
是二元酸),下列有关说法中,正确的是
A.该温度下的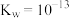 |
B.溶液中存在平衡 ,该温度下此反应的 ,该温度下此反应的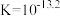 |
C.向0.1mol/L  溶液中加入一定量NaOH固体,溶液橙色变浅 溶液中加入一定量NaOH固体,溶液橙色变浅 |
D.E点溶液中存在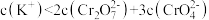 |
您最近一年使用:0次
名校
6 . 相同温度和压强下,研究Cl2在不同溶液中的溶解度(用溶解Cl2的物质的量浓度表示)随溶液浓度的变化。在NaCl溶液和盐酸中Cl2的溶解度以及各种含氯微粒的浓度变化如下图。

下列说法不正确的是

下列说法不正确的是
A.由图1可知,Cl2溶于NaCl溶液时还发生了反应Cl2+Cl-=Cl |
B.随NaCl溶液浓度增大,Cl2+H2O H++Cl-+HClO平衡逆移,Cl2溶解度减小 H++Cl-+HClO平衡逆移,Cl2溶解度减小 |
| C.随盐酸浓度增加Cl2与H2O的反应被抑制,生成Cl3-为主要反应从而抑制Cl2溶解 |
| D.由上述实验可知,H+浓度增大促进 Cl2溶解,由此推知在稀硫酸中,随硫酸浓度增大Cl2的溶解度会增大 |
您最近一年使用:0次
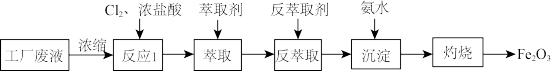
7 . 某电子厂排放的酸性废液中含有Fe3+、Cu2+、Fe2+和Cl-等离子,以这种废液为原料设计制备高纯Fe2O3的工艺流程如图所示(部分操作和条件略)。已知:①HCl(浓)+FeCl3 HFeCl4 (易溶于有机溶剂);②
HFeCl4 (易溶于有机溶剂);②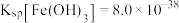 ,
,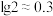 。下列说法不正确的是
。下列说法不正确的是
 HFeCl4 (易溶于有机溶剂);②
HFeCl4 (易溶于有机溶剂);②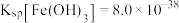 ,
,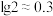 。下列说法不正确的是
。下列说法不正确的是
| A.反应1所发生的反应中存在氧化还原反应 |
| B.在反萃取过程中利用了平衡移动原理,水不可以作为反萃取剂 |
| C.氨水的作用是调节pH使Fe3+沉淀,相关反应离子方程式为:Fe3++3OH-=Fe(OH)3↓ |
| D.为使Fe3+沉淀完全(浓度小于1×10-5 mol/L),需调节溶液pH>3.3 |
您最近一年使用:0次
名校
解题方法
8 . 生活污水中的氮和磷主要以铵盐和磷酸盐的形式存在,可用电解法从溶液中除去。有Cl-存在时。除氮原理如图1所示。主要依靠有效氯(HClO、ClO-)将 或NH3氧化为N2。在不同pH条件下进行电解时,氮的去除率和水中有效氯浓度与溶液pH的关系如图2所示。
或NH3氧化为N2。在不同pH条件下进行电解时,氮的去除率和水中有效氯浓度与溶液pH的关系如图2所示。

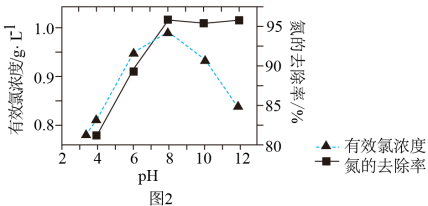
下列说法不正确的是
 或NH3氧化为N2。在不同pH条件下进行电解时,氮的去除率和水中有效氯浓度与溶液pH的关系如图2所示。
或NH3氧化为N2。在不同pH条件下进行电解时,氮的去除率和水中有效氯浓度与溶液pH的关系如图2所示。

下列说法不正确的是
| A.pH=3时,主要发生ClO-氧化NH3的反应 |
| B.pH>8时,有效氯浓度随pH的增大而增大 |
C.pH>8时, 转变为NH3·H2O,且有利于NH3逸出 转变为NH3·H2O,且有利于NH3逸出 |
| D.pH<8时,氮的去除率随pH的减少而下降的原因是c(HClO)减小 |
您最近一年使用:0次
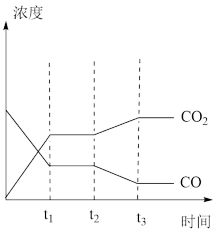
9 . 在一体积固定的密闭容器中发生: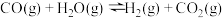 ,如图表示该反应在时刻达到平衡,在
,如图表示该反应在时刻达到平衡,在 时刻分别因改变某个条件而发生变化的情况。图中
时刻分别因改变某个条件而发生变化的情况。图中 时刻发生改变的条件可能是
时刻发生改变的条件可能是
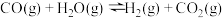 ,如图表示该反应在时刻达到平衡,在
,如图表示该反应在时刻达到平衡,在 时刻分别因改变某个条件而发生变化的情况。图中
时刻分别因改变某个条件而发生变化的情况。图中 时刻发生改变的条件可能是
时刻发生改变的条件可能是
A.加入 | B.加入水蒸气 | C.加入催化剂 | D.分离部分 |
您最近一年使用:0次
2022-01-20更新
|
144次组卷
|
2卷引用:湖南省湖湘名校联盟2021-2022学年高二上学期期末考试化学试题
10 . 痛风是以关节炎反复发作及产生肾结石为特征的一类疾病,形成关节炎的原因归结于在关节滑液中形成了尿酸钠(NaUr)晶体,有关平衡如下:
①HUr(尿酸,aq) Ur-(尿酸根,aq)+H+(aq)
Ur-(尿酸根,aq)+H+(aq)
②NaUr(s) Ur-(aq)+Na+(aq)
Ur-(aq)+Na+(aq)
室温下,将尿酸钠(NaUr)的悬浊液静置,取上层清液滴加盐酸,溶液中尿酸的浓度c(HUr)与pH的关系如图所示。已知Ksp(NaUr)=4.9×10-5,Ka(HUr)=2.0×10-6。下列说法不正确的是

①HUr(尿酸,aq)
 Ur-(尿酸根,aq)+H+(aq)
Ur-(尿酸根,aq)+H+(aq)②NaUr(s)
 Ur-(aq)+Na+(aq)
Ur-(aq)+Na+(aq)室温下,将尿酸钠(NaUr)的悬浊液静置,取上层清液滴加盐酸,溶液中尿酸的浓度c(HUr)与pH的关系如图所示。已知Ksp(NaUr)=4.9×10-5,Ka(HUr)=2.0×10-6。下列说法不正确的是

| A.冬季为关节炎高发期,多在脚趾和手指的关节处,则生成尿酸钠晶体的反应是吸热反应 |
| B.N点时,c(HUr)=c(Cl-) |
C.M→N的变化过程中,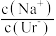 逐渐减小 逐渐减小 |
| D.当某病人尿液中的c(HUr)=c(Ur-)时,该病人的尿液呈酸性 |
您最近一年使用:0次



