2022高一·全国·专题练习
1 . 向新制氯水中加入碳酸钙粉末,能增加氯水中HClO的浓度吗?为什么?______
您最近一年使用:0次
2 . 回答下列问题:
(1)在密闭容器中,加热一氧化碳和水蒸气的气体混合物,在催化剂存在下发生反应: ,500℃时,平衡常数
,500℃时,平衡常数 。若反应开始时,一氧化碳和水蒸气的浓度都是0.2mol/L,则平衡时CO的体积分数为
。若反应开始时,一氧化碳和水蒸气的浓度都是0.2mol/L,则平衡时CO的体积分数为_______ 。
(2)在恒温恒压的密闭容器中,按照n(A):n(B)=1:4投料,发生如下反应①和②
①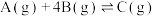 ;②
;②
总压为 ,A的转化率为a,C的分压为P,则反应①的
,A的转化率为a,C的分压为P,则反应①的
_______ (列出算式即可,用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(3)将等物质的量的X、Y气体充入一个密闭容器中,在一定条件下发生反应 并达到平衡状态,若保持容器容积不变再通入一定量的Z,则平衡如何移动
并达到平衡状态,若保持容器容积不变再通入一定量的Z,则平衡如何移动_______ (填“正移”“逆移”或“不移”);达新平衡后,X的体积分数如何变化_______ (填“增大”“减小”或“不变”)。
(1)在密闭容器中,加热一氧化碳和水蒸气的气体混合物,在催化剂存在下发生反应:
 ,500℃时,平衡常数
,500℃时,平衡常数 。若反应开始时,一氧化碳和水蒸气的浓度都是0.2mol/L,则平衡时CO的体积分数为
。若反应开始时,一氧化碳和水蒸气的浓度都是0.2mol/L,则平衡时CO的体积分数为(2)在恒温恒压的密闭容器中,按照n(A):n(B)=1:4投料,发生如下反应①和②
①
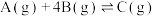 ;②
;②
总压为
 ,A的转化率为a,C的分压为P,则反应①的
,A的转化率为a,C的分压为P,则反应①的
(3)将等物质的量的X、Y气体充入一个密闭容器中,在一定条件下发生反应
 并达到平衡状态,若保持容器容积不变再通入一定量的Z,则平衡如何移动
并达到平衡状态,若保持容器容积不变再通入一定量的Z,则平衡如何移动
您最近一年使用:0次
3 . 回答下列问题:
(1)在密闭容器中,加热一氧化碳和水蒸气的气体混合物,在催化剂存在下发生反应: ,500℃时,平衡常数
,500℃时,平衡常数 。若反应开始时,一氧化碳和水蒸气的浓度都是0.2mol/L,则平衡时CO的体积分数为
。若反应开始时,一氧化碳和水蒸气的浓度都是0.2mol/L,则平衡时CO的体积分数为_______ 。
(2)在恒温恒压的密闭容器中,按照n(A):n(B)=1:4投料,发生如下反应①和②
①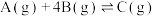 ;②
;②
总压为 ,A的转化率为a,C的分压为P,则反应①的
,A的转化率为a,C的分压为P,则反应①的
_______ (列出算式即可,用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(3)将等物质的量的X、Y气体充入一个密闭容器中,在一定条件下发生反应 并达到平衡状态,若保持容器容积不变再通入一定量的Z,则平衡如何移动
并达到平衡状态,若保持容器容积不变再通入一定量的Z,则平衡如何移动_______ (填“正移”“逆移”或“不移”);达新平衡后,X的体积分数如何变化_______ (填“增大”“减小”或“不变”)。
(1)在密闭容器中,加热一氧化碳和水蒸气的气体混合物,在催化剂存在下发生反应:
 ,500℃时,平衡常数
,500℃时,平衡常数 。若反应开始时,一氧化碳和水蒸气的浓度都是0.2mol/L,则平衡时CO的体积分数为
。若反应开始时,一氧化碳和水蒸气的浓度都是0.2mol/L,则平衡时CO的体积分数为(2)在恒温恒压的密闭容器中,按照n(A):n(B)=1:4投料,发生如下反应①和②
①
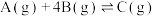 ;②
;②
总压为
 ,A的转化率为a,C的分压为P,则反应①的
,A的转化率为a,C的分压为P,则反应①的
(3)将等物质的量的X、Y气体充入一个密闭容器中,在一定条件下发生反应
 并达到平衡状态,若保持容器容积不变再通入一定量的Z,则平衡如何移动
并达到平衡状态,若保持容器容积不变再通入一定量的Z,则平衡如何移动
您最近一年使用:0次
名校
解题方法
4 . 铁元素及其化合物在生活生产中有广泛的用途。回答下列问题:
(1)Fe3+与SCN-的反应常用来检验Fe3+的存在: Fe3+ + 3SCN- Fe(SCN)3
Fe(SCN)3
若溶液中含有Fe3+,则加入KSCN溶液后的现象为_________ 向加入KSCN后的混合溶液中再加入少量NaOH固体,观察到的现象是_____________ ,产生该现象的原因是________________ 。
(2)向FeSO4溶液中滴入NaOH溶液,会观察到先产生白色沉淀,后迅速变为灰绿色,久置后变为红褐色,用化学方程式说明产生该现象的原因__________________ 。
(3)FeCl3溶液常被用作蚀刻剂腐蚀印刷电路板: 2Fe3++ Cu==2Fe2+ + Cu2+在过量FeCl3溶液腐蚀印刷电路板后的溶液中,加入过量铁粉,依次发生______ 、________ 两个反应(写离子方程式),若最后溶液中有固体剩余,则溶液中不可能含有的离子是____ 。
(4)FeCl2溶液在空气中容易被氧化,0.1 mol· L-1的FeCl2溶液暴露在空气中,20min 后,Fe2+的浓度变为0.05 mol· L-1,则20 min内,以Fe2+ 表示的平均反应速率为_____________ 若要验证该溶液中Fe2+未被完全氧化,则可以需要加入_____ 若出现_________ 现象,则证明Fe2+未被完全氧化。
(5)下列有关铁及其化合物的说法正确的是________
A.铁是第四周期第VIIIB族元素
B.亚铁盐只有还原性,没有氧化性
C.铁粉和铜粉的混合物可用磁铁吸引的方法分离
D.工业上通常采用电解法来冶炼单质铁
E.Fe3O4是一种纯净物
F.铁粉和氧化铝的混合物是一种铝热剂
(1)Fe3+与SCN-的反应常用来检验Fe3+的存在: Fe3+ + 3SCN-
 Fe(SCN)3
Fe(SCN)3 若溶液中含有Fe3+,则加入KSCN溶液后的现象为
(2)向FeSO4溶液中滴入NaOH溶液,会观察到先产生白色沉淀,后迅速变为灰绿色,久置后变为红褐色,用化学方程式说明产生该现象的原因
(3)FeCl3溶液常被用作蚀刻剂腐蚀印刷电路板: 2Fe3++ Cu==2Fe2+ + Cu2+在过量FeCl3溶液腐蚀印刷电路板后的溶液中,加入过量铁粉,依次发生
(4)FeCl2溶液在空气中容易被氧化,0.1 mol· L-1的FeCl2溶液暴露在空气中,20min 后,Fe2+的浓度变为0.05 mol· L-1,则20 min内,以Fe2+ 表示的平均反应速率为
(5)下列有关铁及其化合物的说法正确的是
A.铁是第四周期第VIIIB族元素
B.亚铁盐只有还原性,没有氧化性
C.铁粉和铜粉的混合物可用磁铁吸引的方法分离
D.工业上通常采用电解法来冶炼单质铁
E.Fe3O4是一种纯净物
F.铁粉和氧化铝的混合物是一种铝热剂
您最近一年使用:0次
5 . 化学平衡状态的改变
【观察思考】完成教材P61页“观察·思考”栏目,观察实验现象,完成下表。
结论:化学平衡是在_______ 下建立起来的,当________ 时,原平衡状态被破坏,并在新的条件下建立起新的平衡状态。化学平衡状态通常会受到_______ 、_______ 、_____ 等因素的影响。
【观察思考】完成教材P61页“观察·思考”栏目,观察实验现象,完成下表。
实验现象 | 热水中混合气体颜色较常温下的 |
实验结论 | 混合气体受热颜色变 混合气体被冷却颜色变 |
您最近一年使用:0次



