化学平衡状态的改变
【观察思考】完成教材P61页“观察·思考”栏目,观察实验现象,完成下表。
结论:化学平衡是在_______ 下建立起来的,当________ 时,原平衡状态被破坏,并在新的条件下建立起新的平衡状态。化学平衡状态通常会受到_______ 、_______ 、_____ 等因素的影响。
【观察思考】完成教材P61页“观察·思考”栏目,观察实验现象,完成下表。
实验现象 | 热水中混合气体颜色较常温下的 |
实验结论 | 混合气体受热颜色变 混合气体被冷却颜色变 |
更新时间:2022-03-02 19:24:49
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如右图所示:
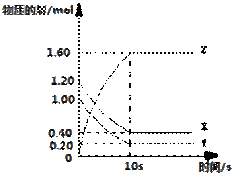
(1)该反应的化学方程式为:_______ 。
(2)反应开始至10s末,X的平均反应速率为:_______ 。
(3)若在第10s时分离出部分Y,则容器中X的物质的量会_______ (填“增大”、“减小”或“不变”)。
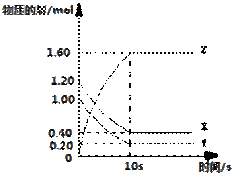
(1)该反应的化学方程式为:
(2)反应开始至10s末,X的平均反应速率为:
(3)若在第10s时分离出部分Y,则容器中X的物质的量会
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】合成氨N2(g)+3H2(g)⇌2NH3(g) ΔH = -92.4 kJ·mol-1。
(1)该反应的化学平衡常数表达式是K=_______ 。
(2)该反应的化学平衡常数K与温度T的关系如表所示:
其中,K1_______ K2(填“>”、“=”或“<”)。
(3)合成氨在农业和国防中有很重要的意义,在实际工业生产中,常采用下列措施,其中可以用勒夏特列原理解释的是_______(填字母)。
(4)在一定温度下,向容积不变的容器中加入2 mol N2、8 mol H2 及固体催化剂,平衡时,容器内气体压强为起始时的80%。反应达到平衡时,则N2的转化率是_______ ,此时反应放出的热量_______ (填“>”、“=”或“<”)92.4 kJ。
(1)该反应的化学平衡常数表达式是K=
(2)该反应的化学平衡常数K与温度T的关系如表所示:
| T / K | 473 | 573 | 673 | …… |
| K | 4.4×10-2 | K1 | K2 | …… |
其中,K1
(3)合成氨在农业和国防中有很重要的意义,在实际工业生产中,常采用下列措施,其中可以用勒夏特列原理解释的是_______(填字母)。
| A.用铁触媒加快化学反应速率 | B.采用较高压强(20 MPa~50 MPa) |
| C.采用较高温度(400℃~500℃) | D.将生成的氨液化并及时从体系中分离出来 |
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】在合成氨工业中,原料气( 、
、 及少量
及少量 、
、 的混合气)在进入合成塔前需经过铜氨液处理,目的是除去其中的CO,其反应为:
的混合气)在进入合成塔前需经过铜氨液处理,目的是除去其中的CO,其反应为:
 。
。
(1)铜氨液吸收CO适宜的生产条件是___________ 。
(2)吸收CO后的铜氨液经过适当处理又可再生,恢复其吸收CO的能力,可供循环使用。铜氨液再生适宜的生产条件是___________ 。
 、
、 及少量
及少量 、
、 的混合气)在进入合成塔前需经过铜氨液处理,目的是除去其中的CO,其反应为:
的混合气)在进入合成塔前需经过铜氨液处理,目的是除去其中的CO,其反应为:
 。
。(1)铜氨液吸收CO适宜的生产条件是
(2)吸收CO后的铜氨液经过适当处理又可再生,恢复其吸收CO的能力,可供循环使用。铜氨液再生适宜的生产条件是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】科学家研究高效催化剂对汽车尾气进行无害化处理,其反应原理为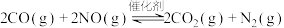
 。回答下列问题:
。回答下列问题:
(1)某温度下,在密闭容器中该反应达到化学平衡后,只改变一种条件对该反应的正、逆反应速率的影响如图甲所示。

①加催化剂对反应速率影响的图像是______ (填字母,下同)。
②适当升高温度对反应速率影响的图像是A,该反应的正反应是__________ 反应(填“吸热”或“放热”)。
③图像D改变的条件是__________ (任写一条)。
(2)在 密闭容器中充入CO和NO共
密闭容器中充入CO和NO共 ,发生反应
,发生反应
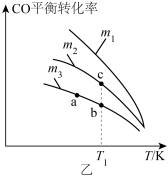
 ,CO的平衡转化率与温度、起始投料比m的关系如图乙所示[起始投料比
,CO的平衡转化率与温度、起始投料比m的关系如图乙所示[起始投料比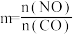 ]。
]。
①该反应的化学平衡常数表达式是__________ 。
②图中a、b、c三点对应的平衡常数 、
、 、
、 相对大小关系是
相对大小关系是__________ , 、
、 、
、 相对大小关系是
相对大小关系是__________ 。
③若 ,温度为
,温度为 ,反应达到平衡所用的时间为
,反应达到平衡所用的时间为 ,CO的平衡转化率为40%。达平衡过程中平均反应速率
,CO的平衡转化率为40%。达平衡过程中平均反应速率
__________  ,平衡时混合气体总物质的量=
,平衡时混合气体总物质的量=__________  ;若
;若 时,该容器中此四种物质均为
时,该容器中此四种物质均为 ,则此时v(正)
,则此时v(正)______ (填“>”“<”或“=”)v(逆)。
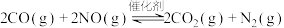
 。回答下列问题:
。回答下列问题:(1)某温度下,在密闭容器中该反应达到化学平衡后,只改变一种条件对该反应的正、逆反应速率的影响如图甲所示。


①加催化剂对反应速率影响的图像是
②适当升高温度对反应速率影响的图像是A,该反应的正反应是
③图像D改变的条件是
(2)在
 密闭容器中充入CO和NO共
密闭容器中充入CO和NO共 ,发生反应
,发生反应
 ,CO的平衡转化率与温度、起始投料比m的关系如图乙所示[起始投料比
,CO的平衡转化率与温度、起始投料比m的关系如图乙所示[起始投料比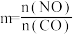 ]。
]。①该反应的化学平衡常数表达式是
②图中a、b、c三点对应的平衡常数
 、
、 、
、 相对大小关系是
相对大小关系是 、
、 、
、 相对大小关系是
相对大小关系是③若
 ,温度为
,温度为 ,反应达到平衡所用的时间为
,反应达到平衡所用的时间为 ,CO的平衡转化率为40%。达平衡过程中平均反应速率
,CO的平衡转化率为40%。达平衡过程中平均反应速率
 ,平衡时混合气体总物质的量=
,平衡时混合气体总物质的量= ;若
;若 时,该容器中此四种物质均为
时,该容器中此四种物质均为 ,则此时v(正)
,则此时v(正)
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】利用反应CO(g)+H2O(g) H2(g)+CO2(g)可得到清洁能源H2。
H2(g)+CO2(g)可得到清洁能源H2。
(1)该反应化学平衡常数表达式K=____ 。
(2)该反应的平衡常数随温度的变化如表:
从上表可以推断:此反应是____ (填“吸热”或“放热”)反应。
(3)830℃时,向容积为2L的密闭容器中充入1molCO与1molH2O,2min时CO为0.6mol。2min内v(CO2)=____ ,此时反应进行的方向是___ ,依据是____ ,可以判断该反应达到平衡的标志是____ (填字母)。
a.体系的压强不再发生变化 b.混合气体的密度不变
c.CO的消耗速率与CO2的消耗速率相等 d.各组分的物质的量浓度不再改变
 H2(g)+CO2(g)可得到清洁能源H2。
H2(g)+CO2(g)可得到清洁能源H2。(1)该反应化学平衡常数表达式K=
(2)该反应的平衡常数随温度的变化如表:
| 温度/℃ | 400 | 500 | 830 | 1000 |
| 平衡常数K | 10 | 9 | 1 | 0.6 |
(3)830℃时,向容积为2L的密闭容器中充入1molCO与1molH2O,2min时CO为0.6mol。2min内v(CO2)=
a.体系的压强不再发生变化 b.混合气体的密度不变
c.CO的消耗速率与CO2的消耗速率相等 d.各组分的物质的量浓度不再改变
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】回答下列问题:
(1)某反应过程的能量变化如图所示。请填写下列空白。
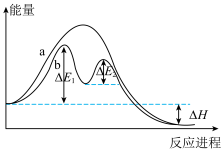
反应过程___________ (填“a”或“b”)有催化剂参与。该反应为___________ 反应(填“放热”或“吸热”),反应热为___________ 。
(2)写出热化学方程式: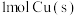 与适量
与适量 反应生成
反应生成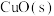 ,放出157.3kJ的热量:
,放出157.3kJ的热量:___________ 。
(3)温度对化学平衡移动的影响如图所示。
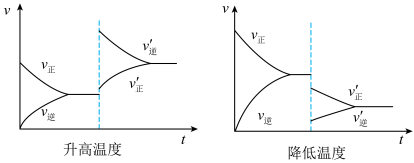
升高温度,平衡向___________ 反应方向移动;降低温度,平衡向___________ 反应方向移动。
(1)某反应过程的能量变化如图所示。请填写下列空白。

反应过程
(2)写出热化学方程式:
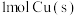 与适量
与适量 反应生成
反应生成 ,放出157.3kJ的热量:
,放出157.3kJ的热量:(3)温度对化学平衡移动的影响如图所示。

升高温度,平衡向
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】现代制备乙烯常用乙烷氧化裂解法,主反应为C2H6(g)+ O2(g)
O2(g) C2H4(g)+H2O(g) ΔH=−110kJ·mol-1,反应时还会生成CH4、CO、CO2等副产物(副反应均为放热反应),如图所示为温度对乙烷氧化裂解反应的影响。[乙烯选择性=
C2H4(g)+H2O(g) ΔH=−110kJ·mol-1,反应时还会生成CH4、CO、CO2等副产物(副反应均为放热反应),如图所示为温度对乙烷氧化裂解反应的影响。[乙烯选择性= ×100%;乙烯收率=乙烷转化率×乙烯选择性]
×100%;乙烯收率=乙烷转化率×乙烯选择性]________ ,反应的最佳温度为_________ 。
A.650℃ B.700℃ C.775℃ D.850℃
(2)工业上,保持体系总压强恒定在100kPa下进行该反应,且通常在乙烷和氧气的混合气体中掺入惰性气体(惰性气体的体积分数为70%),掺入惰性气体的目的是___________ 。
 O2(g)
O2(g) C2H4(g)+H2O(g) ΔH=−110kJ·mol-1,反应时还会生成CH4、CO、CO2等副产物(副反应均为放热反应),如图所示为温度对乙烷氧化裂解反应的影响。[乙烯选择性=
C2H4(g)+H2O(g) ΔH=−110kJ·mol-1,反应时还会生成CH4、CO、CO2等副产物(副反应均为放热反应),如图所示为温度对乙烷氧化裂解反应的影响。[乙烯选择性= ×100%;乙烯收率=乙烷转化率×乙烯选择性]
×100%;乙烯收率=乙烷转化率×乙烯选择性]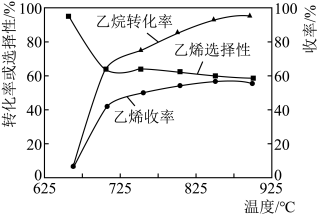
A.650℃ B.700℃ C.775℃ D.850℃
(2)工业上,保持体系总压强恒定在100kPa下进行该反应,且通常在乙烷和氧气的混合气体中掺入惰性气体(惰性气体的体积分数为70%),掺入惰性气体的目的是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】Ⅰ.如图所示,烧瓶A、B中装有相同浓度的NO2和N2O4的混合气体,中间止水夹K夹紧,烧杯甲中盛放100mL6mol·L-1的盐酸,烧杯乙中盛放100mL冷水。现向烧杯甲的溶液中放入25gNaOH固体,同时向烧杯乙中放入25gNH4NO3固体,搅拌使之溶解。
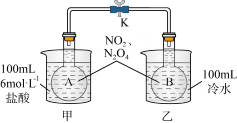
已知:2NO2 N2O4 ΔH<0。
N2O4 ΔH<0。
(1)A瓶中气体颜色____ ,理由是____ 。
(2)B瓶中气体颜色____ ,理由是____ 。
Ⅱ.在水溶液中,橙红色的Cr2O 与黄色的CrO
与黄色的CrO 有下列平衡关系:Cr2O
有下列平衡关系:Cr2O +H2O
+H2O 2CrO
2CrO +2H+。把重铬酸钾(K2Cr2O7)溶于水配成稀溶液呈橙色。
+2H+。把重铬酸钾(K2Cr2O7)溶于水配成稀溶液呈橙色。
(3)向上述溶液中加入NaOH溶液,溶液呈____ 色,因为____ 。
(4)向已加入NaOH溶液的(1)中再加入过量稀硫酸,则溶液呈___ 色,因为____ 。
(5)向原溶液中逐滴加入Ba(NO3)2溶液(已知BaCrO4为黄色沉淀),则平衡____ ,溶液颜色将____ 。

已知:2NO2
 N2O4 ΔH<0。
N2O4 ΔH<0。(1)A瓶中气体颜色
(2)B瓶中气体颜色
Ⅱ.在水溶液中,橙红色的Cr2O
 与黄色的CrO
与黄色的CrO 有下列平衡关系:Cr2O
有下列平衡关系:Cr2O +H2O
+H2O 2CrO
2CrO +2H+。把重铬酸钾(K2Cr2O7)溶于水配成稀溶液呈橙色。
+2H+。把重铬酸钾(K2Cr2O7)溶于水配成稀溶液呈橙色。(3)向上述溶液中加入NaOH溶液,溶液呈
(4)向已加入NaOH溶液的(1)中再加入过量稀硫酸,则溶液呈
(5)向原溶液中逐滴加入Ba(NO3)2溶液(已知BaCrO4为黄色沉淀),则平衡
您最近一年使用:0次



