在合成氨工业中,原料气( 、
、 及少量
及少量 、
、 的混合气)在进入合成塔前需经过铜氨液处理,目的是除去其中的CO,其反应为:
的混合气)在进入合成塔前需经过铜氨液处理,目的是除去其中的CO,其反应为:
 。
。
(1)铜氨液吸收CO适宜的生产条件是___________ 。
(2)吸收CO后的铜氨液经过适当处理又可再生,恢复其吸收CO的能力,可供循环使用。铜氨液再生适宜的生产条件是___________ 。
 、
、 及少量
及少量 、
、 的混合气)在进入合成塔前需经过铜氨液处理,目的是除去其中的CO,其反应为:
的混合气)在进入合成塔前需经过铜氨液处理,目的是除去其中的CO,其反应为:
 。
。(1)铜氨液吸收CO适宜的生产条件是
(2)吸收CO后的铜氨液经过适当处理又可再生,恢复其吸收CO的能力,可供循环使用。铜氨液再生适宜的生产条件是
更新时间:2021-12-02 08:45:25
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】 分解的热化学方程式为
分解的热化学方程式为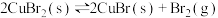
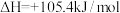 。在密闭容器中将过量
。在密闭容器中将过量 于
于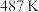 下加热分解,平衡时
下加热分解,平衡时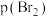 为
为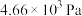 。
。
(1)如果反应体系的容积不变,提高反应温度,则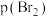 将会
将会___________ (填“增大”“减小”或“不变”)。
(2)利用“化学蒸气转移法”制备 晶体,发生以下反应:
晶体,发生以下反应:
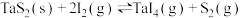
 。
。
①反应的平衡常数表达式K=___________ 。若K=1,向某恒容密闭容器中加入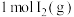 与足量
与足量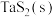 ,
, 的平衡转化率为
的平衡转化率为___________ (结果精确到0.1%)。
②如图所示,上述反应在石英真空管中进行,先在温度为T2的一端放入未提纯的 粉末与少量
粉末与少量 ,一段时间后,在温度为T1的一端得到了纯净的
,一段时间后,在温度为T1的一端得到了纯净的 晶体,则温度T1
晶体,则温度T1___________ (填“>”“<”或“=”)T2.上述反应体系中循环使用的物质是___________ 。

 分解的热化学方程式为
分解的热化学方程式为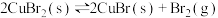
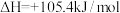 。在密闭容器中将过量
。在密闭容器中将过量 于
于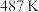 下加热分解,平衡时
下加热分解,平衡时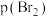 为
为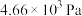 。
。(1)如果反应体系的容积不变,提高反应温度,则
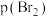 将会
将会(2)利用“化学蒸气转移法”制备
 晶体,发生以下反应:
晶体,发生以下反应: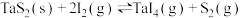
 。
。①反应的平衡常数表达式K=
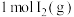 与足量
与足量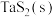 ,
, 的平衡转化率为
的平衡转化率为②如图所示,上述反应在石英真空管中进行,先在温度为T2的一端放入未提纯的
 粉末与少量
粉末与少量 ,一段时间后,在温度为T1的一端得到了纯净的
,一段时间后,在温度为T1的一端得到了纯净的 晶体,则温度T1
晶体,则温度T1
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】氮、碳氧化物的无害化处理是研究的热点。一定条件下 发生如下反应:
发生如下反应:
Ⅰ.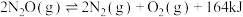
Ⅱ.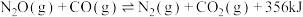
完成下列填空:
(1)反应Ⅰ平衡常数的表达式K=_______ 。
(2)某温度下,反应Ⅰ的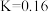 ,该温度下,测得容器中
,该温度下,测得容器中 、
、 、
、 的浓度分别为
的浓度分别为 、
、 、
、 ,此时,反应Ⅰ是否处于平衡状态?若不是,预测反应的方向。
,此时,反应Ⅰ是否处于平衡状态?若不是,预测反应的方向。_______
(3)甲为10L的恒温容器。盛有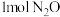 和1mol CO,发生反应Ⅰ和反应Ⅱ,5min时,测得CO转化率为60%,
和1mol CO,发生反应Ⅰ和反应Ⅱ,5min时,测得CO转化率为60%,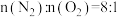 ,则
,则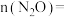
_______ mol;0~5min, 的平均反应速率
的平均反应速率
_______  。
。
(4)乙为10L的绝热容器。向其中充入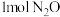 和1mol CO,发生反应Ⅰ和反应Ⅱ,乙中反应达到平衡的时间
和1mol CO,发生反应Ⅰ和反应Ⅱ,乙中反应达到平衡的时间_______ 甲;此时乙中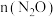 比甲中
比甲中_______ (以上两空选填“>”“<”或“=”),理由是:_______ 。
(5)不同压强的密闭容器中,分别充入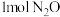 和1mol CO,发生反应Ⅰ和反应Ⅱ,测得
和1mol CO,发生反应Ⅰ和反应Ⅱ,测得 的平衡转化率与温度的关系如图所示。
的平衡转化率与温度的关系如图所示。
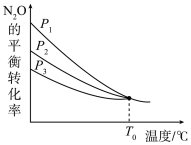
P1、P2、P3由小到大的顺序为_______ ;温度高于T0℃时,容器内发生的主要反应为_______ (填“Ⅰ”“Ⅱ”或“Ⅰ和Ⅱ”)。
 发生如下反应:
发生如下反应:Ⅰ.
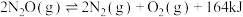
Ⅱ.
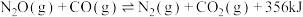
完成下列填空:
(1)反应Ⅰ平衡常数的表达式K=
(2)某温度下,反应Ⅰ的
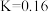 ,该温度下,测得容器中
,该温度下,测得容器中 、
、 、
、 的浓度分别为
的浓度分别为 、
、 、
、 ,此时,反应Ⅰ是否处于平衡状态?若不是,预测反应的方向。
,此时,反应Ⅰ是否处于平衡状态?若不是,预测反应的方向。(3)甲为10L的恒温容器。盛有
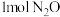 和1mol CO,发生反应Ⅰ和反应Ⅱ,5min时,测得CO转化率为60%,
和1mol CO,发生反应Ⅰ和反应Ⅱ,5min时,测得CO转化率为60%,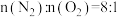 ,则
,则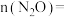
 的平均反应速率
的平均反应速率
 。
。(4)乙为10L的绝热容器。向其中充入
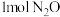 和1mol CO,发生反应Ⅰ和反应Ⅱ,乙中反应达到平衡的时间
和1mol CO,发生反应Ⅰ和反应Ⅱ,乙中反应达到平衡的时间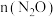 比甲中
比甲中(5)不同压强的密闭容器中,分别充入
 和1mol CO,发生反应Ⅰ和反应Ⅱ,测得
和1mol CO,发生反应Ⅰ和反应Ⅱ,测得 的平衡转化率与温度的关系如图所示。
的平衡转化率与温度的关系如图所示。
P1、P2、P3由小到大的顺序为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】密闭容器中发生反应: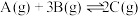
 ,根据下列
,根据下列 图象,回答问题:
图象,回答问题:
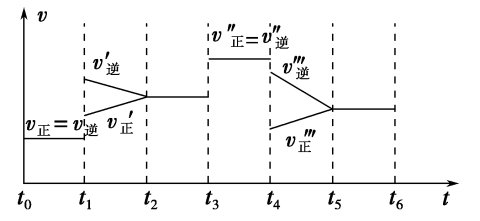
(1)下列时刻所改变的外界条件是
_______ ;
_______ ;
_______ 。
(2)反应速率最快的时间段是_______ 。
(3)下列措施能增大正反应速率的是_______。
 ,根据下列
,根据下列 图象,回答问题:
图象,回答问题:
(1)下列时刻所改变的外界条件是



(2)反应速率最快的时间段是
(3)下列措施能增大正反应速率的是_______。
A.通入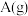 | B.分离出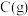 | C.降温 | D.增大容积 |
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】化学平衡的移动
由于温度、压强、浓度的变化而使可逆反应由一个_______ 变为另一个_______ 的过程.
由于温度、压强、浓度的变化而使可逆反应由一个
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】工业上生产硫酸时,利用催化氧化反应将SO2转化为SO3是一个关键步骤、压强及温度对SO2转化率的影响如下表(原料气各成分的体积分数为:SO27%,O211%,N282%):
(1)已知SO2的催化氧化是放热反应,如何利用表中数据推断此结论?_______ ;
(2)在400℃~500℃时,SO2的催化氧化采用常压而不是高压,主要原因是_______ 。
(3)选择适宜的催化剂,是否可以提高SO2的转化率?_______ (填“是”或“否”),是否可以增大该反应所放出的热量?_______ (填“是”或“否”)。
(4)已知:2SO2(g)+O2(g) 2SO3(g) ΔH=-196.6kJ/mol,则每生产1万吨98%硫酸所需要的SO3的质量为
2SO3(g) ΔH=-196.6kJ/mol,则每生产1万吨98%硫酸所需要的SO3的质量为_______ t。由SO2生产这些SO3所放出的热量为_______ kJ。
 | 0.1 | 0.5 | 1 | 10 |
| 400 | 99.2 | 99.6 | 99.7 | 99.9 |
| 500 | 93.5 | 96.9 | 97.8 | 99.3 |
| 600 | 73.7 | 85.8 | 89.5 | 96.4 |
(2)在400℃~500℃时,SO2的催化氧化采用常压而不是高压,主要原因是
(3)选择适宜的催化剂,是否可以提高SO2的转化率?
(4)已知:2SO2(g)+O2(g)
 2SO3(g) ΔH=-196.6kJ/mol,则每生产1万吨98%硫酸所需要的SO3的质量为
2SO3(g) ΔH=-196.6kJ/mol,则每生产1万吨98%硫酸所需要的SO3的质量为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】现有反应mA(g)+nB(g) pC(g)+qD(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:
pC(g)+qD(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:
(1)该反应的逆反应是________ 热反应,且m+n______ p+q(填“>”、“<”或“=”)。
(2)若加入催化剂,平衡时气体混合物的总物质的量________ (填“增大”、“减小”或“不变”)。
(3)若B是有色物质,A、C、D均为无色物质,则加入C(体积不变)时混合物的颜色__________ (填“变深”、“变浅”或“不变”),而维持容器内气体的压强不变,充入氖气时,平衡__________ 移动(填“向左”、“向右”、或“不”)。
 pC(g)+qD(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:
pC(g)+qD(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:(1)该反应的逆反应是
(2)若加入催化剂,平衡时气体混合物的总物质的量
(3)若B是有色物质,A、C、D均为无色物质,则加入C(体积不变)时混合物的颜色
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】可逆反应 在平衡移动时的颜色变化可以用来指示放热过程和吸热过程。下面是某同学的部分实验报告。
在平衡移动时的颜色变化可以用来指示放热过程和吸热过程。下面是某同学的部分实验报告。
(1)根据甲烧杯中的现象,请画出CaO与H2O反应过程的能量变化示意图_________ 。
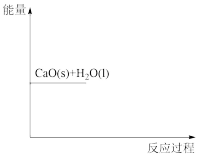
(2)除了CaO,向甲烧杯中加入_______ (填物质名称)也可以获得实验中相同的现象。
(3)NH4NO3晶体溶于水是_______ (填“放热”或“吸热”)过程,乙烧杯中NO2球的红棕色变浅,说明平衡 ΔH
ΔH_______ 0(填“>”或“<”)。
 在平衡移动时的颜色变化可以用来指示放热过程和吸热过程。下面是某同学的部分实验报告。
在平衡移动时的颜色变化可以用来指示放热过程和吸热过程。下面是某同学的部分实验报告。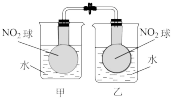 | 1.向甲烧杯中投入一定量的CaO固体,此烧杯中NO2球的红棕色变深。 2.向乙烧杯中加入NH4NO3晶体,此烧杯中NO2球的红棕色变浅。 |
(1)根据甲烧杯中的现象,请画出CaO与H2O反应过程的能量变化示意图

(2)除了CaO,向甲烧杯中加入
(3)NH4NO3晶体溶于水是
 ΔH
ΔH
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】已知:N2(g)+3H2(g) 2NH3(g)ΔH<0。在密闭容器中,充入2molN2和6molH2使之发生反应:
2NH3(g)ΔH<0。在密闭容器中,充入2molN2和6molH2使之发生反应:
(1)当反应达到平衡时,N2和H2的转化率比是___ 。
(2)当达到平衡时,保持体积不变充入氩气,平衡将向___ 移动。(填“向左”、“向右”或“不”)。
(3)当达到平衡时,将c(N2)、c(H2)、c(NH3)同时减小一倍,平衡将向___ 移动。
(4)若有两容器都充入2molN2和6molH2,甲容器保持恒温、恒容,乙容器保持恒容绝热,同时开始反应,更先达平衡的是___ 容器(填“甲”或“乙”),甲中N2的转化率比乙中的更___ (填“高”或“低”)。
 2NH3(g)ΔH<0。在密闭容器中,充入2molN2和6molH2使之发生反应:
2NH3(g)ΔH<0。在密闭容器中,充入2molN2和6molH2使之发生反应:(1)当反应达到平衡时,N2和H2的转化率比是
(2)当达到平衡时,保持体积不变充入氩气,平衡将向
(3)当达到平衡时,将c(N2)、c(H2)、c(NH3)同时减小一倍,平衡将向
(4)若有两容器都充入2molN2和6molH2,甲容器保持恒温、恒容,乙容器保持恒容绝热,同时开始反应,更先达平衡的是
您最近一年使用:0次



