名校
1 . 从平衡移动的角度解释实验室用饱和食盐水收集Cl2的原因___________ 。
您最近一年使用:0次
22-23高一下·上海·期末
2 . 工业合成氨
(1)合成氨的适宜条件探究:N2(g)+3H2(g) 2NH3(g) + Q(Q>0)
2NH3(g) + Q(Q>0)
∴合成氨的合理生产条件:① 使用___________ 为催化剂 ②一定程度的加压 ③温度控制在催化剂的活性温度(500℃) ④及时分离___________
(1)合成氨的适宜条件探究:N2(g)+3H2(g)
 2NH3(g) + Q(Q>0)
2NH3(g) + Q(Q>0)| 反应条件 | 对化学反应速率的影响 | 对平衡混合物中NH3含量的影响 | 化学反应速率与化学平衡综合考虑 |
| 增大压强 | 影响一致,应 | ||
| 升高温度 | 影响 | ||
| 使用催化剂 | 用合适催化剂有利于加快反应速率 | ||
| 增加反应物浓度 | 平衡向 | 影响一致应 |
您最近一年使用:0次
3 . 科学家研究高效催化剂对汽车尾气进行无害化处理,其反应原理为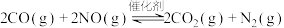
 。回答下列问题:
。回答下列问题:
(1)某温度下,在密闭容器中该反应达到化学平衡后,只改变一种条件对该反应的正、逆反应速率的影响如图甲所示。

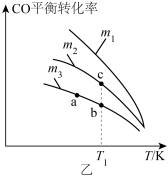
①加催化剂对反应速率影响的图像是______ (填字母,下同)。
②适当升高温度对反应速率影响的图像是A,该反应的正反应是__________ 反应(填“吸热”或“放热”)。
③图像D改变的条件是__________ (任写一条)。
(2)在 密闭容器中充入CO和NO共
密闭容器中充入CO和NO共 ,发生反应
,发生反应
 ,CO的平衡转化率与温度、起始投料比m的关系如图乙所示[起始投料比
,CO的平衡转化率与温度、起始投料比m的关系如图乙所示[起始投料比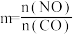 ]。
]。
①该反应的化学平衡常数表达式是__________ 。
②图中a、b、c三点对应的平衡常数 、
、 、
、 相对大小关系是
相对大小关系是__________ , 、
、 、
、 相对大小关系是
相对大小关系是__________ 。
③若 ,温度为
,温度为 ,反应达到平衡所用的时间为
,反应达到平衡所用的时间为 ,CO的平衡转化率为40%。达平衡过程中平均反应速率
,CO的平衡转化率为40%。达平衡过程中平均反应速率
__________  ,平衡时混合气体总物质的量=
,平衡时混合气体总物质的量=__________  ;若
;若 时,该容器中此四种物质均为
时,该容器中此四种物质均为 ,则此时v(正)
,则此时v(正)______ (填“>”“<”或“=”)v(逆)。
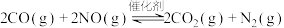
 。回答下列问题:
。回答下列问题:(1)某温度下,在密闭容器中该反应达到化学平衡后,只改变一种条件对该反应的正、逆反应速率的影响如图甲所示。


①加催化剂对反应速率影响的图像是
②适当升高温度对反应速率影响的图像是A,该反应的正反应是
③图像D改变的条件是
(2)在
 密闭容器中充入CO和NO共
密闭容器中充入CO和NO共 ,发生反应
,发生反应
 ,CO的平衡转化率与温度、起始投料比m的关系如图乙所示[起始投料比
,CO的平衡转化率与温度、起始投料比m的关系如图乙所示[起始投料比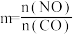 ]。
]。①该反应的化学平衡常数表达式是
②图中a、b、c三点对应的平衡常数
 、
、 、
、 相对大小关系是
相对大小关系是 、
、 、
、 相对大小关系是
相对大小关系是③若
 ,温度为
,温度为 ,反应达到平衡所用的时间为
,反应达到平衡所用的时间为 ,CO的平衡转化率为40%。达平衡过程中平均反应速率
,CO的平衡转化率为40%。达平衡过程中平均反应速率
 ,平衡时混合气体总物质的量=
,平衡时混合气体总物质的量= ;若
;若 时,该容器中此四种物质均为
时,该容器中此四种物质均为 ,则此时v(正)
,则此时v(正)
您最近一年使用:0次
名校
解题方法
4 . 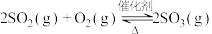
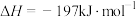 该反应在工业制备硫酸中有重要应用。下列叙述正确的是
该反应在工业制备硫酸中有重要应用。下列叙述正确的是
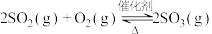
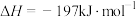 该反应在工业制备硫酸中有重要应用。下列叙述正确的是
该反应在工业制备硫酸中有重要应用。下列叙述正确的是| A.达到反应限度时,反应放出197kJ的热量 |
B.提高反应温度,可实现 的完全转化 的完全转化 |
C.工业生产中可通过增大 浓度来提升 浓度来提升 转化率 转化率 |
D.工业制备硫酸过程中将生成的 用水吸收制得 用水吸收制得 |
您最近一年使用:0次
2023-05-17更新
|
341次组卷
|
2卷引用:辽宁省辽东区域教育科研共同体2022--2023学年高一下学期期中调研化学试题
22-23高二上·广西玉林·期末
5 . 下列说法正确的是
A.某温度下,反应 ,在密闭容器中达到平衡,恒容下,充入一定量的 ,在密闭容器中达到平衡,恒容下,充入一定量的 , , 的平衡转化率增大 的平衡转化率增大 |
B.恒温恒容情况下,发生反应: ,当混合气体密度保持不变时,说明反应已达到平衡 ,当混合气体密度保持不变时,说明反应已达到平衡 |
C.合成氨工业中,恒温恒容情况下,充入惰性气体 ,体系压强增大,反应速率增大 ,体系压强增大,反应速率增大 |
D.某温度下,可逆反应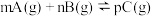 的平衡常数为 的平衡常数为 ,若缩小反应器的容积,能使平衡正向移动,则 ,若缩小反应器的容积,能使平衡正向移动,则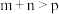 ,并且 ,并且 增大 增大 |
您最近一年使用:0次
名校
6 . 可逆反应2SO2+O2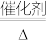 2SO3 △H<0,开始把2molSO2和1molO2充入容积为2L的恒容密闭容器中,在500℃条件下达化学平衡,下列说法中正确的是
2SO3 △H<0,开始把2molSO2和1molO2充入容积为2L的恒容密闭容器中,在500℃条件下达化学平衡,下列说法中正确的是
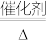 2SO3 △H<0,开始把2molSO2和1molO2充入容积为2L的恒容密闭容器中,在500℃条件下达化学平衡,下列说法中正确的是
2SO3 △H<0,开始把2molSO2和1molO2充入容积为2L的恒容密闭容器中,在500℃条件下达化学平衡,下列说法中正确的是| A.升高温度平衡向正反应方向移动 |
| B.增大压强SO2的转化率增大 |
| C.加入催化剂平衡不发生移动,但反应速率加快 |
| D.只增大SO2浓度平衡不移动 |
您最近一年使用:0次
2022高一·全国·专题练习
7 . 向新制氯水中加入碳酸钙粉末,能增加氯水中HClO的浓度吗?为什么?______
您最近一年使用:0次
8 . 回答下列问题:
(1)在密闭容器中,加热一氧化碳和水蒸气的气体混合物,在催化剂存在下发生反应: ,500℃时,平衡常数
,500℃时,平衡常数 。若反应开始时,一氧化碳和水蒸气的浓度都是0.2mol/L,则平衡时CO的体积分数为
。若反应开始时,一氧化碳和水蒸气的浓度都是0.2mol/L,则平衡时CO的体积分数为_______ 。
(2)在恒温恒压的密闭容器中,按照n(A):n(B)=1:4投料,发生如下反应①和②
①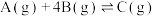 ;②
;②
总压为 ,A的转化率为a,C的分压为P,则反应①的
,A的转化率为a,C的分压为P,则反应①的
_______ (列出算式即可,用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(3)将等物质的量的X、Y气体充入一个密闭容器中,在一定条件下发生反应 并达到平衡状态,若保持容器容积不变再通入一定量的Z,则平衡如何移动
并达到平衡状态,若保持容器容积不变再通入一定量的Z,则平衡如何移动_______ (填“正移”“逆移”或“不移”);达新平衡后,X的体积分数如何变化_______ (填“增大”“减小”或“不变”)。
(1)在密闭容器中,加热一氧化碳和水蒸气的气体混合物,在催化剂存在下发生反应:
 ,500℃时,平衡常数
,500℃时,平衡常数 。若反应开始时,一氧化碳和水蒸气的浓度都是0.2mol/L,则平衡时CO的体积分数为
。若反应开始时,一氧化碳和水蒸气的浓度都是0.2mol/L,则平衡时CO的体积分数为(2)在恒温恒压的密闭容器中,按照n(A):n(B)=1:4投料,发生如下反应①和②
①
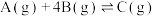 ;②
;②
总压为
 ,A的转化率为a,C的分压为P,则反应①的
,A的转化率为a,C的分压为P,则反应①的
(3)将等物质的量的X、Y气体充入一个密闭容器中,在一定条件下发生反应
 并达到平衡状态,若保持容器容积不变再通入一定量的Z,则平衡如何移动
并达到平衡状态,若保持容器容积不变再通入一定量的Z,则平衡如何移动
您最近一年使用:0次
9 . 回答下列问题:
(1)在密闭容器中,加热一氧化碳和水蒸气的气体混合物,在催化剂存在下发生反应: ,500℃时,平衡常数
,500℃时,平衡常数 。若反应开始时,一氧化碳和水蒸气的浓度都是0.2mol/L,则平衡时CO的体积分数为
。若反应开始时,一氧化碳和水蒸气的浓度都是0.2mol/L,则平衡时CO的体积分数为_______ 。
(2)在恒温恒压的密闭容器中,按照n(A):n(B)=1:4投料,发生如下反应①和②
①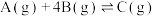 ;②
;②
总压为 ,A的转化率为a,C的分压为P,则反应①的
,A的转化率为a,C的分压为P,则反应①的
_______ (列出算式即可,用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(3)将等物质的量的X、Y气体充入一个密闭容器中,在一定条件下发生反应 并达到平衡状态,若保持容器容积不变再通入一定量的Z,则平衡如何移动
并达到平衡状态,若保持容器容积不变再通入一定量的Z,则平衡如何移动_______ (填“正移”“逆移”或“不移”);达新平衡后,X的体积分数如何变化_______ (填“增大”“减小”或“不变”)。
(1)在密闭容器中,加热一氧化碳和水蒸气的气体混合物,在催化剂存在下发生反应:
 ,500℃时,平衡常数
,500℃时,平衡常数 。若反应开始时,一氧化碳和水蒸气的浓度都是0.2mol/L,则平衡时CO的体积分数为
。若反应开始时,一氧化碳和水蒸气的浓度都是0.2mol/L,则平衡时CO的体积分数为(2)在恒温恒压的密闭容器中,按照n(A):n(B)=1:4投料,发生如下反应①和②
①
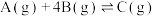 ;②
;②
总压为
 ,A的转化率为a,C的分压为P,则反应①的
,A的转化率为a,C的分压为P,则反应①的
(3)将等物质的量的X、Y气体充入一个密闭容器中,在一定条件下发生反应
 并达到平衡状态,若保持容器容积不变再通入一定量的Z,则平衡如何移动
并达到平衡状态,若保持容器容积不变再通入一定量的Z,则平衡如何移动
您最近一年使用:0次
名校
解题方法
10 . 铁元素及其化合物在生活生产中有广泛的用途。回答下列问题:
(1)Fe3+与SCN-的反应常用来检验Fe3+的存在: Fe3+ + 3SCN- Fe(SCN)3
Fe(SCN)3
若溶液中含有Fe3+,则加入KSCN溶液后的现象为_________ 向加入KSCN后的混合溶液中再加入少量NaOH固体,观察到的现象是_____________ ,产生该现象的原因是________________ 。
(2)向FeSO4溶液中滴入NaOH溶液,会观察到先产生白色沉淀,后迅速变为灰绿色,久置后变为红褐色,用化学方程式说明产生该现象的原因__________________ 。
(3)FeCl3溶液常被用作蚀刻剂腐蚀印刷电路板: 2Fe3++ Cu==2Fe2+ + Cu2+在过量FeCl3溶液腐蚀印刷电路板后的溶液中,加入过量铁粉,依次发生______ 、________ 两个反应(写离子方程式),若最后溶液中有固体剩余,则溶液中不可能含有的离子是____ 。
(4)FeCl2溶液在空气中容易被氧化,0.1 mol· L-1的FeCl2溶液暴露在空气中,20min 后,Fe2+的浓度变为0.05 mol· L-1,则20 min内,以Fe2+ 表示的平均反应速率为_____________ 若要验证该溶液中Fe2+未被完全氧化,则可以需要加入_____ 若出现_________ 现象,则证明Fe2+未被完全氧化。
(5)下列有关铁及其化合物的说法正确的是________
A.铁是第四周期第VIIIB族元素
B.亚铁盐只有还原性,没有氧化性
C.铁粉和铜粉的混合物可用磁铁吸引的方法分离
D.工业上通常采用电解法来冶炼单质铁
E.Fe3O4是一种纯净物
F.铁粉和氧化铝的混合物是一种铝热剂
(1)Fe3+与SCN-的反应常用来检验Fe3+的存在: Fe3+ + 3SCN-
 Fe(SCN)3
Fe(SCN)3 若溶液中含有Fe3+,则加入KSCN溶液后的现象为
(2)向FeSO4溶液中滴入NaOH溶液,会观察到先产生白色沉淀,后迅速变为灰绿色,久置后变为红褐色,用化学方程式说明产生该现象的原因
(3)FeCl3溶液常被用作蚀刻剂腐蚀印刷电路板: 2Fe3++ Cu==2Fe2+ + Cu2+在过量FeCl3溶液腐蚀印刷电路板后的溶液中,加入过量铁粉,依次发生
(4)FeCl2溶液在空气中容易被氧化,0.1 mol· L-1的FeCl2溶液暴露在空气中,20min 后,Fe2+的浓度变为0.05 mol· L-1,则20 min内,以Fe2+ 表示的平均反应速率为
(5)下列有关铁及其化合物的说法正确的是
A.铁是第四周期第VIIIB族元素
B.亚铁盐只有还原性,没有氧化性
C.铁粉和铜粉的混合物可用磁铁吸引的方法分离
D.工业上通常采用电解法来冶炼单质铁
E.Fe3O4是一种纯净物
F.铁粉和氧化铝的混合物是一种铝热剂
您最近一年使用:0次



