1 . 电离平衡常数的影响因素
电离平衡常数K 值只与电解质____________ 和______ 有关,与浓度______ 。
由于电离是______ 的,所以电离平衡常数随着温度的升高而______ 。
电离平衡常数K 值只与电解质
由于电离是
您最近一年使用:0次
解题方法
2 . 温度变化对化学平衡影响的规律
mA(g)+nB(g) pC(g),当反应达平衡后,若温度改变,其反应速率的变化曲线分别如下图所示:
pC(g),当反应达平衡后,若温度改变,其反应速率的变化曲线分别如下图所示:
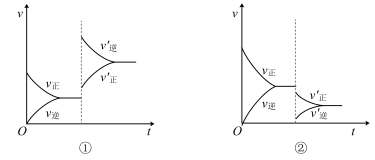
(1)图①表示的温度变化是________ ,平衡移动方向是________ 方向。
(2)图②表示的温度变化是________ ,平衡移动方向是________ 方向。
(3)正反应是放热反应,逆反应是________ 热反应。温度升高,平衡向________ 方向移动;温度降低,平衡向________ 方向移动。
mA(g)+nB(g)
 pC(g),当反应达平衡后,若温度改变,其反应速率的变化曲线分别如下图所示:
pC(g),当反应达平衡后,若温度改变,其反应速率的变化曲线分别如下图所示:
(1)图①表示的温度变化是
(2)图②表示的温度变化是
(3)正反应是放热反应,逆反应是
您最近一年使用:0次
解题方法
3 . 改变温度对平衡常数的影响
(1)改变温度可以使化学平衡发生移动,化学平衡常数也会发生改变,通过分析以下两个反应,总结出温度对化学平衡常数的影响规律。
①N2(g)+3H2(g) 2NH3(g)
2NH3(g)
化学平衡常数K1=_______ ,升温化学平衡向逆向移动,K1______ (填“增大”或“减小”,下同),ΔH____ 0(填“>”或“<”,下同)。
②CO2(g)+H2(g) CO(g)+H2O(g)
CO(g)+H2O(g)
化学平衡常数K2=________ ,升温化学平衡向正向移动,K2________ ,ΔH________ 0。
(2)判断反应的热效应
①升高温度:K值增大→正反应为________ 反应;K值减小→正反应为________ 反应。
②降低温度:K值增大→正反应为________ 反应;K值减小→正反应为________ 反应。
(1)改变温度可以使化学平衡发生移动,化学平衡常数也会发生改变,通过分析以下两个反应,总结出温度对化学平衡常数的影响规律。
①N2(g)+3H2(g)
 2NH3(g)
2NH3(g)化学平衡常数K1=
②CO2(g)+H2(g)
 CO(g)+H2O(g)
CO(g)+H2O(g)化学平衡常数K2=
(2)判断反应的热效应
①升高温度:K值增大→正反应为
②降低温度:K值增大→正反应为
您最近一年使用:0次
4 . 温度对化学平衡的影响有什么规律?提示:升高温度,平衡向着吸热反应的方向移动;降低温度,平衡向着放热反应的方向移动。
_________ 。
您最近一年使用:0次
5 . 探究外界条件变化化学平衡的影响。向一密闭容器中通入1 mol N2、3 mol H2发生反应N2(g)+3H2(g) 2NH3(g) ΔH<0,一段时间后达到平衡。
2NH3(g) ΔH<0,一段时间后达到平衡。
(1)若增大N2的浓度,平衡移动的方向是_____________ ;达新平衡时,氮气的浓度与改变时相比较,其变化是________ 。
(2)若升高温度,平衡移动的方向是__________ ;达新平衡时的温度与改变时相比较,其变化是________ 。
(3)若增大压强,平衡移动的方向是__________ ;达新平衡时的压强与改变时相比较,其变化是________ 。
 2NH3(g) ΔH<0,一段时间后达到平衡。
2NH3(g) ΔH<0,一段时间后达到平衡。(1)若增大N2的浓度,平衡移动的方向是
(2)若升高温度,平衡移动的方向是
(3)若增大压强,平衡移动的方向是
您最近一年使用:0次
2023-07-15更新
|
68次组卷
|
2卷引用:2.3.2温度 催化剂对化学平衡的影响 课前
6 . “先拐先平”原则
在化学平衡图像中,先出现拐点的反应则先达到平衡,先出现拐点的曲线表示的温度较高(如图1)或表示的压强较大(如图2)[仍以aA(g)+bB(g) cC(g)为例]。
cC(g)为例]。
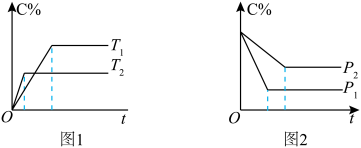
根据图像回答下列问题:
(1)图1中,温度T1、T2的大小关系是___________ ,温度升高,C%(C的含量)的变化是___________ ,化学平衡___________ 移动,正反应是___________ 反应。
(2)图2中,压强p1、p2的大小关系是___________ ,压强增大,C%(C的含量)的变化是___________ ,化学平衡___________ 移动,a+b___________ c。
在化学平衡图像中,先出现拐点的反应则先达到平衡,先出现拐点的曲线表示的温度较高(如图1)或表示的压强较大(如图2)[仍以aA(g)+bB(g)
 cC(g)为例]。
cC(g)为例]。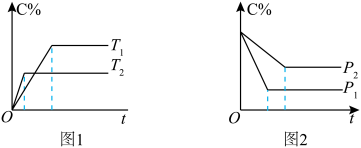
根据图像回答下列问题:
(1)图1中,温度T1、T2的大小关系是
(2)图2中,压强p1、p2的大小关系是
您最近一年使用:0次
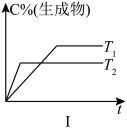
7 . 百分含量(或转化率)—时间—温度(或压强)图像
(1)T2___________ T1,温度升高,平衡___________ 移动,正反应是___________ 反应。
(2)p2___________ p1,压强增大,A(反应物)的转化率___________ ,说明正反应是___________ 的反应。
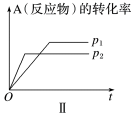
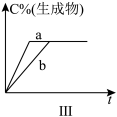
(3)生成物C的百分含量不变,说明平衡___________ 移动,但反应速率a___________ b,故a可能___________ ;若该反应是反应前后气体分子数目的可逆反应,a也可能是___________ 。
(1)T2

(2)p2

(3)生成物C的百分含量不变,说明平衡

您最近一年使用:0次
8 . 化学反应达到平衡后,改变温度平衡是否一定发生移动________ ?
您最近一年使用:0次
9 . 化学平衡状态的改变
【观察思考】完成教材P61页“观察·思考”栏目,观察实验现象,完成下表。
结论:化学平衡是在_______ 下建立起来的,当________ 时,原平衡状态被破坏,并在新的条件下建立起新的平衡状态。化学平衡状态通常会受到_______ 、_______ 、_____ 等因素的影响。
【观察思考】完成教材P61页“观察·思考”栏目,观察实验现象,完成下表。
实验现象 | 热水中混合气体颜色较常温下的 |
实验结论 | 混合气体受热颜色变 混合气体被冷却颜色变 |
您最近一年使用:0次
10 . 预测温度对化学平衡的影响
在容积一定的密闭容器中,化学反应mA(g)+nB(g) pC(g)+qD(g) ΔH>0,达到平衡时:
pC(g)+qD(g) ΔH>0,达到平衡时:
(1)若升高温度,K值___________ ,平衡___________ 移动,c(A)___________ ,反应物B的转化率___________ ,混合气体的密度___________ 。
(2)若降低温度,K值___________ ,平衡___________ 移动,反应产物C、D的浓度___________ ,混合气体的密度___________ 。
【拓展延伸】
(1)催化剂对平衡常数无影响,因为催化剂不能改变平衡常数,也不能改变平衡状态时反应混合物的组成,K与Q都不改变,即Q=K,因而平衡不移动。
(2)催化剂虽然不能使平衡移动,但能缩短到达平衡的时间。
【情境问题思考】
(3)填空
在容积一定的密闭容器中,化学反应mA(g)+nB(g)
 pC(g)+qD(g) ΔH>0,达到平衡时:
pC(g)+qD(g) ΔH>0,达到平衡时:(1)若升高温度,K值
(2)若降低温度,K值
【拓展延伸】
(1)催化剂对平衡常数无影响,因为催化剂不能改变平衡常数,也不能改变平衡状态时反应混合物的组成,K与Q都不改变,即Q=K,因而平衡不移动。
(2)催化剂虽然不能使平衡移动,但能缩短到达平衡的时间。
【情境问题思考】
(3)填空
| 实验原理 | 2NO2(g) N2O4(g) ΔH=-57.2 kJ·mol-1 N2O4(g) ΔH=-57.2 kJ·mol-1红棕色 无色 |
| 实验装置 |  |
| 实验现象 | 热水中红棕色加深;冰水中红棕色变浅 |
| 实验结论 | 体系受热颜色 |
您最近一年使用:0次



