名校
1 . 1molCO2与足量的碳在恒容密闭容器中反应:C(s)+CO2(g)⇌2CO(g)。测得平衡时,体系中气体体积分数与温度的关系如图所示:
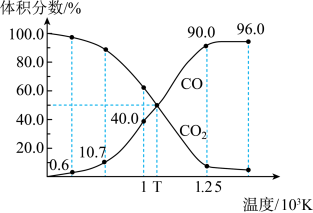
| A.1×103K时,若充入惰性气体,v正、v逆均减小,v逆变化幅度更大 |
| B.1×103K时,突然升温,v正、v逆均增大,v正变化幅度更大 |
| C.1×103K时,反应达平衡后CO2的转化率为25.0% |
| D.T×103K时,若再充入等体积的CO2和CO,平衡向逆反应方向移动 |
您最近一年使用:0次
2 . 对于反应Ag2CO3(s) ⇌Ag2O(s) + CO2(g),其298.15K下的反应焓变为ΔH= 81.5kJ·mol-1,下列说法中 正确的是
| A.Ag2CO3的转化率随着温度升高而增大 |
| B.反应平衡常数不随其他因素而改变 |
| C.反应体系中存在Ag2CO3,Ag2O和CO2 |
| D.在敞开体系中,Ag2CO3完 全分解为Ag2O |
您最近一年使用:0次
3 . 某些稀土合金晶体结构中,原子排列十分紧密,具有良好的贮氢功能,常用作贮氢材料。目前,贮氢合金中最具有代表性的是镧镍-合金(LaxNiy),其结构如图,已知在200-300kPa的压强下,1mol合金最多能吸收3mol氢气同时放出31.77kJ的能量。下列说法正确的是
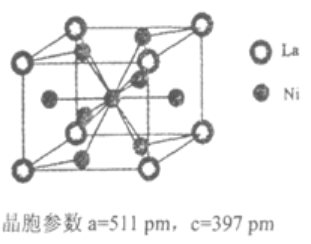

A.镧镍合金贮氢时的热化学方程式为:LaNi4(s)+3H2(g) LaNi4H6(s) ΔH=-31.77kJ/mol LaNi4H6(s) ΔH=-31.77kJ/mol |
| B.高压高温有利于氢气的贮氢 |
| C.可以利用镧镍合金良好的贮氢功能获取高纯度的氢气 |
| D.镧镍合金中氢的密度远大于标况下的氢,也大于液态氢,根据贮氢反应和镧镍合金的晶胞参数可以计算出合金中氢的密度约为0.111g/cm-3 |
您最近一年使用:0次
4 . 已知[Co(H2O)6]2+呈粉红色,[CoCl4]2-呈蓝色,[ZnCl4]2-为无色。现将CoCl2溶于水,加入浓盐酸后,溶液由粉红色变为蓝色,存在平衡:[Co(H2O)6]2++4Cl-⇌[CoCl4]2-+6H2O ΔH。用该溶液做实验,溶液的颜色变化如图:

| A.等物质的量的[Co(H2O)6]2+和[CoCl4]2-中σ键数之比为3:2 |
| B.由实验①可推知∆H>0 |
| C.实验②是由于c(H2O)增大,导致平衡逆向移动 |
| D.由实验③可知配离子的稳定性: [ZnCl4]2->[CoCl4]2- |
您最近一年使用:0次



