2023高三·全国·专题练习
1 . 萨巴蒂尔反应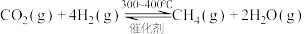 ,与水的电解联合使用是一种重要的载人航天器中氧气再生的方法。下列说法不正确的是
,与水的电解联合使用是一种重要的载人航天器中氧气再生的方法。下列说法不正确的是
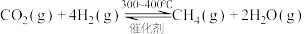 ,与水的电解联合使用是一种重要的载人航天器中氧气再生的方法。下列说法不正确的是
,与水的电解联合使用是一种重要的载人航天器中氧气再生的方法。下列说法不正确的是A.上述反应 >0 >0 |
B.增大 , , 的平衡转化率升高 的平衡转化率升高 |
C.上述反应平衡常数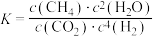 |
D.萨巴蒂尔反应产生的 可作航天器燃料 可作航天器燃料 |
您最近一年使用:0次
名校
2 . 某反应可有效降低汽车尾气污染物的排放,一定条件下该反应经历三个基元反应阶段,反应历程如图所示(TS表示过渡态)。下列说法正确的是


| A.三个基元反应中,反应②和反应③是放热反应 |
| B.该化学反应的速率主要由反应③决定 |
| C.增大压强,反应物的转化率降低 |
| D.温度过高可能导致催化剂失去活性,反应速率急剧下降,汽车尾气污染物增多 |
您最近一年使用:0次
名校
解题方法
3 . 已知: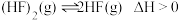 ,平衡体系的总质量m(总)与总物质的量n(总)之比在不同温度下随压强的变化曲线如图所示。下列说法正确的是
,平衡体系的总质量m(总)与总物质的量n(总)之比在不同温度下随压强的变化曲线如图所示。下列说法正确的是
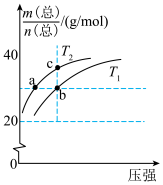
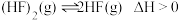 ,平衡体系的总质量m(总)与总物质的量n(总)之比在不同温度下随压强的变化曲线如图所示。下列说法正确的是
,平衡体系的总质量m(总)与总物质的量n(总)之比在不同温度下随压强的变化曲线如图所示。下列说法正确的是
A.温度: |
B.反应速率: |
C.平衡常数: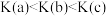 |
D.欲测定 的相对分子质量,宜在高温低压下进行 的相对分子质量,宜在高温低压下进行 |
您最近一年使用:0次
2023-05-04更新
|
681次组卷
|
3卷引用:【知识图鉴】单元讲练测选择性必修1第2单元02基础练
(已下线)【知识图鉴】单元讲练测选择性必修1第2单元02基础练海南省海口市海南中学,文昌中学,海口一中,嘉积中学2023届高三第一次模拟考试化学试题山东省青岛第一中学2023-2024学年高二上学期10月月考化学试题
名校
解题方法
4 . 研究NOx之间的转化对大气污染控制具有重要意义,已知:N2O4(g)⇌2NO2(g) ΔH>0。如图所示,在恒容密闭容器中,反应温度为T1时,c(N2O4)和c(NO2)随t变化为曲线Ⅰ、Ⅱ,改变温度到T2,c(NO2)随t变化为曲线Ⅲ,下列判断正确的是


| A.反应速率v(a)=v(b) |
| B.温度T1<T2 |
| C.升高温度,正向反应速率增加,逆向反应速率减小 |
| D.温度T1、T2下,反应分别达到平衡时,c(N2O4) 前者大 |
您最近一年使用:0次
2023-04-28更新
|
324次组卷
|
4卷引用:2023年高考山东卷化学真题变式题(不定项选择题)
(已下线)2023年高考山东卷化学真题变式题(不定项选择题)河南省实验中学2022-2023学年高一下学期期中考试化学试题江西省湖口中学2022-2023学年高一下学期5月期中考试化学试题江西省丰城中学2022-2023学年高一下学期期末考试化学试题
名校
5 . 反应
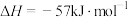 ,在温度为
,在温度为 、
、 时,平衡体系中
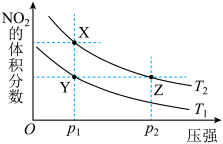
时,平衡体系中 的体积分数随压强变化的曲线如图所示。下列说法正确的是
的体积分数随压强变化的曲线如图所示。下列说法正确的是

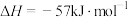 ,在温度为
,在温度为 、
、 时,平衡体系中
时,平衡体系中 的体积分数随压强变化的曲线如图所示。下列说法正确的是
的体积分数随压强变化的曲线如图所示。下列说法正确的是
A. | B.X、Y两点的反应速率:X>Y |
| C.X、Z两点气体的颜色:X比Z浅 | D.X、Z两点气体的平均相对分子质量:X>Z |
您最近一年使用:0次
2023-02-10更新
|
513次组卷
|
6卷引用:2019年高考江苏卷化学试题变式题(不定项选择题)
2023高三·全国·专题练习
6 . 已知反应:CH2=CHCH3(g)+Cl2(g)⇌CH2=CHCH2Cl(g)+HCl(g)。在一定压强下,按w=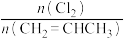 向密闭容器中充入氯气与丙烯。图甲表示平衡时,丙烯的体积分数(φ)与温度(T)、w的关系,图乙表示正、逆反应的平衡常数与温度的关系,则下列说法错误的是
向密闭容器中充入氯气与丙烯。图甲表示平衡时,丙烯的体积分数(φ)与温度(T)、w的关系,图乙表示正、逆反应的平衡常数与温度的关系,则下列说法错误的是

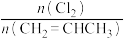 向密闭容器中充入氯气与丙烯。图甲表示平衡时,丙烯的体积分数(φ)与温度(T)、w的关系,图乙表示正、逆反应的平衡常数与温度的关系,则下列说法错误的是
向密闭容器中充入氯气与丙烯。图甲表示平衡时,丙烯的体积分数(φ)与温度(T)、w的关系,图乙表示正、逆反应的平衡常数与温度的关系,则下列说法错误的是
| A.图甲中,w2>1 |
| B.图乙中,A线表示正反应的平衡常数 |
| C.温度为T1、w=2时,Cl2的平衡转化率为50% |
| D.若在恒容绝热装置中进行上述反应,达到平衡时,装置内的气体压强将增大 |
您最近一年使用:0次
2023高三·全国·专题练习
解题方法
7 . 某研究小组,在某恒容密闭容器中,在不同温度(T1>T2)下进行储氢合金储氢过程的探究。平衡时,氢气的压强(p)与固相中氢原子与金属原子(M)的个数比[ ]的关系如图:
]的关系如图:

已知:①OA(或OA′)段:M(s)+ H2(g)
H2(g) MHx(s) △H1(I)
MHx(s) △H1(I)
②AB(或A′B′)段:zMHx(s)+H2(g) zMHy(s) △H2(II)
zMHy(s) △H2(II)
③在B或B′点,氢化反应结束,进一步增大氢气压强, 的值变化较小。下列说法正确的是
的值变化较小。下列说法正确的是
 ]的关系如图:
]的关系如图:
已知:①OA(或OA′)段:M(s)+
 H2(g)
H2(g) MHx(s) △H1(I)
MHx(s) △H1(I)②AB(或A′B′)段:zMHx(s)+H2(g)
 zMHy(s) △H2(II)
zMHy(s) △H2(II)③在B或B′点,氢化反应结束,进一步增大氢气压强,
 的值变化较小。下列说法正确的是
的值变化较小。下列说法正确的是| A.反应I、II均为△S>0的反应 |
| B.平衡常数:K(c)<K(a)=K(b) |
| C.该储氢合金可通过升温或减压的方式释放H2 |
| D.由a点移到d点,需在恒温恒容条件下通入少量氢气 |
您最近一年使用:0次
2023高三·全国·专题练习
名校
解题方法
8 . 乙烯气相直接水合反应制备乙醇:C2H4(g)+H2O(g) ⇌C2H5OH(g)。乙烯的平衡转化率随温度、压强的变化关系如图[起始时,n(H2O)=n(C2H4)=1mol,容器体积为1L]。下列分析不正确的是
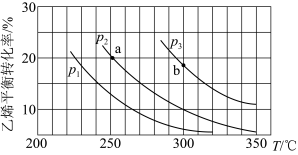

| A.乙烯气相直接水合反应的ΔH>0 |
| B.图中压强的大小关系为p1>p2>p3 |
C.图中a点对应的平衡常数的数值K= |
| D.达到平衡状态a、b所需要的时间:a>b |
您最近一年使用:0次
名校
9 . 将1mol M和2mol N置于体积为2L的恒容密闭容器中,发生反应:
 。反应过程中测得Q的体积分数在不同温度下随时间的变化如图所示。下列结论正确的是
。反应过程中测得Q的体积分数在不同温度下随时间的变化如图所示。下列结论正确的是


 。反应过程中测得Q的体积分数在不同温度下随时间的变化如图所示。下列结论正确的是
。反应过程中测得Q的体积分数在不同温度下随时间的变化如图所示。下列结论正确的是
A. |
B.温度: |
C.温度为 时,M的平衡转化率为50% 时,M的平衡转化率为50% |
D.若X、Y两点的平衡常数分别为 、 、 ,则 ,则 |
您最近一年使用:0次
2023-01-15更新
|
177次组卷
|
3卷引用:2019年高考江苏卷化学试题变式题(不定项选择题)
(已下线)2019年高考江苏卷化学试题变式题(不定项选择题)山东省菏泽市鄄城县第一中学2022-2023学年高二上学期期末考试化学试题山东省鄄城县第一中学2023-2024学年高二上学期9月月考化学试题
名校
10 . CO2催化加氢合成甲醇是重要的碳捕获利用与封存技术,该过程主要发生下列反应:
反应①:
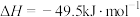
反应②:
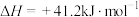
在0.5MPa条件下,将n(CO2):n(H2)为1:3的混合气体以一定流速通过装有催化剂的反应器,实验测得CO2的转化率、CH3OH的选择性 与温度的关系如图所示。下列说法错误的是
与温度的关系如图所示。下列说法错误的是

反应①:

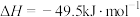
反应②:

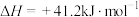
在0.5MPa条件下,将n(CO2):n(H2)为1:3的混合气体以一定流速通过装有催化剂的反应器,实验测得CO2的转化率、CH3OH的选择性
 与温度的关系如图所示。下列说法错误的是
与温度的关系如图所示。下列说法错误的是
| A.升高温度时,CO的选择性增大 |
| B.一定温度下,增大起始n(CO2):n(H2)的比值,可提高CO2的平衡转化率 |
C.其他条件不变,在280~400℃,产物中 随温度的升高而减小 随温度的升高而减小 |
| D.为高效生产CH3OH,需研发低温下CO2转化率高和CH3OH选择性高的催化剂 |
您最近一年使用:0次



