某些稀土合金晶体结构中,原子排列十分紧密,具有良好的贮氢功能,常用作贮氢材料。目前,贮氢合金中最具有代表性的是镧镍-合金(LaxNiy),其结构如图,已知在200-300kPa的压强下,1mol合金最多能吸收3mol氢气同时放出31.77kJ的能量。下列说法正确的是
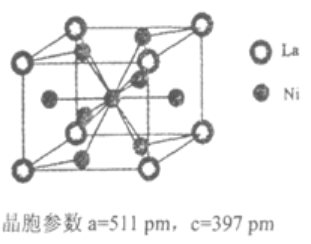

A.镧镍合金贮氢时的热化学方程式为:LaNi4(s)+3H2(g) LaNi4H6(s) ΔH=-31.77kJ/mol LaNi4H6(s) ΔH=-31.77kJ/mol |
| B.高压高温有利于氢气的贮氢 |
| C.可以利用镧镍合金良好的贮氢功能获取高纯度的氢气 |
| D.镧镍合金中氢的密度远大于标况下的氢,也大于液态氢,根据贮氢反应和镧镍合金的晶胞参数可以计算出合金中氢的密度约为0.111g/cm-3 |
2012高二·浙江·竞赛 查看更多[1]
更新时间:2021-08-02 21:59:38
|
相似题推荐
多选题
|
适中
(0.65)
【推荐1】铁触媒催化合成氨的反应历程如图所示,其中吸附在催化剂表面的物质用“ad”表示,下列说法正确的是
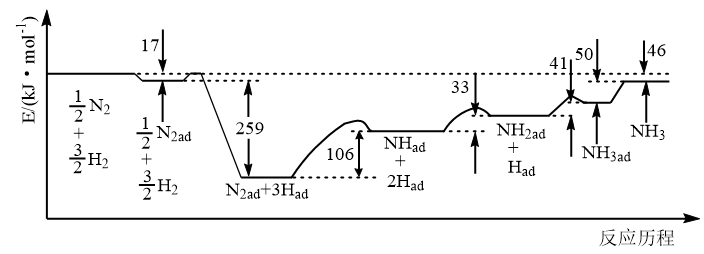

| A.“吸附”过程吸热,“脱附”过程放热 |
B.合成氨反应 的 的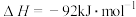 |
| C.降温或加压可以增大反应速率 |
D.该历程中反应速率最慢的过程为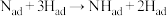 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐2】我国科学家研究化合物M(s)催化CO2氢化机理。由化合物M(s)生成化合物N(s)过程的机理和相对能量曲线如图所示(已知1eV=1.6×10−19J)。TS1、TS2均为过渡态。下列说法错误的是
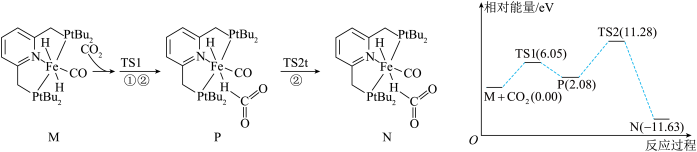

| A.过渡态TS1比TS2更稳定 |
| B.过程P→TS2为化合物M生成化合物N的决速步骤 |
| C.化合物M催化CO2氢化反应过程中一定有Fe−O键的断裂 |
| D.该过程的热化学方程式为:M(s)+CO2(g)=N(s) ΔH=−11.63 kJ·mol −1 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐1】在恒压、 和
和 的起始浓度一定的条件下,催化反应相同时间,测得不同温度下
的起始浓度一定的条件下,催化反应相同时间,测得不同温度下 转化为
转化为 的转化率如图中实线所示(图中虚线表示相同条件下
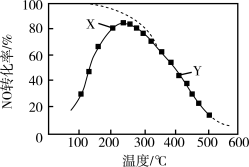
的转化率如图中实线所示(图中虚线表示相同条件下 的平衡转化率随温度的变化)。下列说法正确的是
的平衡转化率随温度的变化)。下列说法正确的是
 和
和 的起始浓度一定的条件下,催化反应相同时间,测得不同温度下
的起始浓度一定的条件下,催化反应相同时间,测得不同温度下 转化为
转化为 的转化率如图中实线所示(图中虚线表示相同条件下
的转化率如图中实线所示(图中虚线表示相同条件下 的平衡转化率随温度的变化)。下列说法正确的是
的平衡转化率随温度的变化)。下列说法正确的是
A.图中X点所示条件下,延长反应时间能提高 转化率 转化率 |
B.反应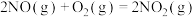 的 的 |
C.图中Y点所示条件下,增加 的浓度不能提高 的浓度不能提高 转化率 转化率 |
| D.X点的化学平衡常数大于Y点的化学平衡常数 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐2】氮氧化物(NOx)作为大气中重要污染物之一,其消除已成为环保领域中的研究热点。利用催化剂ZAg对NO催化转化的反应过程与能量变化如图1,在ZAg催化剂表面转化过程如图2。
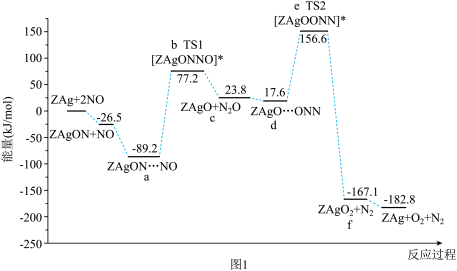

下列说法错误的是


下列说法错误的是
| A.高温下有利于反应过程中NO的转化 | B.由a释放N2O的过程为控速步骤 |
| C.a到b、d到e,都有非极性共价键的生成 | D.过渡态d比a稳定 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐3】温度为T时,向2.0L恒容密闭容器中充入1.0mol  ,反应
,反应 经过一段时间后达到平衡。反应过程中测定的部分数据见下表,下列说法正确的是
经过一段时间后达到平衡。反应过程中测定的部分数据见下表,下列说法正确的是
 ,反应
,反应 经过一段时间后达到平衡。反应过程中测定的部分数据见下表,下列说法正确的是
经过一段时间后达到平衡。反应过程中测定的部分数据见下表,下列说法正确的是t/s | 0 | 50 | 150 | 250 | 350 |
| 0 | 0.16 | 0.19 | 0.20 | 0.20 |
A.反应在前50s的平均速率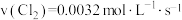 |
B.保持其他条件不变,升高温度,平衡时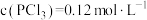 ,则反应的ΔH>0 ,则反应的ΔH>0 |
C.相同温度下,起始时向容器中充入1.80mol  、0.20mol 、0.20mol  和0.20mol 和0.20mol  ,反应达到平衡前v(正)>v(逆) ,反应达到平衡前v(正)>v(逆) |
D.平衡后,减小压强不利于提高 的平衡转化率 的平衡转化率 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐1】铁镁合金是目前已发现的储氢密度较高的储氢材料之一,其晶胞结构如图所示(黑球代表Fe,白球代表Mg)。则下列说法正确的是
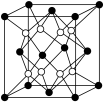

| A.铁镁合金的化学式可表示为Fe2Mg |
| B.晶胞中有4个铁原子 |
| C.晶体中存在的化学键类型为离子键 |
D.该晶胞的质量是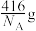 ( ( 表示阿伏加德罗常数的值) 表示阿伏加德罗常数的值) |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐2】作为第三代半导体材料的砷化镓(GaAs)可由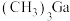 和
和 反应制得,发生反应的化学方程式为
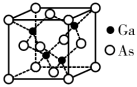
反应制得,发生反应的化学方程式为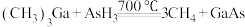 ,GaAs的晶胞单元如图所示(设晶胞边长为a pm,阿伏加德罗常数的值为
,GaAs的晶胞单元如图所示(设晶胞边长为a pm,阿伏加德罗常数的值为 ),关于该反应中涉及的物质,下列说法错误的是
),关于该反应中涉及的物质,下列说法错误的是
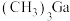 和
和 反应制得,发生反应的化学方程式为
反应制得,发生反应的化学方程式为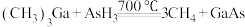 ,GaAs的晶胞单元如图所示(设晶胞边长为a pm,阿伏加德罗常数的值为
,GaAs的晶胞单元如图所示(设晶胞边长为a pm,阿伏加德罗常数的值为 ),关于该反应中涉及的物质,下列说法错误的是
),关于该反应中涉及的物质,下列说法错误的是
A. 的沸点低于 的沸点低于 的 的 |
| B.甲烷形成的晶体是分子晶体 |
C.GaAs的晶胞密度为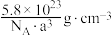 |
D.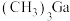 中Ga位于由C组成的平面三角形中心 中Ga位于由C组成的平面三角形中心 |
您最近一年使用:0次


 ,则
,则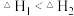

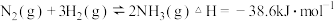
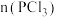 /mol
/mol