解题方法
1 . 在一定条件下,一定量的X在恒容密闭容器中发生反应: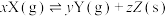
 ,达到平衡时,Y的浓度与温度和容器容积的关系如图所示,下列判断正确的是
,达到平衡时,Y的浓度与温度和容器容积的关系如图所示,下列判断正确的是
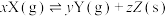
 ,达到平衡时,Y的浓度与温度和容器容积的关系如图所示,下列判断正确的是
,达到平衡时,Y的浓度与温度和容器容积的关系如图所示,下列判断正确的是
A. |
B. |
| C.在M点,投入适量Z,逆反应速率增大 |
| D.在M点,增大X的浓度,X的平衡质量分数增大 |
您最近一年使用:0次
2022·四川雅安·三模
名校
2 . 气态含氮化合物及相关反应是新型科研热点。
I.工业上主要采用氨催化氧化法生产NO:
主反应: 4NH3(g)+5O2(g) 4NO(g)+6H2O(g ) △H1
4NO(g)+6H2O(g ) △H1
副反应: 4NH3(g)+3O2(g) 2N2(g)+6H2O(g) △H2=- 1265kJ·mol-1
2N2(g)+6H2O(g) △H2=- 1265kJ·mol-1
(1)王金兰课题组提出合成氨的“表面氢化机理”如图,在较低的电压下实现氮气还原合成氨。“N2+ 2*H=中间体”是氮气还原合成氨的决速步,“中间体”为___________ (写化学式)。
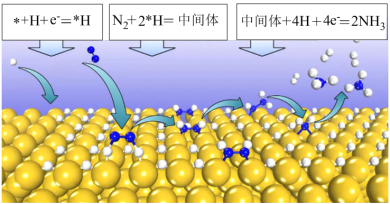
(2)已知N2(g)+O2(g)= 2NO(g) △H =+180kJ·mol-1,则△H1=___________ kJ·mol -1。
(3)制备NO时,在某种氨的初始含量下,温度升高一段时间后,体系中 减小,可能的原因是
减小,可能的原因是___________ 。
II.已知工业上常利用NO和Cl2反应来制备有机合成中的重要试剂亚硝酰氯(NOC1),化学方程式为2NO(g)+Cl2(g) 2NOCl(g) △H <0。
2NOCl(g) △H <0。
(4)保持恒温恒容条件,将物质的量之和为3mol的NO和Cl2以不同的氮氯比 进行反应,平衡时某反应物的转化率和氮氯比及不同温度的关系如图所示:
进行反应,平衡时某反应物的转化率和氮氯比及不同温度的关系如图所示:
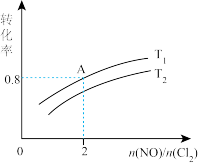
①图中T1、T2的关系为T1___________ T2(填“<”或“=”)
②体系的初始压强为P0,则A点的平衡常数Kp=___________ ; (以分压表示,分压=总压×物质的量分数)
III. NOx是空气污染物之一,用焦炭还原NO2的反应为: 2NO2(g)+2C(s) N2(g)+2CO2(g) △H >0. T°C时,向容积不等的恒容密闭容器中分别加入足量活性炭和1mol NO2,经t min,测得各容器中NO2的转化率与容器容积的关系如图所示。
N2(g)+2CO2(g) △H >0. T°C时,向容积不等的恒容密闭容器中分别加入足量活性炭和1mol NO2,经t min,测得各容器中NO2的转化率与容器容积的关系如图所示。
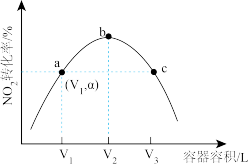
(5)①提高NO2平衡转化率可采取的措施是_____ (答出两种即可)。
②a点对应的容器,t min内v(NO2)=___________ (用含字母的代数式表示)。
③a、b、c三点中,已达平衡状态的有___________ 。
I.工业上主要采用氨催化氧化法生产NO:
主反应: 4NH3(g)+5O2(g)
 4NO(g)+6H2O(g ) △H1
4NO(g)+6H2O(g ) △H1副反应: 4NH3(g)+3O2(g)
 2N2(g)+6H2O(g) △H2=- 1265kJ·mol-1
2N2(g)+6H2O(g) △H2=- 1265kJ·mol-1(1)王金兰课题组提出合成氨的“表面氢化机理”如图,在较低的电压下实现氮气还原合成氨。“N2+ 2*H=中间体”是氮气还原合成氨的决速步,“中间体”为

(2)已知N2(g)+O2(g)= 2NO(g) △H =+180kJ·mol-1,则△H1=
(3)制备NO时,在某种氨的初始含量下,温度升高一段时间后,体系中
 减小,可能的原因是
减小,可能的原因是II.已知工业上常利用NO和Cl2反应来制备有机合成中的重要试剂亚硝酰氯(NOC1),化学方程式为2NO(g)+Cl2(g)
 2NOCl(g) △H <0。
2NOCl(g) △H <0。(4)保持恒温恒容条件,将物质的量之和为3mol的NO和Cl2以不同的氮氯比
 进行反应,平衡时某反应物的转化率和氮氯比及不同温度的关系如图所示:
进行反应,平衡时某反应物的转化率和氮氯比及不同温度的关系如图所示:
①图中T1、T2的关系为T1
②体系的初始压强为P0,则A点的平衡常数Kp=
III. NOx是空气污染物之一,用焦炭还原NO2的反应为: 2NO2(g)+2C(s)
 N2(g)+2CO2(g) △H >0. T°C时,向容积不等的恒容密闭容器中分别加入足量活性炭和1mol NO2,经t min,测得各容器中NO2的转化率与容器容积的关系如图所示。
N2(g)+2CO2(g) △H >0. T°C时,向容积不等的恒容密闭容器中分别加入足量活性炭和1mol NO2,经t min,测得各容器中NO2的转化率与容器容积的关系如图所示。
(5)①提高NO2平衡转化率可采取的措施是
②a点对应的容器,t min内v(NO2)=
③a、b、c三点中,已达平衡状态的有
您最近一年使用:0次
2022-06-27更新
|
617次组卷
|
3卷引用:2022年海南省高考真题变式题15-19
3 . 在一定温度下,向某密闭容器中充入2 mol A和1 mol B发生如下反应,2A(g)+B(g) 3C(g)+D(s) △H<0,T℃时反应达到平衡,此时C的百分含量如图中实线所示,若要使图中实线变为虚线,则改变的条件为
3C(g)+D(s) △H<0,T℃时反应达到平衡,此时C的百分含量如图中实线所示,若要使图中实线变为虚线,则改变的条件为

 3C(g)+D(s) △H<0,T℃时反应达到平衡,此时C的百分含量如图中实线所示,若要使图中实线变为虚线,则改变的条件为
3C(g)+D(s) △H<0,T℃时反应达到平衡,此时C的百分含量如图中实线所示,若要使图中实线变为虚线,则改变的条件为
| A.升高温度 | B.增大压强 | C.使用适当催化剂 | D.移走容器中的D |
您最近一年使用:0次
2020-10-31更新
|
148次组卷
|
2卷引用:海南省万宁市北京师范大学万宁附属中学2021届高三上学期第三次月考化学试题



