名校
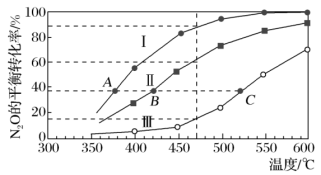
1 . 现有反应2N2O(g) 2N2(g)+O2(g),在四个恒容密闭容器中按下表充入气体进行反应,容器Ⅰ、Ⅱ、Ⅲ中N2O的平衡转化率如图所示。下列说法正确的是
2N2(g)+O2(g),在四个恒容密闭容器中按下表充入气体进行反应,容器Ⅰ、Ⅱ、Ⅲ中N2O的平衡转化率如图所示。下列说法正确的是
 2N2(g)+O2(g),在四个恒容密闭容器中按下表充入气体进行反应,容器Ⅰ、Ⅱ、Ⅲ中N2O的平衡转化率如图所示。下列说法正确的是
2N2(g)+O2(g),在四个恒容密闭容器中按下表充入气体进行反应,容器Ⅰ、Ⅱ、Ⅲ中N2O的平衡转化率如图所示。下列说法正确的是| 容器 | 容积/L | 起始物质的量/mol | ||
| N2O | N2 | O2 | ||
| Ⅰ | V1 | 0.1 | 0 | 0 |
| Ⅱ | 1.0 | 0.1 | 0 | 0 |
| Ⅲ | V3 | 0.1 | 0 | 0 |
| Ⅳ | 1.0 | 0.06 | 0.06 | 0.04 |

| A.该反应的正反应放热 |
| B.相同温度下,起始反应速率:v(Ⅰ)>v(Ⅱ) |
| C.图中A、B、C三点处,三个容器内的压强:pA(Ⅰ)<pB(Ⅱ)<pC(Ⅲ) |
| D.若Ⅳ在470℃进行反应,反应逆向进行 |
您最近一年使用:0次
2024-02-03更新
|
138次组卷
|
2卷引用:湖南省衡阳市第八中学2024届高三模拟预测信息卷(一)化学试题
名校
解题方法
2 . 下列实验装置或操作能达到实验目的的是
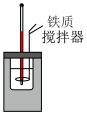 | 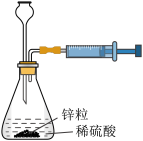 |
| A.测定中和反应的反应热 | B.测定锌与稀硫酸反应的反应速率 |
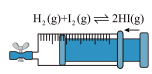 | 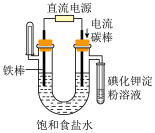 |
| C.探究压强对平衡的影响 | D.验证NaCl溶液(含酚酞)电解产物 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-11-11更新
|
326次组卷
|
3卷引用:湖南省衡阳市第八中学2024届高三模拟预测信息卷(一)化学试题
3 . 已知 催化加氢合成乙醇的反应原理为
催化加氢合成乙醇的反应原理为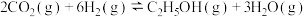 。设
。设 为起始时的投料比,即
为起始时的投料比,即 。
。 的平衡转化率与压强、温度和投料比的关系如图所示,下列有关说法错误的是
的平衡转化率与压强、温度和投料比的关系如图所示,下列有关说法错误的是

 催化加氢合成乙醇的反应原理为
催化加氢合成乙醇的反应原理为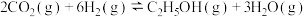 。设
。设 为起始时的投料比,即
为起始时的投料比,即 。
。 的平衡转化率与压强、温度和投料比的关系如图所示,下列有关说法错误的是
的平衡转化率与压强、温度和投料比的关系如图所示,下列有关说法错误的是
A.图1中投料比相同,温度从高到低的顺序为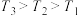 |
B.图2中投料比由大到小的顺序为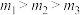 |
C.若图1中投料比 ,a点时乙醇的分压为 ,a点时乙醇的分压为 |
D.若图2中投料比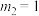 ,随着温度的升高,该平衡体系中 ,随着温度的升高,该平衡体系中 的百分含量逐渐减小 的百分含量逐渐减小 |
您最近一年使用:0次
名校
解题方法
4 . 在1 L的密闭容器中充入2 mol N2和7 mol H2,发生反应 ,保持其他条件不变,相同时间内测得NH3的浓度与温度的关系如图所示。下列叙述错误的是
,保持其他条件不变,相同时间内测得NH3的浓度与温度的关系如图所示。下列叙述错误的是

 ,保持其他条件不变,相同时间内测得NH3的浓度与温度的关系如图所示。下列叙述错误的是
,保持其他条件不变,相同时间内测得NH3的浓度与温度的关系如图所示。下列叙述错误的是 
| A.该反应是放热反应 |
| B.温度为T1 K时,再加入1 mol N2和1 mol NH3,平衡向正反应方向移动 |
| C.温度为T1 K时,N2的平衡转化率为50% |
| D.a、c两点对应的压强:Pa<Pc |
您最近一年使用:0次
2022-05-12更新
|
187次组卷
|
2卷引用:湖南省常宁市第一中学2022届高三下学期第三次模拟考试化学试题
5 . 在一定条件下,反应A2+ B2 2AB △H=QkJ/mol的反应时间与生成物AB的质量分数(AB%)的关系如图所示,其中a、b为不同温度时的反应曲线(其他条件不变),c为在t3时刻开始缩小容器容积(温度不变)的变化曲线。下列有关说法正确的是
2AB △H=QkJ/mol的反应时间与生成物AB的质量分数(AB%)的关系如图所示,其中a、b为不同温度时的反应曲线(其他条件不变),c为在t3时刻开始缩小容器容积(温度不变)的变化曲线。下列有关说法正确的是
 2AB △H=QkJ/mol的反应时间与生成物AB的质量分数(AB%)的关系如图所示,其中a、b为不同温度时的反应曲线(其他条件不变),c为在t3时刻开始缩小容器容积(温度不变)的变化曲线。下列有关说法正确的是
2AB △H=QkJ/mol的反应时间与生成物AB的质量分数(AB%)的关系如图所示,其中a、b为不同温度时的反应曲线(其他条件不变),c为在t3时刻开始缩小容器容积(温度不变)的变化曲线。下列有关说法正确的是 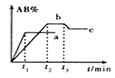
| A.△H>0 | B.AB一定是气体物质 |
| C.反应温度a低于b | D.A2、B2中最少有一种是气态物质 |
您最近一年使用:0次



