解题方法
1 . 反应:aA(g)+bB(g) 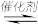 cC(g)在恒温恒容条件下进行,各物质的浓度随时间变化的曲线如图所示。
cC(g)在恒温恒容条件下进行,各物质的浓度随时间变化的曲线如图所示。
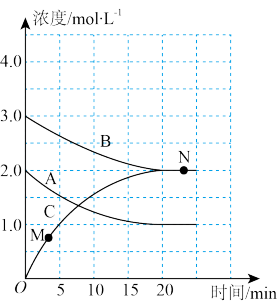
(1)该反应的化学方程式中,a:b:c为________ 。
(2)反应从起始至20min内,A的平均反应速率v (A)=_________ 。平衡时B的体积分数为_______ 。
(3)判断该反应是否达到平衡的依据为______ (填字母)。
A 压强不随时间改变
B A的物质的量分数不随时间改变
C 气体的密度不随时间改变
D 单位时间内消耗A和B的物质的量相等
(4)下列措施能增大反应速率的是______ (填字母)。
A 升高温度 B 降低压强 C 减小C的浓度 D 加入合适的催化剂
(5)N点的正反应速率v正(C)________ (填“大于”“小于”或“等于”)M点的逆反应速率v逆(C)。
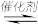 cC(g)在恒温恒容条件下进行,各物质的浓度随时间变化的曲线如图所示。
cC(g)在恒温恒容条件下进行,各物质的浓度随时间变化的曲线如图所示。
(1)该反应的化学方程式中,a:b:c为
(2)反应从起始至20min内,A的平均反应速率v (A)=
(3)判断该反应是否达到平衡的依据为
A 压强不随时间改变
B A的物质的量分数不随时间改变
C 气体的密度不随时间改变
D 单位时间内消耗A和B的物质的量相等
(4)下列措施能增大反应速率的是
A 升高温度 B 降低压强 C 减小C的浓度 D 加入合适的催化剂
(5)N点的正反应速率v正(C)
您最近一年使用:0次
2020-09-07更新
|
153次组卷
|
2卷引用:湖北省荆门市2019-2020学年高一下学期期末考试化学试题
名校
2 . 1,2-二氯丙烷(CH2ClCHClCH3)是重要的化工原料,工业上可用丙烯加成法生产,主要副产物为3-氯丙烯(CH2=CHCH2C1) ,反应原理为
i. CH2=CHCH3(g)+Cl2(g) CH2ClCHClCH3(g) ΔH1= -134 kJ• mol-1
CH2ClCHClCH3(g) ΔH1= -134 kJ• mol-1
ii. CH2=CHCH3(g)+Cl2(g) CH2=CHCH2Cl (g)+HCl(g) ΔH2= -l02 kJ • mol-1
CH2=CHCH2Cl (g)+HCl(g) ΔH2= -l02 kJ • mol-1
已知:相关化学键的键能数据如下表所示:
请回答下列问题:
(1)由反应i计算出表中x=_____________ 。
(2)一定温度下,密闭容器中发生反应i和反应ii,达到平衡后增大压强,CH2C1CHClCH3的产率____________ (填“增大”“减小”或“不变”)。
(3)T1℃时,向10L恒容的密闭容器中充入1 mol CH2=CHCH2C1和2 mol HCl,只发生以下反应:CH2=CH CH2Cl (g)+HCl(g) CH2ClCHClCH3(g) ΔH3。5min反应达到平衡,测得 0〜5 min内,用CH2ClCHClCH3表示的反应速率 v(CH2ClCHClCH3)=0.016 mol·L-1• min-1。
CH2ClCHClCH3(g) ΔH3。5min反应达到平衡,测得 0〜5 min内,用CH2ClCHClCH3表示的反应速率 v(CH2ClCHClCH3)=0.016 mol·L-1• min-1。
①平衡时,HCl的体积分数为__________________ (保留三位有效数字)。
②保持其它条件不变,6 min时再向该容器中充入0. 6 mol CH2=CHCH2Cl、0.2molHCl和0.1mol CH2ClCHClCH3,则起始反应速率 v正(HCl)______________ (填“>”“<”或“=”)V逆(HCl).
(4)一定压强下,向密闭容器中充入一定量的CH2=CHCH3和C12发生反应ii。设起始的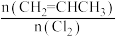 =w,平衡时Cl2的体积分数(φ)与温度(T)、w的关系如图甲所示。W=1时,正、逆反应的平衡常数(K)与温度(T)的关系如图乙所示。
=w,平衡时Cl2的体积分数(φ)与温度(T)、w的关系如图甲所示。W=1时,正、逆反应的平衡常数(K)与温度(T)的关系如图乙所示。
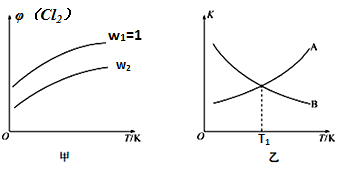
①图甲中,w2__________ (填“>”“<”或“=”)1
②图乙中,表示正反应平衡常数的曲线为________ (填“A”或“B”),理由为________________ 。
③T1K下,平衡时Cl2的转化率为_______________ 。
(5)起始时向某恒容绝热容器中充入1 mol CH2=CHCH3和1 mol Cl2发生反应ii,达到平衡时,容器内气体压强_________________ (填“增大”“减小”或“不变”)。
i. CH2=CHCH3(g)+Cl2(g)
 CH2ClCHClCH3(g) ΔH1= -134 kJ• mol-1
CH2ClCHClCH3(g) ΔH1= -134 kJ• mol-1ii. CH2=CHCH3(g)+Cl2(g)
 CH2=CHCH2Cl (g)+HCl(g) ΔH2= -l02 kJ • mol-1
CH2=CHCH2Cl (g)+HCl(g) ΔH2= -l02 kJ • mol-1已知:相关化学键的键能数据如下表所示:
| 化学键 | C=C | C—C | C—Cl | Cl—Cl |
| E/( kJ • mol-1) | 611 | X | 328 | 243 |
(1)由反应i计算出表中x=
(2)一定温度下,密闭容器中发生反应i和反应ii,达到平衡后增大压强,CH2C1CHClCH3的产率
(3)T1℃时,向10L恒容的密闭容器中充入1 mol CH2=CHCH2C1和2 mol HCl,只发生以下反应:CH2=CH CH2Cl (g)+HCl(g)
 CH2ClCHClCH3(g) ΔH3。5min反应达到平衡,测得 0〜5 min内,用CH2ClCHClCH3表示的反应速率 v(CH2ClCHClCH3)=0.016 mol·L-1• min-1。
CH2ClCHClCH3(g) ΔH3。5min反应达到平衡,测得 0〜5 min内,用CH2ClCHClCH3表示的反应速率 v(CH2ClCHClCH3)=0.016 mol·L-1• min-1。①平衡时,HCl的体积分数为
②保持其它条件不变,6 min时再向该容器中充入0. 6 mol CH2=CHCH2Cl、0.2molHCl和0.1mol CH2ClCHClCH3,则起始反应速率 v正(HCl)
(4)一定压强下,向密闭容器中充入一定量的CH2=CHCH3和C12发生反应ii。设起始的
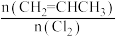 =w,平衡时Cl2的体积分数(φ)与温度(T)、w的关系如图甲所示。W=1时,正、逆反应的平衡常数(K)与温度(T)的关系如图乙所示。
=w,平衡时Cl2的体积分数(φ)与温度(T)、w的关系如图甲所示。W=1时,正、逆反应的平衡常数(K)与温度(T)的关系如图乙所示。
①图甲中,w2
②图乙中,表示正反应平衡常数的曲线为
③T1K下,平衡时Cl2的转化率为
(5)起始时向某恒容绝热容器中充入1 mol CH2=CHCH3和1 mol Cl2发生反应ii,达到平衡时,容器内气体压强
您最近一年使用:0次



