名校
解题方法
1 . 根据要求,回答下列问题:
(1)某温度下,纯水中的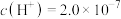 mol·L
mol·L ,则该温度时的水的离子积
,则该温度时的水的离子积
_______ ;保持温度不变,滴入稀盐酸使溶液中的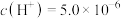 mol·L
mol·L ,则溶液中的
,则溶液中的 为
为_______ mol·L ;
;
(2)将浓度均为0.1 mo/L的 和
和 等体积混合,溶液
等体积混合,溶液 。分析该溶液中离子浓度从大到小依次是:
。分析该溶液中离子浓度从大到小依次是:_______ ;
(3)将 溶液蒸干、灼烧,最后所得的固体的主要成份是
溶液蒸干、灼烧,最后所得的固体的主要成份是_______ ;
(4)物质的量浓度相同的三种盐NaX、NaY、NaZ的溶液,其pH依次为8、9、10,则HX、HY、HZ的酸性由强到弱的顺序是_______ ;
(5)已知:a. ,
, ,
,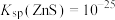 ,
,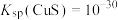
b.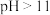 时,
时, 会转化为
会转化为
c.离子浓度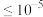 mol/L,即认为其完全沉淀
mol/L,即认为其完全沉淀
①若加入 来沉淀
来沉淀 和
和 ,当溶液中ZnS和CuS共存时,
,当溶液中ZnS和CuS共存时,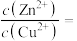
_______ 。
②若加入NaOH溶液来调节pH,使 和
和 完全沉淀,pH应满足的条件为
完全沉淀,pH应满足的条件为_______ 。
(1)某温度下,纯水中的
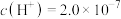 mol·L
mol·L ,则该温度时的水的离子积
,则该温度时的水的离子积
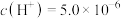 mol·L
mol·L ,则溶液中的
,则溶液中的 为
为 ;
;(2)将浓度均为0.1 mo/L的
 和
和 等体积混合,溶液
等体积混合,溶液 。分析该溶液中离子浓度从大到小依次是:
。分析该溶液中离子浓度从大到小依次是:(3)将
 溶液蒸干、灼烧,最后所得的固体的主要成份是
溶液蒸干、灼烧,最后所得的固体的主要成份是(4)物质的量浓度相同的三种盐NaX、NaY、NaZ的溶液,其pH依次为8、9、10,则HX、HY、HZ的酸性由强到弱的顺序是
(5)已知:a.
 ,
, ,
,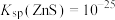 ,
,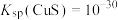
b.
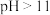 时,
时, 会转化为
会转化为
c.离子浓度
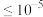 mol/L,即认为其完全沉淀
mol/L,即认为其完全沉淀①若加入
 来沉淀
来沉淀 和
和 ,当溶液中ZnS和CuS共存时,
,当溶液中ZnS和CuS共存时,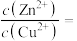
②若加入NaOH溶液来调节pH,使
 和
和 完全沉淀,pH应满足的条件为
完全沉淀,pH应满足的条件为
您最近一年使用:0次
2 . 物质在水中可能存在电离平衡、水解平衡和沉淀溶解平衡。请回答下列问题:
(1)碳酸钠俗称___________ ,可作为碱使用的原因是___________ (用离子方程式表示)。
(2)为抑制水解,实验室中配制FeCl3溶液时常加入___________ (填名称)。将FeCl3溶液和NaHCO3溶液混合,产生红褐色沉淀和无色气体,反应的离子方程式为___________ 。
(3)25℃时,pH均为5的醋酸和硫酸铝两种溶液中,由水电离出的c(H+)之比为___________ 。
(4)25℃时,Ksp(AgCl)=1.8×10-10.现将足量氯化银固体放入100 mL 0.2 mol/L AgNO3溶液中,则溶液中氯离子的浓度为___________ mol·L-1(忽略溶液体积的变化)。
(5)某温度时,Ksp(BaCO3)=2.6×10−9,Ksp(BaSO4)=1.1×10−10.在该温度下,向含有BaSO4固体的溶液中滴加Na2CO3溶液,当有BaCO3沉淀生成时溶液中 =
=___________ (保留三位有效数字)。
(1)碳酸钠俗称
(2)为抑制水解,实验室中配制FeCl3溶液时常加入
(3)25℃时,pH均为5的醋酸和硫酸铝两种溶液中,由水电离出的c(H+)之比为
(4)25℃时,Ksp(AgCl)=1.8×10-10.现将足量氯化银固体放入100 mL 0.2 mol/L AgNO3溶液中,则溶液中氯离子的浓度为
(5)某温度时,Ksp(BaCO3)=2.6×10−9,Ksp(BaSO4)=1.1×10−10.在该温度下,向含有BaSO4固体的溶液中滴加Na2CO3溶液,当有BaCO3沉淀生成时溶液中
 =
=
您最近一年使用:0次
3 . 某溶液中含有Ba2+和Sr2+,它们的浓度均为0.010mol/L,向其中滴加Na2CrO4溶液,请通过计算说明下列问题,已知Ksp[BaCrO4]=1.2×10-10;Ksp[SrCrO4]=2.2 ×10-5,)
(1)当溶液中Ba2+开始沉淀,溶液中CrO 的浓度为多少?
的浓度为多少?
(2)当溶液中Ba2+沉淀完全时,Sr2+是否开始沉淀?
(1)当溶液中Ba2+开始沉淀,溶液中CrO
 的浓度为多少?
的浓度为多少?(2)当溶液中Ba2+沉淀完全时,Sr2+是否开始沉淀?
您最近一年使用:0次
4 . 已知25℃时,Ksp(Mg(OH)2)=1.8×10-11,Ksp(Cu(OH)2)=2.2×10-20。请按要求回答下列问题:
(1)在25℃下,向浓度均为0.1 mol・L-1的MgCl2和CuCl2混合溶液中逐滴加入氨水,先生成____________沉淀(填化学式),生成该沉淀的离子方程式为________________。
(2)25℃时,向0.01 mol・L-1的MgCl2溶液中,逐滴加入浓NaOH溶液,当Mg2+完全沉淀时,溶液的pH为_______________(忽略溶液体积变化,已知lg1.8=0.26)。
(3)已知25℃时,Ksp(Fe(OH)3)=2.79×10-39,试求该温度下反应Fe(OH)3+3H+ Fe3++3H2O的平衡常数K,写出计算推理过程。
Fe3++3H2O的平衡常数K,写出计算推理过程。
(1)在25℃下,向浓度均为0.1 mol・L-1的MgCl2和CuCl2混合溶液中逐滴加入氨水,先生成____________沉淀(填化学式),生成该沉淀的离子方程式为________________。
(2)25℃时,向0.01 mol・L-1的MgCl2溶液中,逐滴加入浓NaOH溶液,当Mg2+完全沉淀时,溶液的pH为_______________(忽略溶液体积变化,已知lg1.8=0.26)。
(3)已知25℃时,Ksp(Fe(OH)3)=2.79×10-39,试求该温度下反应Fe(OH)3+3H+
 Fe3++3H2O的平衡常数K,写出计算推理过程。
Fe3++3H2O的平衡常数K,写出计算推理过程。
您最近一年使用:0次



