1 . (1)下列物质中,物质的量最大的是___________ (填序号,下同),含分子个数最多的是___________ ,含原子个数最多的是___________ ,质量最大的是___________ 。
A.6 g H2; B.0.5 mol CO2; C.1.20×1024个HCl分子;D.148 g H2SO4; E.92 g乙醇(C2H5OH); F.4 ℃时10 mL水
(2)12.4 g Na2R含Na+0.4 mol,则Na2R的摩尔质量为___________ ,R的相对原子质量为___________ 。含R的质量为1.6 g的Na2R,其物质的量为___________ 。
(3)将10.6gNa2CO3溶于水配成100 mL溶液,该溶液的物质的量浓度是___________ ,Na+离子的物质的量的浓度___________ ;取10 mL该溶液,物质的量的浓度是___________ ,其物质的量是___________ 。
A.6 g H2; B.0.5 mol CO2; C.1.20×1024个HCl分子;D.148 g H2SO4; E.92 g乙醇(C2H5OH); F.4 ℃时10 mL水
(2)12.4 g Na2R含Na+0.4 mol,则Na2R的摩尔质量为
(3)将10.6gNa2CO3溶于水配成100 mL溶液,该溶液的物质的量浓度是
您最近一年使用:0次
2 . 阿伏加 德罗常数的值近似为6.02×1023。按要求完成下列填空:
(1)1molCl2中约含有__ 个氯气分子,约含有个__ 氯原子;含有6.02×1023个氢原子的H2SO4的物质的量是__ 。
(2)某硫酸钠溶液中含有3.01×1023个Na+,则该溶液中SO 的物质的量是
的物质的量是__ 。
(3)含2molMgCl2的溶液中Mg2+的物质的量为__ ,Cl-的物质的量为__ 。
(4)三种盐的混合溶液中含有0.2molNa+、0.25molMg2+、0.4molCl-、xmolSO ,则SO
,则SO 的个数约为
的个数约为__ 。
(1)1molCl2中约含有
(2)某硫酸钠溶液中含有3.01×1023个Na+,则该溶液中SO
 的物质的量是
的物质的量是(3)含2molMgCl2的溶液中Mg2+的物质的量为
(4)三种盐的混合溶液中含有0.2molNa+、0.25molMg2+、0.4molCl-、xmolSO
 ,则SO
,则SO 的个数约为
的个数约为
您最近一年使用:0次
解题方法
3 . 用石墨作电极电解100mL只含有以下离子(未考虑水的电离)的溶液,
①表中x=________ 。
②电解一段时间后,当阴极收集到0.3mol的气体时(忽略电极产物可能存在的溶解现象),收集到O2的物质的量为________ mol。
| 离子 | Cu2+ | H+ | Cl﹣ | SO |
| c/mol•L﹣1 | 1 | 6 | 4 | x |
①表中x=
②电解一段时间后,当阴极收集到0.3mol的气体时(忽略电极产物可能存在的溶解现象),收集到O2的物质的量为
您最近一年使用:0次
4 . (1)今有五种物质:①铜线 ②熔化的NaCl ③NaCl晶体 ④氨气 ⑤液态氯化氢,其中能导电的物质是__ ;属于电解质的是___ ;属于非电解质的是___ 。
(2)0.5molH2SO4的质量是__ g,能中和___ molNaOH,该硫酸所含氢元素的质量与___ molNH3中所含氢元素的质量相同。
(3)相同质量的CH4和H2S中分子个数比为___ 。
(4)在KCl、MgCl2、Mg(NO3)2形成的混合溶液中,n(K+)=0.2mol,n(Mg2+)=0.15mol,n(Cl-)=0.2mol,则n(NO3-)为( )
A.0.05mol B.0.20mol C.0.30mol D.0.40mol
(2)0.5molH2SO4的质量是
(3)相同质量的CH4和H2S中分子个数比为
(4)在KCl、MgCl2、Mg(NO3)2形成的混合溶液中,n(K+)=0.2mol,n(Mg2+)=0.15mol,n(Cl-)=0.2mol,则n(NO3-)为
A.0.05mol B.0.20mol C.0.30mol D.0.40mol
您最近一年使用:0次
18-19高一·浙江·期末
5 . 医院处方药“复方电解质注射液”可作为水、电解质的补充源,注射液中含有NaCl、MgCl2和KCl三种无机盐,其中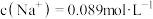 。
。
(1)若实验室药配制该电解质注射液500mL,所需的玻璃仪器有:玻璃板、烧杯和_______ ,需用托盘天平称量氯化钠固体___________ g;
(2)已知该注射液中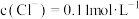 ,
,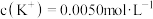 ,则
,则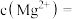
________  。
。
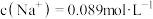 。
。(1)若实验室药配制该电解质注射液500mL,所需的玻璃仪器有:玻璃板、烧杯和
(2)已知该注射液中
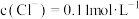 ,
,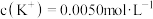 ,则
,则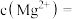
 。
。
您最近一年使用:0次



