解题方法
1 . 水溶液广泛存在于生命体及其赖以生存的环境中。弱电解质的电离平衡、盐类的水解平衡和难溶电解质的沉淀溶解平衡都与日常生活、工农业生产等息息相关。回答下列问题:
(1)25℃时, 溶液呈酸性的原因是
溶液呈酸性的原因是_______ (用离子方程式表示),把 溶液蒸干并灼烧得到的固体产物是
溶液蒸干并灼烧得到的固体产物是_______ (填化学式),该固体产物可用作_______ (填一种常见的用途)。
(2)25℃时,柠檬酸(用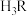 表示)为三元弱酸,其电离常数:
表示)为三元弱酸,其电离常数: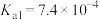 ,
,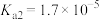 ,
,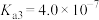 ;电离常数的负对数:
;电离常数的负对数: ,
,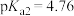 ,
, 。
。
①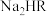 溶液呈
溶液呈_______ (填“酸”、“中”或“碱”)性,原因是_______ (结合计算分析)。
②在含有浓度均为 的
的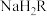 和
和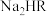 的混合液中,
的混合液中,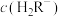
_______ (填“<”、“>”或“=”)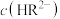 ;
;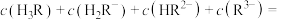
_______ (填写准确数值,下同);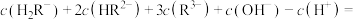
_______ 。
③当 时,溶液的pH=
时,溶液的pH=_______ 。(保留三位有效数字,已知: )
)
(1)25℃时,
 溶液呈酸性的原因是
溶液呈酸性的原因是 溶液蒸干并灼烧得到的固体产物是
溶液蒸干并灼烧得到的固体产物是(2)25℃时,柠檬酸(用
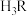 表示)为三元弱酸,其电离常数:
表示)为三元弱酸,其电离常数: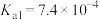 ,
,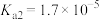 ,
,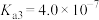 ;电离常数的负对数:
;电离常数的负对数: ,
,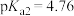 ,
, 。
。①
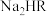 溶液呈
溶液呈②在含有浓度均为
 的
的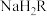 和
和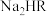 的混合液中,
的混合液中,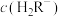
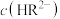 ;
;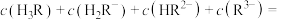
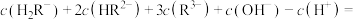
③当
 时,溶液的pH=
时,溶液的pH= )
)
您最近一年使用:0次
2022-11-30更新
|
417次组卷
|
2卷引用:河南省创新联盟2022-2023学年高二上学期第三次联考化学试题
2 . Na2CO3、NaHCO3及xNa2CO3·yH2O2 (过碳酸钠)在工农业生产上用途非常广泛。
(1)0.1mol·L-1Na2CO3溶液加水稀释时,溶液的pH___________ (填“增大”、“减小”或“不变”)。
(2)25℃时,H2CO3的电离常数Ka1=5×10-7,Ka2=5×10-11,NH3·H2O的电离常数Kb=1.8×10-5,计算下列平衡常数。
①NaHCO3水解反应HCO3-+H2O H2CO3+OH-的平衡常数为K=
H2CO3+OH-的平衡常数为K=___________ (填数值)。
②反应HCO3-+NH3·H2O CO32-+NH4++H2O的平衡常数为K=
CO32-+NH4++H2O的平衡常数为K=___________ (填数值)。
(3)一种测定xNa2CO3·yH2O2中y/x值的方法如下:
①滴定CO 时,终点溶液颜色变化是
时,终点溶液颜色变化是___________ 。
②滴定H2O2时,MnO 被还原为Mn2+,反应的离子方程式为
被还原为Mn2+,反应的离子方程式为___________ 。
③若消耗盐酸25.00mL,消耗KMnO4溶液19.00mL。计算y/x的值(列出计算过程)。
(1)0.1mol·L-1Na2CO3溶液加水稀释时,溶液的pH
(2)25℃时,H2CO3的电离常数Ka1=5×10-7,Ka2=5×10-11,NH3·H2O的电离常数Kb=1.8×10-5,计算下列平衡常数。
①NaHCO3水解反应HCO3-+H2O
 H2CO3+OH-的平衡常数为K=
H2CO3+OH-的平衡常数为K=②反应HCO3-+NH3·H2O
 CO32-+NH4++H2O的平衡常数为K=
CO32-+NH4++H2O的平衡常数为K=(3)一种测定xNa2CO3·yH2O2中y/x值的方法如下:

①滴定CO
 时,终点溶液颜色变化是
时,终点溶液颜色变化是②滴定H2O2时,MnO
 被还原为Mn2+,反应的离子方程式为
被还原为Mn2+,反应的离子方程式为③若消耗盐酸25.00mL,消耗KMnO4溶液19.00mL。计算y/x的值(列出计算过程)。
您最近一年使用:0次



