名校
解题方法
1 . 已知 在
在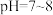 时溶解度最小。某工厂利用钒铬渣提取液(主要成分为
时溶解度最小。某工厂利用钒铬渣提取液(主要成分为 和
和 )制备
)制备 和
和 晶体,流程如下:
晶体,流程如下:
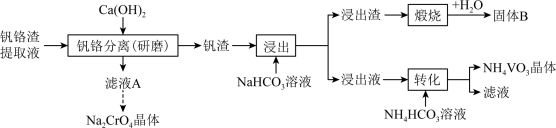
不同温度下相关物质的溶解度
(1)关于“钒铬分离”过程,下列说法正确的是_______。
(2)从滤液A中获取 晶体时,应采用的结晶方法为
晶体时,应采用的结晶方法为_______ ;残留的含铬废水不能直接排放,处理时需要经过“酸化→还原→沉降”三个步骤用 溶液还原时,还原产物为
溶液还原时,还原产物为 ,则反应的离子方程式
,则反应的离子方程式_______ 。
(3)钒渣成份是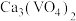 ,“浸出”过程中生成
,“浸出”过程中生成 的离子方程式为
的离子方程式为_______ 。
(4)“转化”过程中选用 溶液不选用
溶液不选用 溶液的可能原因为
溶液的可能原因为_______ 。(写一条原因即可)
(5)该流程中可循环利用的物质有_______ 。
(6)研究表明 固体(固体的组成用
固体(固体的组成用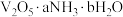 表示)热分解得到
表示)热分解得到 的过程可分为四步,每一步产生
的过程可分为四步,每一步产生 和
和 的物质的量之比依次为2∶1、3∶1、3∶2、3∶2,取
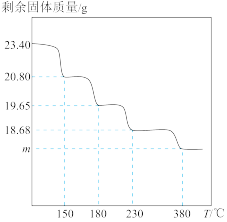
的物质的量之比依次为2∶1、3∶1、3∶2、3∶2,取 固体进行热重分析,剩余固体质量与温度关系如图,
固体进行热重分析,剩余固体质量与温度关系如图, 时剩余固体的组成可表示为:
时剩余固体的组成可表示为:_______ 。
 在
在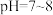 时溶解度最小。某工厂利用钒铬渣提取液(主要成分为
时溶解度最小。某工厂利用钒铬渣提取液(主要成分为 和
和 )制备
)制备 和
和 晶体,流程如下:
晶体,流程如下:
不同温度下相关物质的溶解度
 |  | 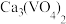 | 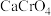 | |
 | 19.3 | 84.0 | 0.1 | 5.5 |
 | 22.5 | 96.5 | 0.09 | 2.49 |
 | 26.3 | 102 | 0.09 | 1.3 |
A.研磨可防止生成的沉淀覆在 表面,提高 表面,提高 利用率 利用率 |
| B.研磨减小了所得钒渣的粒径,提高了后续步骤中钒渣的浸出率 |
C.相对于 、 、 ,工业上更宜选用 ,工业上更宜选用 |
| D.该过程发生了氧化还原反应 |
 晶体时,应采用的结晶方法为
晶体时,应采用的结晶方法为 溶液还原时,还原产物为
溶液还原时,还原产物为 ,则反应的离子方程式
,则反应的离子方程式(3)钒渣成份是
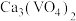 ,“浸出”过程中生成
,“浸出”过程中生成 的离子方程式为
的离子方程式为(4)“转化”过程中选用
 溶液不选用
溶液不选用 溶液的可能原因为
溶液的可能原因为
(5)该流程中可循环利用的物质有
(6)研究表明
 固体(固体的组成用
固体(固体的组成用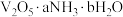 表示)热分解得到
表示)热分解得到 的过程可分为四步,每一步产生
的过程可分为四步,每一步产生 和
和 的物质的量之比依次为2∶1、3∶1、3∶2、3∶2,取
的物质的量之比依次为2∶1、3∶1、3∶2、3∶2,取 固体进行热重分析,剩余固体质量与温度关系如图,
固体进行热重分析,剩余固体质量与温度关系如图, 时剩余固体的组成可表示为:
时剩余固体的组成可表示为:
您最近一年使用:0次
2 . 下列实验操作及现象,能推出相应结论的是
| 选项 | 实验操作及现象 | 结论 |
| A | 常温下,用pH计测得0.1mol·L-1NaClO溶液和0.1mol·L-1CH3COONa溶液的pH,前者大 | 酸性:CH3COOH>HClO |
| B | 向淀粉溶液中加入稀硫酸并加热,再加入银氨溶液,水浴加热,未见有银镜产生 | 淀粉没有水解 |
| C | 向MgCl2溶液中滴加足量NaOH溶液,有白色沉淀生成;再滴加CuCl2溶液,有蓝色沉淀生成 | Ksp[Cu(OH)2]<Ksp[Mg(OH)2] |
| D | 向Fe(NO3)2样品,溶于稀硫酸,滴加KSCN溶液,溶液变红 | Fe(NO3)2样品溶于稀硫酸前已氧化变质 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2018-03-15更新
|
404次组卷
|
3卷引用:辽宁省丹东市2018届高三一模考试理综-化学试题
名校
3 . I.氯化铁可用于金属蚀刻,污水处理。
(1)25℃时,FeCl3溶液显酸性,原因是(用离子方程式表示)_____ 。把FeCl3溶液蒸干灼烧得到的主要产物是____ 。
(2)为了探究外界条件对氯化铁水解平衡的影响,某研究性学习小组设计实验方案,获得如下数据:
下列说法正确的是______ (填序号)。
A.上述实验能判断出温度对氯化铁水解的影响。
B.表格中x>y>z
C.上述实验能得出:增大盐的浓度,水解平衡正向移动,水解程度越大。
II、滴定实验是化学学科中最重要的定量实验之一、葡萄酒中抗氧化剂残留量的测定,常采用氧化还原滴定法。葡萄酒常用Na2S2O5作抗氧化剂,测定某葡萄酒中抗氧化剂的残留量(以游离SO2计算)的方案如下:

往实验中加入盐酸的目的是将Na2S2O5转化成SO2;滴定过程中发生的反应是:I2+SO2+2H2O=2HI+H2SO4
(3)滴定时,I2溶液应装在_______ (“酸”或“碱”)式滴定管中,该滴定过程的指示剂是____ ,滴定终点的现象为______ 。
(4)实验消耗标准I2溶液50.00ml,所测样品中抗氧化剂的残留量(以游离SO2计算)为___ g·L-1。
(5)下列情形会造成测定结果偏高的是___________(填序号)。
(1)25℃时,FeCl3溶液显酸性,原因是(用离子方程式表示)
(2)为了探究外界条件对氯化铁水解平衡的影响,某研究性学习小组设计实验方案,获得如下数据:
| 实验 | c(FeCl3)/mol·L−1 | V(FeCl3)/mL | 温度/℃ | pH |
| 1 | 0.1 | 5 | 25 | x |
| 2 | 0.1 | 5 | 35 | y |
| 3 | 0.2 | 5 | 25 | z |
A.上述实验能判断出温度对氯化铁水解的影响。
B.表格中x>y>z
C.上述实验能得出:增大盐的浓度,水解平衡正向移动,水解程度越大。
II、滴定实验是化学学科中最重要的定量实验之一、葡萄酒中抗氧化剂残留量的测定,常采用氧化还原滴定法。葡萄酒常用Na2S2O5作抗氧化剂,测定某葡萄酒中抗氧化剂的残留量(以游离SO2计算)的方案如下:

往实验中加入盐酸的目的是将Na2S2O5转化成SO2;滴定过程中发生的反应是:I2+SO2+2H2O=2HI+H2SO4
(3)滴定时,I2溶液应装在
(4)实验消耗标准I2溶液50.00ml,所测样品中抗氧化剂的残留量(以游离SO2计算)为
(5)下列情形会造成测定结果偏高的是___________(填序号)。
| A.滴定持续时间稍长,溶液中部分HI被空气氧化 |
| B.盛装标准I2溶液的滴定管用蒸馏水洗净后,未润洗 |
| C.滴定前平视,滴定后俯视 |
| D.滴定前滴定管尖嘴有气泡滴定后气泡消失 |
您最近一年使用:0次



