名校
解题方法
1 . 氢化镁(MgH2)可用作供氢剂。某兴趣小组以工业废渣(主要成分是MgO,含Al2O3、FeO、Fe2O3、MnO和SiO2等杂质)为原料制备氢化镁的流程如下:

已知:SOCl2遇水反应生成SO2和HCl。请回答下列问题:
(1)滤渣A的主要成分是_______ (填化学式),SOCl2的作用是_______ 。
(2)滤液A和次氯酸钠反应生成MnO2的离子方程式为_______ 。
(3)将一定量的工业废渣溶于一定体积4mol·L-1盐酸中,相同时间内镁元素的浸出率与温度的关系如图所示。其他条件相同,温度高于40℃时,镁元素的浸出率降低的主要原因可能是_______ 。

(4)①试剂X宜选择_______ (填字母)。
A.NaOH B. MgO C. Mg(OH)2 D. NH3·H2O
②电热水器中的镁棒可防止内胆(主要成分是铁)被腐蚀,这种保护金属的方法叫做_______ 。
③已知:常温下,Ksp[Fe(OH)3]=4.0×10-38,Ksp[Al(OH)3]=1.0×10-34,假设滤液B中含等物质的量浓度的Al3+与Fe3+,加入试剂X产生Al(OH)3沉淀的质量与X的质量关系如图所示。其中符合题意的是_______ (填字母)。

(5)为充分回收金属元素,设计以滤渣C为原料制备高纯度氢氧化铝的较优合成路线如下。请在括号里填入合适试剂:①_______ ;②_______ 。
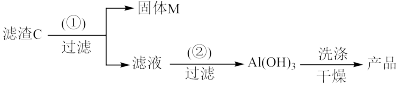

已知:SOCl2遇水反应生成SO2和HCl。请回答下列问题:
(1)滤渣A的主要成分是
(2)滤液A和次氯酸钠反应生成MnO2的离子方程式为
(3)将一定量的工业废渣溶于一定体积4mol·L-1盐酸中,相同时间内镁元素的浸出率与温度的关系如图所示。其他条件相同,温度高于40℃时,镁元素的浸出率降低的主要原因可能是

(4)①试剂X宜选择
A.NaOH B. MgO C. Mg(OH)2 D. NH3·H2O
②电热水器中的镁棒可防止内胆(主要成分是铁)被腐蚀,这种保护金属的方法叫做
③已知:常温下,Ksp[Fe(OH)3]=4.0×10-38,Ksp[Al(OH)3]=1.0×10-34,假设滤液B中含等物质的量浓度的Al3+与Fe3+,加入试剂X产生Al(OH)3沉淀的质量与X的质量关系如图所示。其中符合题意的是

(5)为充分回收金属元素,设计以滤渣C为原料制备高纯度氢氧化铝的较优合成路线如下。请在括号里填入合适试剂:①

您最近一年使用:0次
2021-03-07更新
|
787次组卷
|
2卷引用:辽宁省沈阳市东北育才学校2022-2023学年高三高考适应性测试(二)化学试题
2 . 科学家成功研制了太空用高强度延展合金——FeCoNiCr和C合金。某小组以镍废料(主要含Ni,还含少量Cu、Fe、Al等金属)为原料制备合成太空合金所用的镍,流程如图所示:

①已知几种金属氢氧化物沉淀的pH如表所示:
②镍的金属性介于镁和氢之间。
回答下列问题:
(1)“酸浸”时不用浓硫酸替代稀硫酸,其主要原因是___________ (答一条)。
(2)“滤渣2”的主要成分是NiO、___________ (填化学式)。
(3)如果省去 ,对该流程的影响是
,对该流程的影响是___________ 。
(4)下列试剂可以替代NiO的是___________(填标号)。
(5)“电解”时以石墨为电极,阳极的电极反应式为___________ 。
(6)雷尼镍(镍铝合金)是储氢材料,常作有机氢化反应的高效催化剂,制备雷尼镍的工艺流程如下:

①进行“操作X”时所用的玻璃仪器有___________ 。
②向“操作X”所得的“溶液”中缓慢通入 气体,产生沉淀的质量与
气体,产生沉淀的质量与 气体体积之间的关系如图所示,OA段不产生沉淀的原因是
气体体积之间的关系如图所示,OA段不产生沉淀的原因是___________ ;AB段的离子方程式为___________ 。


①已知几种金属氢氧化物沉淀的pH如表所示:
| 金属氢氧化物 |  |  |  |  |
| 开始沉淀的pH | 2.7 | 7.6 | 4.0 | 7.7 |
| 完全沉淀的pH | 3.7 | 9.6 | 5.2 | 9.5 |
回答下列问题:
(1)“酸浸”时不用浓硫酸替代稀硫酸,其主要原因是
(2)“滤渣2”的主要成分是NiO、
(3)如果省去
 ,对该流程的影响是
,对该流程的影响是(4)下列试剂可以替代NiO的是___________(填标号)。
A. | B. | C.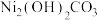 | D.CuO |
(6)雷尼镍(镍铝合金)是储氢材料,常作有机氢化反应的高效催化剂,制备雷尼镍的工艺流程如下:

①进行“操作X”时所用的玻璃仪器有
②向“操作X”所得的“溶液”中缓慢通入
 气体,产生沉淀的质量与
气体,产生沉淀的质量与 气体体积之间的关系如图所示,OA段不产生沉淀的原因是
气体体积之间的关系如图所示,OA段不产生沉淀的原因是
您最近一年使用:0次
3 . 氨是合成硝酸、铵盐和氮肥的基本原料,回答下列问题:
(1)氨的水溶液显弱碱性,其原因为_________ (用离子方程式表示),0.1 mol·L-1的氨水中加入少量的NH4Cl固体,溶液的pH _________ (填“升高”或“降低”);若加入少量的明矾,溶液中的NH4+的浓度_________ (填“增大”或“减小”)。
(2)硝酸铵加热分解可得到N2O和H2O,250℃时,硝酸铵在密闭容器中分解达到平衡,该分解反应的化学方程式为_________ ,平衡常数表达式为 _________ ;若有1mol硝酸铵完全分解,转移的电子数为_________ mol。
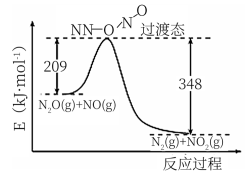
(3)由N2O和NO反应生成N2和NO2的能量变化如图所示,若生成1molN2, 其△H=_________ kJ·mol-1。
(1)氨的水溶液显弱碱性,其原因为
(2)硝酸铵加热分解可得到N2O和H2O,250℃时,硝酸铵在密闭容器中分解达到平衡,该分解反应的化学方程式为
(3)由N2O和NO反应生成N2和NO2的能量变化如图所示,若生成1molN2, 其△H=

您最近一年使用:0次
2019-01-30更新
|
1132次组卷
|
8卷引用:2016-2017学年辽宁沈阳东北育才学校高二阶段考一化学卷



