解题方法
1 . 室温下,有浓度均为 的下列五种溶液,请回答问题。
的下列五种溶液,请回答问题。
① ②
② ③
③ ④
④ ⑤
⑤
资料:室温下电离常数,醋酸 ;碳酸
;碳酸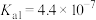 ,
, 。
。
(1)上述溶液加入水中,对水的电离无影响的是______ (填序号),溶液④中溶质与水作用的离子方程式为______ 。
(2)上述溶液的 由小到大的顺序为
由小到大的顺序为______ (填序号)。
(3)比较溶液③和④中 的物质的量浓度:③
的物质的量浓度:③______ ④(填“大于”、“等于”或“小于”)。
(4)室温下,向溶液①中加水稀释至原体积的100倍,所得溶液的 为
为______ 。
(5)向20mL0.1mol/L 中滴加0.1mol/L
中滴加0.1mol/L 过程中,
过程中, 变化如图所示。
变化如图所示。
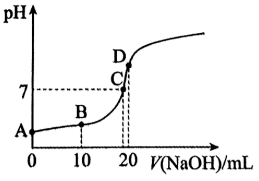
①滴加过程中发生反应的离子方程式是______ 。
②下列说法正确的是______ 。
a. 、
、 两点水的电离程度:
两点水的电离程度:
b. 点溶液中微粒浓度满足:
点溶液中微粒浓度满足: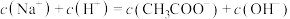
c. 点溶液微粒浓度满足:
点溶液微粒浓度满足: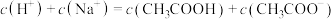
 的下列五种溶液,请回答问题。
的下列五种溶液,请回答问题。①
 ②
② ③
③ ④
④ ⑤
⑤
资料:室温下电离常数,醋酸
 ;碳酸
;碳酸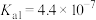 ,
, 。
。(1)上述溶液加入水中,对水的电离无影响的是
(2)上述溶液的
 由小到大的顺序为
由小到大的顺序为(3)比较溶液③和④中
 的物质的量浓度:③
的物质的量浓度:③(4)室温下,向溶液①中加水稀释至原体积的100倍,所得溶液的
 为
为(5)向20mL0.1mol/L
 中滴加0.1mol/L
中滴加0.1mol/L 过程中,
过程中, 变化如图所示。
变化如图所示。
①滴加过程中发生反应的离子方程式是
②下列说法正确的是
a.
 、
、 两点水的电离程度:
两点水的电离程度:
b.
 点溶液中微粒浓度满足:
点溶液中微粒浓度满足: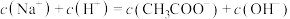
c.
 点溶液微粒浓度满足:
点溶液微粒浓度满足: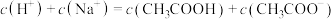
您最近一年使用:0次
名校
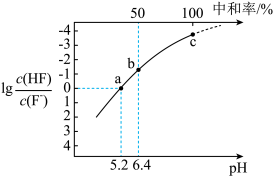
2 . 25℃时,向20 mL 0.2 HF溶液中逐滴加入浓度为0.2
HF溶液中逐滴加入浓度为0.2  的NaOH溶液,溶液中
的NaOH溶液,溶液中 、pH、中和率(中和率=
、pH、中和率(中和率= )变化如图。下列说法正确的是
)变化如图。下列说法正确的是
 HF溶液中逐滴加入浓度为0.2
HF溶液中逐滴加入浓度为0.2  的NaOH溶液,溶液中
的NaOH溶液,溶液中 、pH、中和率(中和率=
、pH、中和率(中和率= )变化如图。下列说法正确的是
)变化如图。下列说法正确的是
A.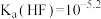 | B.水的电离程度:c点<b点 |
C.a点,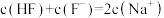 | D.b点,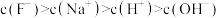 |
您最近一年使用:0次
2023-02-11更新
|
200次组卷
|
2卷引用:山东省泰安市新泰第一中学老校区2023-2024学年高二上学期第三次月考化学试题



