1 . 常温下,在含有 (s)的溶液中,一定pH范围内,存在平衡:
(s)的溶液中,一定pH范围内,存在平衡: ;
;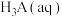
 ;
;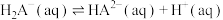 ;
;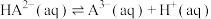 。平衡常数依次为
。平衡常数依次为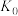 、
、 、
、 、
、 。已知
。已知 、
、 、
、 、
、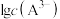 随pH变化关系如图所示。其中,
随pH变化关系如图所示。其中, 和
和 交点
交点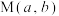 ,
, 和
和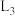 交点为
交点为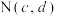 ,
, 和
和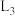 交点为
交点为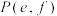 。下列说法错误的是
。下列说法错误的是
 (s)的溶液中,一定pH范围内,存在平衡:
(s)的溶液中,一定pH范围内,存在平衡: ;
;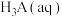
 ;
;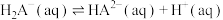 ;
;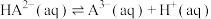 。平衡常数依次为
。平衡常数依次为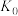 、
、 、
、 、
、 。已知
。已知 、
、 、
、 、
、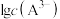 随pH变化关系如图所示。其中,
随pH变化关系如图所示。其中, 和
和 交点
交点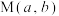 ,
, 和
和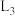 交点为
交点为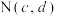 ,
, 和
和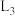 交点为
交点为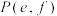 。下列说法错误的是
。下列说法错误的是
A.直线 表示 表示 的变化情况 的变化情况 |
B.N点时,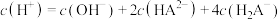 |
| C.随pH增大,溶液中含A微粒的总浓度一直增大 |
D. |
您最近一年使用:0次
名校
解题方法
2 . 回答下列问题:
(1)在质量分数为28%的KOH水溶液中,OH-与H2O数目之比是__ 。
(2)由硫酸钾、硫酸铁和硫酸组成的混合溶液,其中c(H+)=0.1mol/L,c(Fe3+)=0.3mol/L,c(SO )=0.6mol/L,则c(K+)为
)=0.6mol/L,则c(K+)为___ 。
(3)相同物质的量浓度的氯化钠、氯化镁、氯化铝溶液,分别与硝酸银溶液反应,当生成沉淀的质量之比为3∶2∶1时,消耗三种盐溶液的体积比为__ 。
(4)某状况下aL氨气(此时气体摩尔体积为Vm)溶解在一定量的水中形成bmL氨水溶液,所得溶液的密度为ρg/mL,则该氨水的物质的量浓度可表示为___ mol/L;氨水的质量分数为___ 。
(1)在质量分数为28%的KOH水溶液中,OH-与H2O数目之比是
(2)由硫酸钾、硫酸铁和硫酸组成的混合溶液,其中c(H+)=0.1mol/L,c(Fe3+)=0.3mol/L,c(SO
 )=0.6mol/L,则c(K+)为
)=0.6mol/L,则c(K+)为(3)相同物质的量浓度的氯化钠、氯化镁、氯化铝溶液,分别与硝酸银溶液反应,当生成沉淀的质量之比为3∶2∶1时,消耗三种盐溶液的体积比为
(4)某状况下aL氨气(此时气体摩尔体积为Vm)溶解在一定量的水中形成bmL氨水溶液,所得溶液的密度为ρg/mL,则该氨水的物质的量浓度可表示为
您最近一年使用:0次
名校
3 . 已知:pOH=-lgc(OH-)。室温下,将稀盐酸滴加到某一元碱(BOH)溶液中,测得混合溶液的pOH与离子浓度的变化关系如图所示。下列叙述错误的是
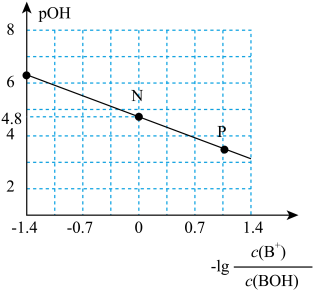

| A.BOH属于弱碱 |
| B.BOH的电离常数K=1×10-4.8 |
| C.P点所示的溶液中:c(Cl-)>c(B+) |
| D.N点所示的溶液中:c(H+)=c(Cl-)+c(OH-)-c(BOH) |
您最近一年使用:0次
2019-04-23更新
|
2075次组卷
|
6卷引用:陕西省西安中学2021-2022学年高三下学期第三次模拟考试理科综合化学试题



