1 . 工业采用氯化铵焙烧菱锰矿制备碳酸锰的流程如下图所示:
已知:①菱锰矿的主要成分是MnCO3 ,其中含Fe、Ca、Mg、Al等元素。
②焙烧过程中主要反应为:MnCO3 +2NH4Cl MnCl2+2NH3↑ +CO2↑+ H2O。
MnCl2+2NH3↑ +CO2↑+ H2O。
③部分阳离子沉淀时溶液的pH的值:
(1)实验室“焙烧”操作盛放固体的仪器为____________________ 。
(2)结合图1、2、3,分析焙烧过程中对温度、NH4Cl用量[m(NH4Cl):m(锰矿粉)]、时间的最佳选择依次为________________ 、_______________ 、______________ 。

(3)对锰浸出液净化除杂时,先加入MnO2将Fe2+转化为Fe3+,再调节溶液pH的范围为_________________ ,将Fe3+和Al3+变为沉淀除去。然后加入NH4F将Ca2+、Mg2+变为氟化物沉淀除去。
(4)“碳化结晶”步骤中,加入碳酸氢铵是反应的离子方程式为________________ 。
(5)上述流程中可循环使用的物质是_______________ 。
(6)为测定产品中碳酸锰的含量,设计如下实验(杂质不参加反应):实验步骤为:称取16.80g试样,溶于适量的稀硫酸溶液中,向所得溶液中加入稍过量的磷酸和硝酸,加热使反应:2Mn2++NO3-+4PO43-+2H+ 2[Mn(PO4)2]3-+NO2-+H2O充分进行。除去溶液中存在的NO3-和NO2-后,加入l00.00mL2.00 mol·L-1的(NH4)2Fe(SO4)2溶液,发生的反应为:[Mn(PO4)2]3-+Fe2+=Mn2++Fe3++2PO3-;再用1.00mol·L-1酸性K2Cr2O7溶液滴定过量的Fe2+,滴定终点时消耗10.00mL酸性K2Cr2O7溶液。
2[Mn(PO4)2]3-+NO2-+H2O充分进行。除去溶液中存在的NO3-和NO2-后,加入l00.00mL2.00 mol·L-1的(NH4)2Fe(SO4)2溶液,发生的反应为:[Mn(PO4)2]3-+Fe2+=Mn2++Fe3++2PO3-;再用1.00mol·L-1酸性K2Cr2O7溶液滴定过量的Fe2+,滴定终点时消耗10.00mL酸性K2Cr2O7溶液。
①酸性K2Cr2O7溶液与Fe2+反应的离子方程式为_____________________ (还原产物是Cr3+)。
②产品中碳酸锰的质量分数为_____________ (结果保留3位有效数字)。

已知:①菱锰矿的主要成分是MnCO3 ,其中含Fe、Ca、Mg、Al等元素。
②焙烧过程中主要反应为:MnCO3 +2NH4Cl
 MnCl2+2NH3↑ +CO2↑+ H2O。
MnCl2+2NH3↑ +CO2↑+ H2O。③部分阳离子沉淀时溶液的pH的值:
| Al3- | Fe3+ | Ca2+ | Mn2+ | Mg2+ | |
| 开始沉淀的pH值 | 4.1 | 2.2 | 10.6 | 8.8 | 9.6 |
| 沉淀完全的pH值 | 4.7 | 3.2 | 13.1 | 10.1 | 11.1 |
(1)实验室“焙烧”操作盛放固体的仪器为
(2)结合图1、2、3,分析焙烧过程中对温度、NH4Cl用量[m(NH4Cl):m(锰矿粉)]、时间的最佳选择依次为

(3)对锰浸出液净化除杂时,先加入MnO2将Fe2+转化为Fe3+,再调节溶液pH的范围为
(4)“碳化结晶”步骤中,加入碳酸氢铵是反应的离子方程式为
(5)上述流程中可循环使用的物质是
(6)为测定产品中碳酸锰的含量,设计如下实验(杂质不参加反应):实验步骤为:称取16.80g试样,溶于适量的稀硫酸溶液中,向所得溶液中加入稍过量的磷酸和硝酸,加热使反应:2Mn2++NO3-+4PO43-+2H+
 2[Mn(PO4)2]3-+NO2-+H2O充分进行。除去溶液中存在的NO3-和NO2-后,加入l00.00mL2.00 mol·L-1的(NH4)2Fe(SO4)2溶液,发生的反应为:[Mn(PO4)2]3-+Fe2+=Mn2++Fe3++2PO3-;再用1.00mol·L-1酸性K2Cr2O7溶液滴定过量的Fe2+,滴定终点时消耗10.00mL酸性K2Cr2O7溶液。
2[Mn(PO4)2]3-+NO2-+H2O充分进行。除去溶液中存在的NO3-和NO2-后,加入l00.00mL2.00 mol·L-1的(NH4)2Fe(SO4)2溶液,发生的反应为:[Mn(PO4)2]3-+Fe2+=Mn2++Fe3++2PO3-;再用1.00mol·L-1酸性K2Cr2O7溶液滴定过量的Fe2+,滴定终点时消耗10.00mL酸性K2Cr2O7溶液。①酸性K2Cr2O7溶液与Fe2+反应的离子方程式为
②产品中碳酸锰的质量分数为
您最近一年使用:0次
解题方法
2 . 铊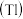 的价态分析及处理方法是环境保护研究的重点课题。
的价态分析及处理方法是环境保护研究的重点课题。
 三价铊各物种
三价铊各物种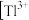 、
、 、
、 、
、 、
、 分布分数
分布分数 平衡时某物种的物质的量占各物种的总物质的量之和的分数
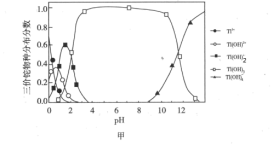
平衡时某物种的物质的量占各物种的总物质的量之和的分数 与pH的关系如图甲所示。当
与pH的关系如图甲所示。当 时,溶液中浓度最大的含铊物种是
时,溶液中浓度最大的含铊物种是___________  填化学式
填化学式 。
。
 铁盐、铁炭混合物、纳米
铁盐、铁炭混合物、纳米 均可作为去除废水中
均可作为去除废水中 和
和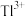 的吸附剂。
的吸附剂。
①铁炭混合物去除铊的原理是___________ 。若铁炭混合物中添加少量铝粉,铊的去除速率明显加快,其可能原因是___________ 。
②用纳米 去除水体中的
去除水体中的 和
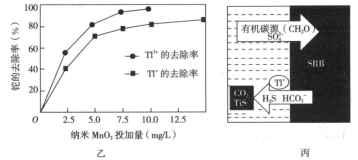
和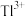 ,测得铊的去除率随
,测得铊的去除率随 投加量的变化关系如图乙所示。在纳米
投加量的变化关系如图乙所示。在纳米 用量不变的情况下,欲提高铊的去除效果,可采取的措施是
用量不变的情况下,欲提高铊的去除效果,可采取的措施是___________ 。
 通过沉淀法也可以去除工业废水中的
通过沉淀法也可以去除工业废水中的 和
和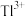 。
。
①利用硫酸盐还原菌 的催化作用,可以将废水中有机碳源
的催化作用,可以将废水中有机碳源 以
以 表示
表示 、
、 、
、 去除
去除 原理如图丙所示
原理如图丙所示 。写出该反应的离子方程式:
。写出该反应的离子方程式:___________ 。
② 工业污水铊的污染物排放限值为
工业污水铊的污染物排放限值为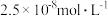 。已知:
。已知: ,若铊的含量符合国家排放限值,则处理后的废水中
,若铊的含量符合国家排放限值,则处理后的废水中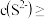
___________ 。
③ 向含铊废水中加入溴水,使
向含铊废水中加入溴水,使 充分氧化成
充分氧化成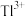 ,调节溶液pH,沉淀去除铊元素。若pH过大,铊元素去除率下降的原因是
,调节溶液pH,沉淀去除铊元素。若pH过大,铊元素去除率下降的原因是___________ 。
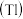 的价态分析及处理方法是环境保护研究的重点课题。
的价态分析及处理方法是环境保护研究的重点课题。  三价铊各物种
三价铊各物种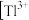 、
、 、
、 、
、 、
、 分布分数
分布分数 平衡时某物种的物质的量占各物种的总物质的量之和的分数
平衡时某物种的物质的量占各物种的总物质的量之和的分数 与pH的关系如图甲所示。当
与pH的关系如图甲所示。当 时,溶液中浓度最大的含铊物种是
时,溶液中浓度最大的含铊物种是 填化学式
填化学式 。
。

 铁盐、铁炭混合物、纳米
铁盐、铁炭混合物、纳米 均可作为去除废水中
均可作为去除废水中 和
和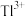 的吸附剂。
的吸附剂。①铁炭混合物去除铊的原理是
②用纳米
 去除水体中的
去除水体中的 和
和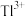 ,测得铊的去除率随
,测得铊的去除率随 投加量的变化关系如图乙所示。在纳米
投加量的变化关系如图乙所示。在纳米 用量不变的情况下,欲提高铊的去除效果,可采取的措施是
用量不变的情况下,欲提高铊的去除效果,可采取的措施是 通过沉淀法也可以去除工业废水中的
通过沉淀法也可以去除工业废水中的 和
和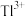 。
。①利用硫酸盐还原菌
 的催化作用,可以将废水中有机碳源
的催化作用,可以将废水中有机碳源 以
以 表示
表示 、
、 、
、 去除
去除 原理如图丙所示
原理如图丙所示 。写出该反应的离子方程式:
。写出该反应的离子方程式:②
 工业污水铊的污染物排放限值为
工业污水铊的污染物排放限值为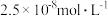 。已知:
。已知: ,若铊的含量符合国家排放限值,则处理后的废水中
,若铊的含量符合国家排放限值,则处理后的废水中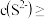
③
 向含铊废水中加入溴水,使
向含铊废水中加入溴水,使 充分氧化成
充分氧化成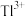 ,调节溶液pH,沉淀去除铊元素。若pH过大,铊元素去除率下降的原因是
,调节溶液pH,沉淀去除铊元素。若pH过大,铊元素去除率下降的原因是
您最近一年使用:0次



